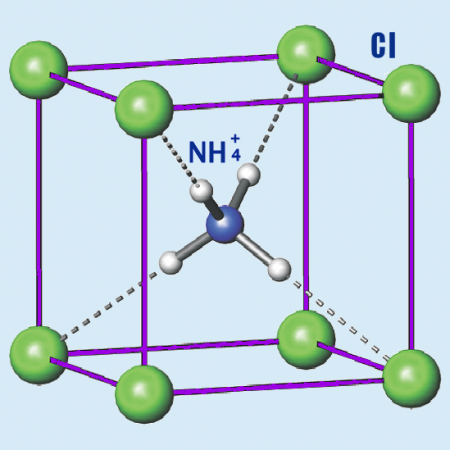
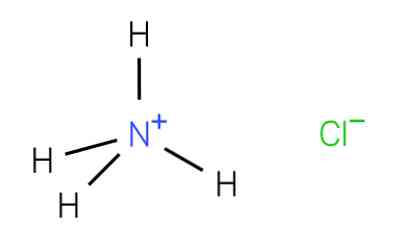
Соли аммония. Общая характеристика. Химические свойства.
Соли аммония.
Ион аммония образуется, когда аммиак, слабое основание, реагирует с кислотами Бренстеда (доноры протонов):
Таким образом, обработка концентрированных растворов солей аммония сильным основанием дает аммиак.
Когда аммиак растворяется в воде, его небольшое количество превращается в ионы аммония:
— если pH низкий, равновесие смещается вправо: больше молекул аммиака превращается в ионы аммония.
— если pH высокий, равновесие сдвигается влево: ион гидроксида отнимает протон от иона аммония, образуя аммиак.
Важно! Все соли аммония растворимы в воде, кроме гексахлороплатината аммония (раньше использовалось в качестве теста на NH4 + )
Наибольшее значение среди солей аммония в промышленности имеют хлорид аммония (NH4Cl), сульфат аммония ((NH4)2SO4), нитрат аммония (NH4NO3), характеристики которых мы сегодня и пройдем.
Уровень опасности: раздражающее средство
3) С щелочами (Ме АІ):
4) С щелочами (Ме АІІ):
5) С нерастворимыми основаниями:
6) C основаниями (комплексообразующими):
8) С солями летучих кислот:
9) С оксидами малоактивных Ме:
10) С оксидами активных Ме:
Уровень опасности: окислитель, раздражающее средство, экологически опасен
Уровень опасности: окислитель (взрывчатое вещество), раздражающее вещество
NH4NO 3
Хлорид аммония
Характеристики и физические свойства хлорида аммония
Рис. 1. Хлорид аммония. Внешний вид.
Основные характеристики хлорида аммония приведены в таблице ниже:
Молярная масса, г/моль
Температура плавления, o С
Растворимость в воде (20 o С), г/100 мл
Получение хлорида аммония
Получение хлорида аммония в промышленных масштабах заключается в упаривании маточного раствора, остающегося после отделения гидрокарбоната натрия, образующегося по следующей реакции:
В лабораторных условиях эту соль получают, используя такие реакции, как
Химические свойства хлорида аммония
Хлорид аммония – это средняя соль, образованная слабым основанием – гидроксидом аммония (NH4OH) и сильной кислотой – соляной (хлороводородной) (HCl). В водном растворе гидролизуется. Гидролиз протекает по катиону. Наличие катионов Н + свидетельствует о кислом характере среды.
NH4 + + Cl — + HOH ↔ NH4OH + Cl — + H + ;
При нагревании хлорид аммония как бы возгоняется – разлагается на аммиак и хлороводород, которые на холодных частях сосуда вновь соединяются в хлорид аммония:
Хлорид аммония разлагается концентрированной серной кислотой и щелочами:
Он реагирует с хлором (1), типичными металлами (2), оксидами (3) и нитритами металлов (4):
NH4Cl + 3Cl2 = Cl3N↑ + 4HCl (t = 60 – 70 o C) (1);
2NH4Cl + 4CuO = N2 + 4H2O + CuCl2 + 3Cu (t = 300 o C) (3);
Применение хлорида аммония
Хлорид аммония, или нашатырь, применяется в красильном деле, в ситцепечатании, при паянии и лужении, а также в гальванических элементах. Применение хлорида аммония при паянии основано на том, что он способствует удалению с поверхности металла оксидных пленок, благодаря чему припой хорошо пристает к металлу. При соприкосновении сильно нагретого металла с хлоридом аммония оксиды, находящиеся на поверхности металла, либо восстанавливаются, либо переходят в хлориды. Последние, будучи более летучи, чем оксиды, удаляются с поверхности металла. Для случая меди и железа основные происходящие при этом процессы можно выразить такими уравнениями:
Примеры решения задач
| Задание | Какую массу хлорида аммония можно получить при взаимодействии 17,7 г хлороводорода и 12 л аммиака (н.у.)? Какой объем 0,06М раствора можно приготовить из этой массы соли? |
| Решение | Запишем уравнение реакции: |
Найдем количество моль хлороводорода (молярная масса – 36,5 г/моль) и аммиака, вступивших в реакцию используя данные указанные в условии задачи:
n(HCl) = m (HCl) / M (HCl);
n (HCl) = 17,7 / 36,5 = 0,5моль.
n (NH3) = 12 / 22,4 = 0,54 моль.
Согласно уравнению задачи n (HCl):n (NH3) = 1:1. Это означает, что аммиак находится в избытке и все дальнейшие расчеты следует вести по хлороводороду. Найдем количество вещества и массу образовавшегося хлорида аммония (молярная масса 53,5 г/моль):
n (NH4Cl) = n (HCl) = 0,5моль.
Рассчитаем объем 0,06М раствора, который можно получить из 26,75 г хлорида аммония:
| Задание | Вычислите массовую долю хлорида аммония в растворе, полученном при растворении соли массой 40 г в воде количеством 20 моль. |
| Решение | Найдем массу воды (молярная масса 18г/моль): |
m (H2O)= 20 × 18 = 360 г.
Рассчитаем массу раствора хлорида аммония:
msolution(NH4Cl) = 40 + 360 = 400 г.
Вычислим массовую долю хлорида аммония в растворе:
ω (NH4Cl)=40 / 400 × 100% = 10%.
Копирование материалов с сайта возможно только с разрешения
администрации портала и при наличие активной ссылки на источник.
Соли аммония: получение и химические свойства
Соли аммония
Способы получения солей аммония
2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями.
Химические свойства солей аммония
NH4Cl ⇄ NH4 + + Cl –
Соли аммония реагируют с щелочами с образованием аммиака.
NH4Cl + KOH → KCl + NH3 + H2O
Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки.
Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония:
При температуре 250 – 300°C:
При температуре выше 300°C:
Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР):
Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Видеоопыт разложения дихромата аммония можно посмотреть здесь.
Хлорид аммония
наименование
Хлорид аммония (хлористый аммоний; техническое название — нашатырь; NH4Cl) — соль аммония, белый кристаллический слегка гигроскопичный порошок без запаха.
Содержание
Физические свойства
Бесцветные или белые кубические кристаллы. Растворимость (безводного вещества в безводном растворителе): в этаноле — 0,6 г/100 г, в метаноле — 3,3 г/100 г. Водные растворы вследствие гидролиза имеют слабокислую реакцию; хорошо растворим в жидком аммиаке.
| 0 °C | 10 °C | 20 °C | 30 °C | 40 °C | 50 °C | 60 °C | 70 °C | 80 °C | 90 °C | 100 °C |
|---|---|---|---|---|---|---|---|---|---|---|
| 29,4 | 33,3 | 37,2 | 41,4 | 45,8 | 50,4 | 55,2 | 60,2 | 65,6 | 71,3 | 77,3 |
При нагревании до 338 °C полностью распадается на NH3 и HCl (возгонка).
Химические свойства
Получение
В промышленности хлорид аммония получают упариванием маточного раствора, остающегося после отделения гидрокарбоната натрия NaHCO3 после реакции, в которой углекислый газ пропускают через раствор аммиака и хлорида натрия.
В лаборатории хлорид аммония получают взаимодействием хлороводорода с аммиаком при пропускании их через раствор NaCl.
Иногда используют реакцию взаимодействия аммиака с хлором:
Реакция взаимодействия аммиака и соляной кислоты:
Хлорид аммония (NH4Cl) формула, свойства, риски и использование
хлорид аммония, также известная как аммиачная соль, является неорганической солью в моче, формула которой NH4Кл. Встречается в минералогических образованиях и в таком виде называется аммиачной солью. Он также был найден в некоторых вулканических жерлах и пепла.
Это может быть получено различными методами. Первый заключается в нейтрализации с помощью HCl аммиачного остатка, образующегося при перегонке угля: NH3 + HCl → NH4Cl.
Вторая стратегия заключается в процессе Сольве для получения карбоната натрия (или бикарбоната) и где хлорид аммония образуется в качестве побочного продукта:
В процессе Solvay бикарбонат натрия выделяют фильтрацией, а затем кристаллизуется хлорид аммония, который остается в растворе (формула хлорида аммония, S.F.).
Ежегодно в Японии производится более 230 000 тонн хлорида аммония, где он в основном используется для удобрения при выращивании риса..
Физико-химические свойства
Соединение имеет триклинную сетчатую структуру с кубической структурой с центром в центре. Его молекулярная масса составляет 53 490 г / моль, его плотность составляет 1,5274 г / мл, а температуры плавления и кипения составляют 338 ° С и 520 ° С..
Хлорид аммония растворим в воде, способен растворять 383,0 г соединения на литр растворителя. Он также растворим в этаноле, метаноле и глицерине и мало растворим в ацетоне. Он нерастворим в органических растворителях, таких как этилацетат (Royal Society of Chemistry, 2015).
Хлорид аммония может подвергаться различным реакциям, имеющим большое значение для химической и фармацевтической промышленности. Может разлагаться при нагревании в соляной кислоте и аммиаке:
Кроме того, он может реагировать с основаниями, такими как гидроксид натрия или калия, с образованием газообразного аммиака:
Хлорид аммония считается кислой солью. Полученные растворы содержат умеренные концентрации ионов гидрония и имеют рН менее 7,0. Реагируют как кислоты, чтобы нейтрализовать основания.
Как правило, они не реагируют как окислители или восстановители, но такое поведение не является невозможным. Многие из этих соединений катализируют органические реакции (хлорид аммония, 2016 г.).
Реактивность и опасности
Хлорид аммония чрезвычайно ядовит и токсичен. Он вызывает повреждение органов при проглатывании или длительном воздействии, а также вреден для глаз. Он не воспламеняется и не реагирует с другими химическими веществами (Национальный институт безопасности и гигиены труда, 2014).
В случае попадания в глаза, следует проверить, носите ли вы контактные линзы, и немедленно снять их. Глаза следует промыть проточной водой не менее 15 минут, держа веки открытыми. Вы можете использовать холодную воду. Мазь не следует использовать для глаз.
Если химическое вещество попало на одежду, удалите его как можно быстрее, защищая свои руки и тело.
Поместите жертву под безопасный душ. Если химическое вещество накапливается на незащищенной коже жертвы, например на руках, оно осторожно моет загрязненную кожу проточной водой и неабразивным мылом. Вы можете использовать холодную воду. Если раздражение не проходит, обратитесь к врачу. Выстирать загрязненную одежду перед повторным использованием.
Если контакт с кожей серьезный, его следует промыть дезинфицирующим мылом и покрыть кожу, загрязненную антибактериальным кремом..
В случае вдыхания пострадавшему должно быть разрешено отдыхать в хорошо проветриваемом помещении. Если вдыхание является серьезным, пострадавшего следует как можно скорее эвакуировать в безопасное место. Ослабьте тесную одежду, такую как воротник рубашки, ремни или галстук.
Если пострадавшему трудно дышать, следует назначить кислород. Если пострадавший не дышит, проводится реанимация из уст в уста. Всегда принимая во внимание, что человеку, оказывающему помощь в проведении реанимации изо рта в рот, может быть опасно, когда вдыхаемый материал токсичен, инфекционен или вызывает коррозию.
В случае проглатывания не вызывать рвоту. Ослабьте тесную одежду, такую как воротники рубашки, ремни или галстуки. Если пострадавший не дышит, проведите реанимацию из уст в уста.
Во всех случаях вам следует немедленно обратиться к врачу (паспорт безопасности материала Хлорид аммония, 2013).
приложений
1- Медицина
Хлорид аммония выполняет очень важную биохимическую функцию: он поддерживает физиологический уровень pH.
Как кислотная соль, она может помочь исправить ситуации, в которых концентрация хлорид-ионов в плазме низкая или в случаях алкалоза крови (высокий уровень pH крови). Это может произойти после рвоты, всасывания (удаления) содержимого желудка, использования диуретиков (таблеток с водой или жидкостью) или при некоторых заболеваниях желудка..
Хлорид аммония также вызывает выведение излишков солей и воды через мочеиспускание и вызывает ацидоз в моче (делает его более кислым).
Хлорид аммония также используется для уменьшения отека или увеличения веса, которое происходит до менструации, и в качестве помощи при лечении инфекций мочевыводящих путей (Университет Юты, 2017).
Это компонент многих лекарств от простуды и кашля из-за его эффективности в качестве отхаркивающего средства. В ветеринарной медицине его используют для профилактики мочекаменной болезни у коз, крупного рогатого скота и овец (Encyclopædia Britannica, 2016).
2- Удобрения
Хлорид аммония в основном используется в качестве источника азота в удобрениях (что соответствует 90% мирового производства соединения), таких как хлораммонийфосфат, в основном для выращивания риса и пшеницы в Азии..
3- Металлургия
Хлорид аммония используется в качестве флюса при изготовлении металлов, которые должны быть покрыты оловом, оцинкованы или сварены. Он работает как флюс, очищая поверхность заготовок, реагируя с оксидами металлов на поверхности, образуя летучий хлорид металла..
Для этого он продается в блоках в хозяйственных магазинах для использования при чистке наконечника паяльника и может быть включен в припой в виде флюса..
4- компонент батареи
Хлорид аммония, NH4Cl, является компонентом сухих батарей, энергетических резервуаров, которые питают электрические устройства. Батареи позволяют вам использовать электричество, когда вы не находитесь рядом с электрической розеткой или розеткой.
Для каждой батареи есть три основных компонента: катод (верхняя часть вашей обычной батарейки АА, из которой текут электроны), анод (нижняя часть батареи АА, в которую текут электроны) и электролит для через которые могут двигаться электроны и ионы.
Когда хлорид аммония используется в качестве электролита в батарее, он превращается в водную пасту и помещается между катодом и анодом.
Химические реакции между катодами батареи и анодами заставляют электроны протекать через пасту из хлорида аммония от катода к аноду.
Электроны проходят через металлические контакты в батарейном отсеке, заставляя электрическое оборудование работать (American Chemistry Council, Inc., 2005).
5- Еда
В некоторых странах хлорид аммония, под названием соль аммиака или разговорно сальмиакки, используется в качестве пищевой добавки под номером E E510, обычно в качестве дрожжевого питательного вещества при производстве хлеба.
Это пищевая добавка для крупного рогатого скота и ингредиент в питательной среде для дрожжей и многих микроорганизмов.
Хлорид аммония используется для придания вкуса темным конфетам, называемым соленой солодкой (очень популярным в скандинавских странах), для выпечки, чтобы дать бисквитам очень хрустящую текстуру, а в ликере Salmiakki Koskenkorva для ароматизации..
В Индии и Пакистане его называют «ношадер» и используют для улучшения свежести бутербродов, таких как самоса и джалеби.
6- Другое использование
Хлорид аммония можно найти в шампунях, красках и отбеливателях для волос, средствах для мытья и очищения тела, моющих средствах для лица, кондиционере, моющем средстве для мытья посуды, а также в маслах и солях для ванн..
Хлорид аммония также используется в травлении при изготовлении печатных плат, таких как огнетушитель. Он также является компонентом фейерверков, взрывчатых веществ и спичек, а также отвердителем в клеях на основе формальдегида..