секционный материал
Смотреть что такое «секционный материал» в других словарях:
ТУБЕРКУЛЕЗ — ТУБЕРКУЛЕЗ. Содержание: I. Исторический очерк. 9 II. Возбудитель туберкулеза. 18 III. Патологическая анатомия. 34 IV. Статистика. 55 V. Социальное значение туберкулеза. 63 VІ.… … Большая медицинская энциклопедия
ГОЛОД — ГОЛОД, термин, употребляющийся как для обозначения ощущения, сопровождающего определенное физиологическое состояние организма (см. Голодание), так и в разрезе социальном для обозначения массового явления, выражающегося в длительной… … Большая медицинская энциклопедия
холера — острое инфекционное заболевание человека, вызываемое холерным вибрионом (Vibrio cholerae). Как и все вибрионы, он имеет форму слегка изогнутой палочки, грамотрицателен, обладает активной подвижностью за счет единственного жгутика, хемоорганотроф … Словарь микробиологии
Микроскопи́ческие ме́тоды иссле́дования — способы изучения различных объектов с помощью микроскопа. В биологии и медицине эти методы позволяют изучать строение микроскопических объектов, размеры которых лежат за пределами разрешающей способности глаза человека. Основу М.м.и. составляет… … Медицинская энциклопедия
БОТУЛИЗМ — мед. Ботулизм острая бактериальная зоонозная инфекция. Клинически манифестные формы обусловлены воздействием экзотоксинов возбудителя на клетки нервной системы. Характеризуются парезами и параличами поперечно полосатой и гладкой мускулатуры,… … Справочник по болезням
ЛИСТЕРИОЗ — мед. Листериоз полиморфное инфекционное заболевание, протекающее с поражением нервных тканей или в виде ангинозно септической формы. Наиболее часто встречается во внутриутробном периоде (диссеминированный инфантильный листериоз), у новорождённых… … Справочник по болезням
ГРАФОЛОГИЯ — (от греч. grapho пишу и logos учение), научное изучение почерка у здоровых и б ных. Г., или «хирограммато мантия» (что в переводе с греч. означает «предсказание по рукописи») возникла как искусство определять характер и… … Большая медицинская энциклопедия
ЭХИНОКОНН — ЭХИНОКОНН, личиночный стадий ленточного червя Echinococcus granulosus (Batsch, 1786) (рис. 1). Глистное заболевание человека и ряда домашних и диких млекопитающих, зависящее от поселения Э. в разных органах и тканях (особенно часто в печени и… … Большая медицинская энциклопедия
БЦЖ — Бацилла Кальметта Герена при микроскопическом увеличении (БЦЖ, Японский субштамм). Окрашивание по методу Циля Нельсена. Маштаб увеличения: 1,000 (фото 23 … Википедия
МЕЛИОИАОЗ — мед. Мелиоидоз инфекционное заболевание из группы зооно зов, протекающее по типу септицемии с образованием абсце дирующих казеозных гранулём в различных органах. Заболевание относят к оппортунистическим инфекциям при СПИДе. Этиология Возбудитель… … Справочник по болезням
ХОЛЕРА — мед. Холера острое карантинное инфекционное заболевание, протекающее с тяжёлой диареей, рвотой, приводящими к обезвоживанию организма. Этиология Возбудитель подвижная грамотрицательная бактерия Vibrio cholerae (холерный вибрион, или запятая Коха) … Справочник по болезням
Как проводится гистологическое исследование: виды, методы, особенности
Злокачественные новообразования — это группа заболеваний, насчитывающая несколько тысяч видов опухолей разных типов и разной степени злокачественности. Они подразделяются на большие группы в зависимости от того из каких тканей они развиваются: если из эпителиальных (барьерных) — то это раки, если из соединительных тканей (мягких тканей и костей) – саркомы, если из лимфоидных (иммунных) – лимфомы/лейкозы. От того насколько правильно верифицирована опухоль (определен ее тип, степень злокачественности и другие характеристики) зависит правильность и эффективность лечения. Важную роль в этом играют гистологические исследования.
О том, как проходят гистологические исследования, какие задачи кроме диагностических они позволяют решать, что влияет на сроки их выполнения рассказывает заведующая патологоанатомическим отделением с прозектурой НМИЦ онкологии им. Н.Н. Петрова, к.м.н. Анна Сергеевна Артемьева.
Что служит материалом для патоморфологических (гистологических) исследований?
Процесс получения фрагмента ткани (биоптата) — биопсия – это несколько разных способов забора материала для гистологического исследования.
Биопсию внутренних органов делают под УЗИ-навигацией, либо с помощью хирургического вмешательства.
Как обрабатывают эти материалы для проведения гистологического исследования?
1 Этап. Фиксация — «консервирование» биоптата в формалине — специальном химическом растворе, который предотвращает гниение, позволяет сохранить структуры ткани.
Фиксация биоптата может занимать от 6 до 24 часов – в зависимости от его вида и размера.
Операционный материал фиксируется дольше, в несколько этапов. Сначала предварительная фиксация, которая занимает примерно 12 часов. Затем вырезка нужных фрагментов и повторная фиксация еще 24 часа.
Соотношение объема материала к объему формалина должно быть 1:20.
2 Этап. Процессинг — процесс обезвоживания, обезжиривания и пропитки материала парафином. Автомат перемещает кусочек материала из раствора в раствор.
В качестве растворов применяются: абсолютированный изопропиловый спирт (6-8 смен), ксилол (2 смены), расплавленный парафин (2 смены).
Программа разнится для «жирного» материала (к которым относятся, например, ткани молочной железы) и «нежирного» – 36 и 24 часа соответственно.
Процесс получения парафиновых блоков.
3 Этап. Изготовление парафинового блока. Кусок материала помещается в форму с расплавленным парафином (уже другим нежели во время процессинга – с более высокой температурой плавления) и охлаждается. Выполняется вручную, сложно ускорить.
4 Этап. Изготовление срезов. Толщина образца — кусочка ткани, залитого в парафин – 1-3 мм. Толщина каждого среза 4-5 мкм (0,004-0,005 мм). Выполняет лаборант с использованием специального инструмента – микротома.
Срезы монтируются на стекла и должны высохнуть.
Несмотря на то, что часть материала теряется при выравнивании в микротоме, при должном профессионализме, из одного образца — материала от одной биопсии, операционного материала от одной опухоли, возможно изготовить около 100 стекол (микропрепаратов).
Для чего делаются срезы?
Срезы делаются для рутинной окраски гематоксилинном и эозином, иммуногистохимического исследования и других видов исследований.
Срезы для всех исследований используются одинаковые, различается окраска, могут отличаться стекла, на которые они монтируются, так для ИГХ и FISH нужны специальные адгезивные стекла или заряженные стекла.
Блоки и стекла способны храниться долгие годы и использоваться для проведения дополнительных гистологических исследований, пересмотров, а также в научных целях.
Архив гистологических материалов собирается в НМИЦ онкологии им. Н.Н. Петрова с 1927 года и содержит более 10 млн единиц хранения (микропрепараты — стекла, парафиновые блоки, архивные карточки, влажный архив).
Какие виды гистологических исследований наиболее информативны?
Что позволяют определить разные виды гистологических исследований
Гистологическое исследование – что это такое?
Позволяет верифицировать опухоль – то есть определить из каких клеток она состоит (из какой ткани она развивается), степень ее дифференцировки (зрелости).
Рутинная окраска, выполняющаяся при гистологическом исследовании, позволяет выявить патологический процесс в анализируемом материале (биоптате, операционном материале):
Также, в большинстве случаев, благодаря рутинной окраске, можно определить степень злокачественности опухоли и, если она достаточно зрелая, то какова ее природа.
Окрашенные срезы под микроскопом
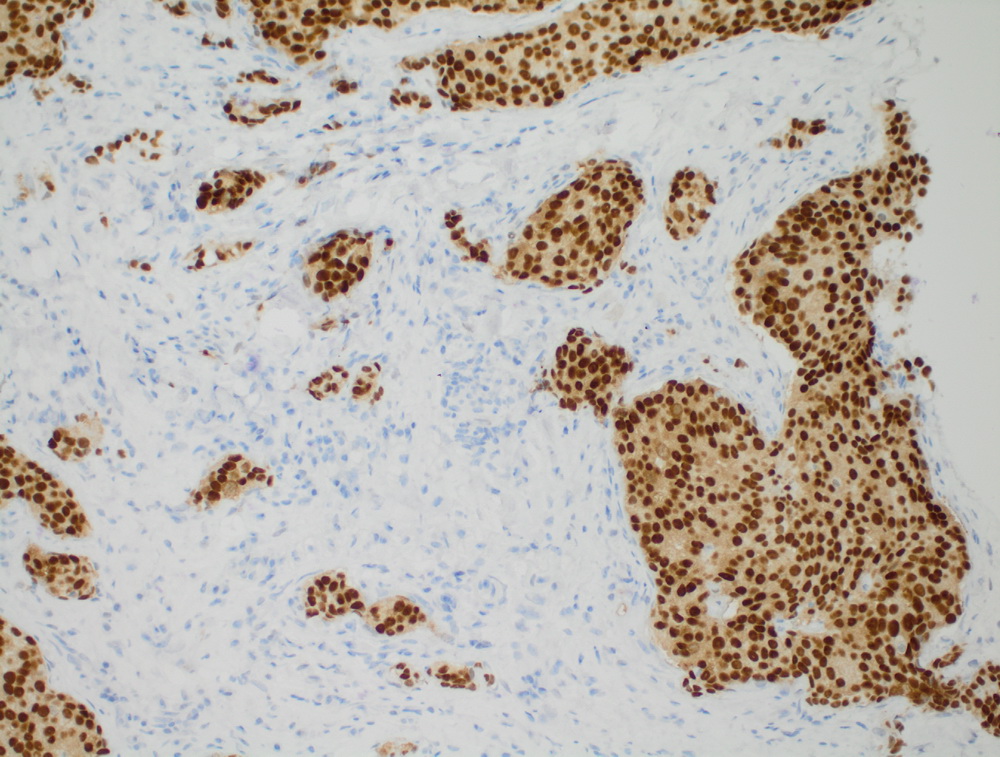 |
Инвазивный протоковый рак er 100%.
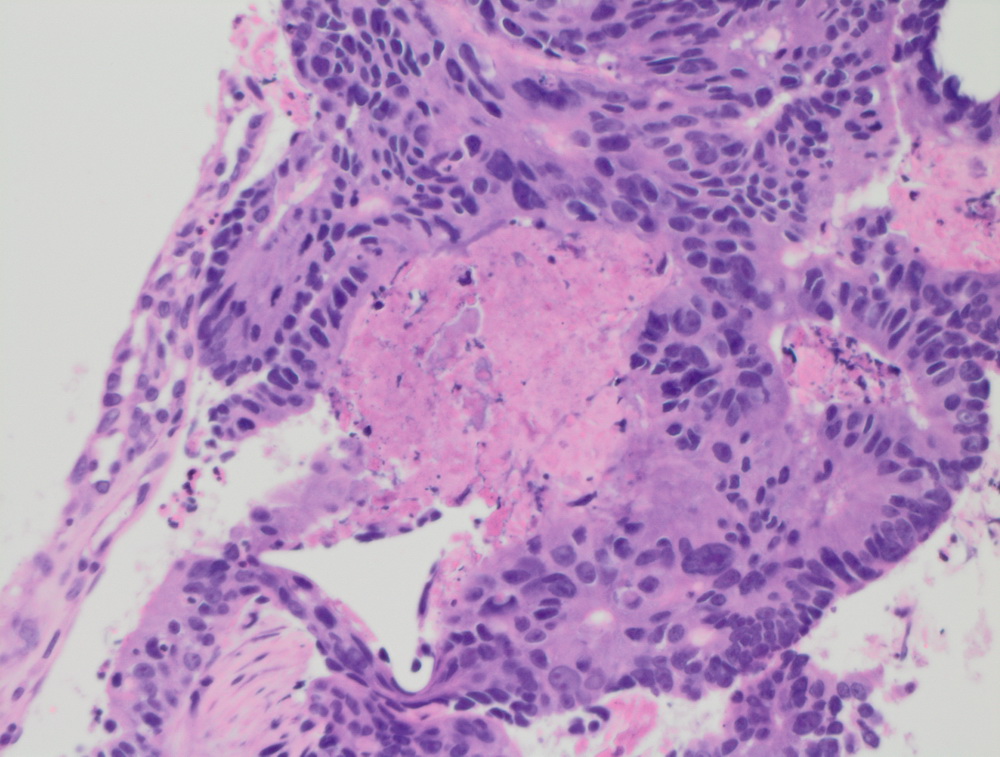
Карцинома сигмовидной кишки.
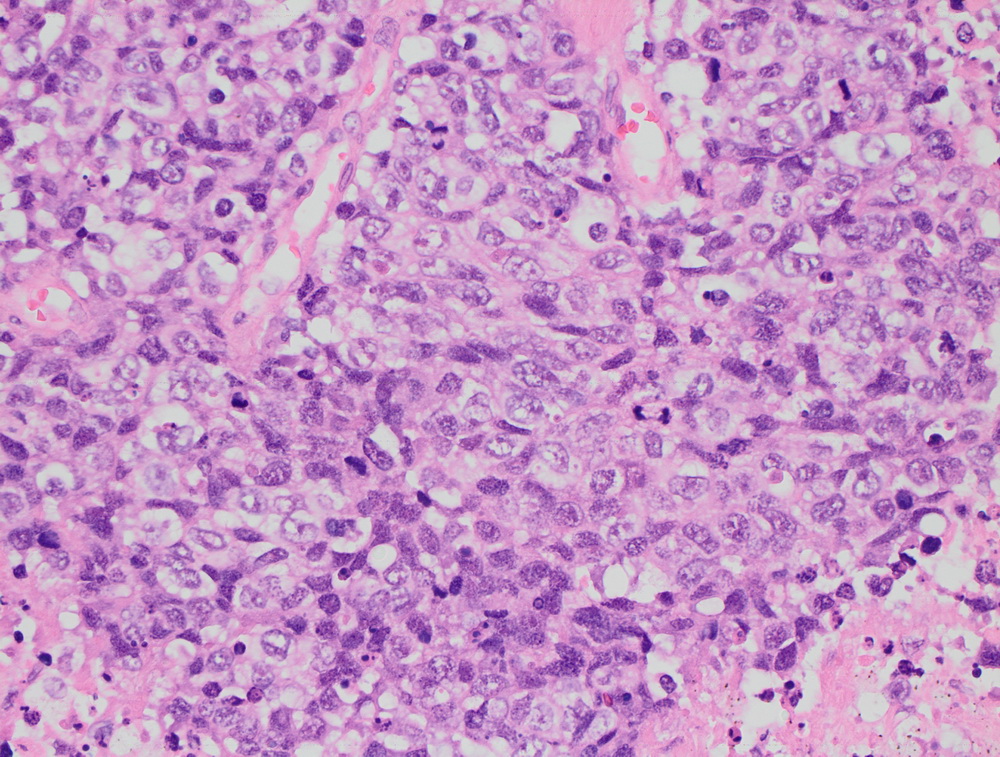
Крупноклеточная нейроэндокринная опухоль.
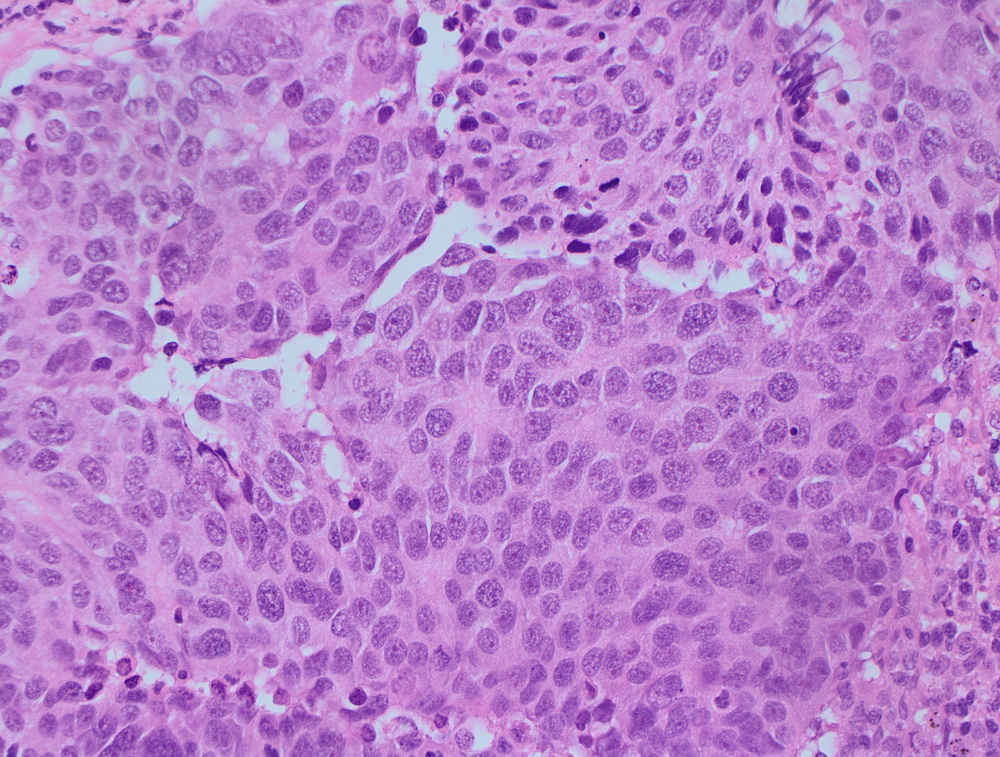
МТС крупноклеточной нейроэндокринной опухоли.
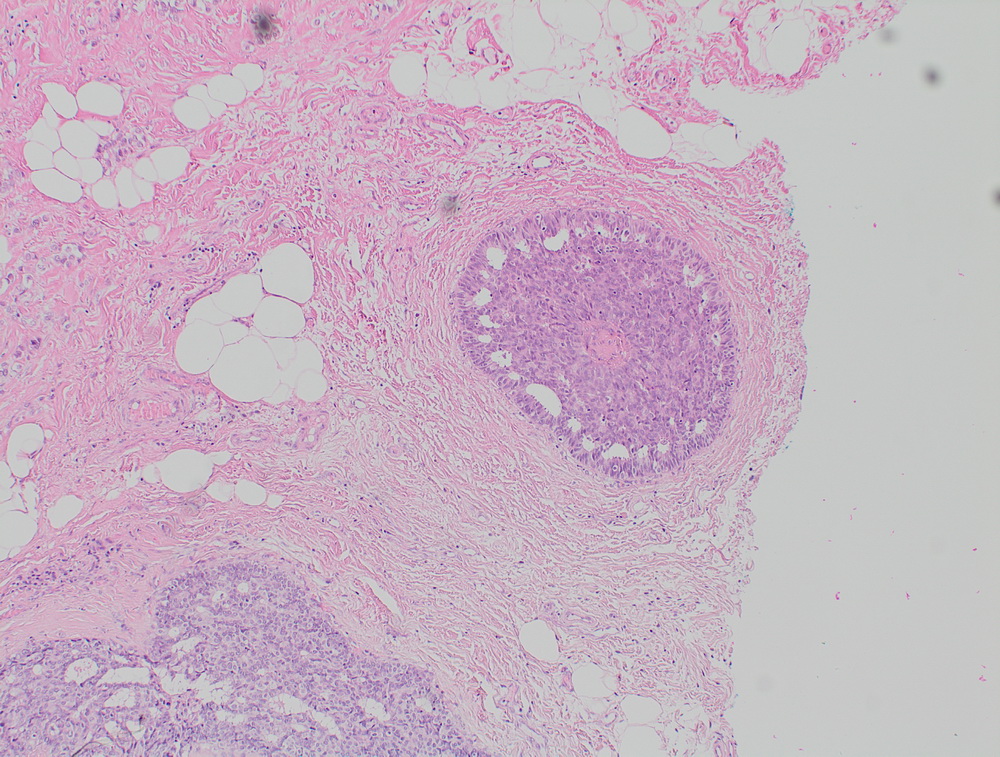
Неспецифический рак молочной железы. Участок in situ карциномы внутри протока, криброзного типа.
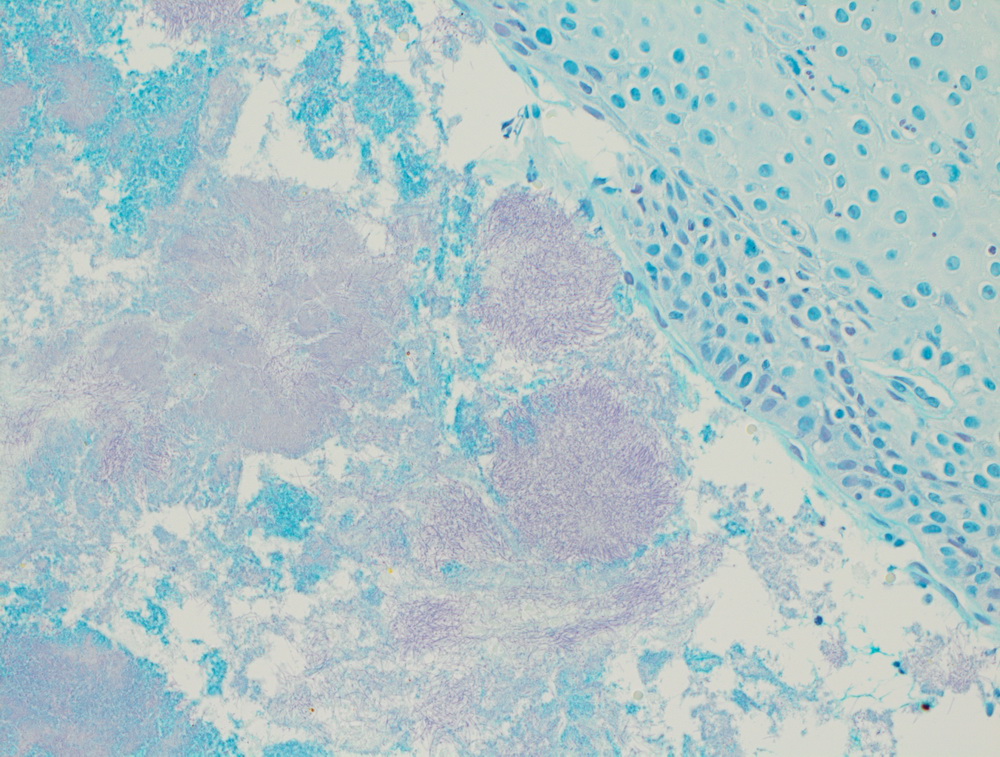
Низкодифферинцированный рак пищевода.
При гистологическом исследовании биоптата и операционного материала можно оценить распространенность: размер опухоли и прорастание в окружающие ткани, насколько затронуты лимфоузлы и есть ли метастазы в отдаленные органы (если эти все структуры присланы для гистологического исследования). При консультации готовых микропрепаратов – стекол, это, как правило, невозможно, если опухоль больше размеров гистологической кассеты или рассечена предыдущим исследователем и не предоставлены данные макроскопического исследования.
Во время гистологического исследования изучаются все стекла от одного образца – материала, полученного от одного вмешательства — одной операции или одной биопсии, вне зависимости от их количества, это считается одной консультацией.
Сроки выполнения гистологического исследования зависят от количества микропрепаратов и от категории сложности того процесса, который в них обнаруживается, сроки могут удлиняться, особенно при необходимости использования дополнительных методов исследования и анализа дополнительных сведений. На сроки выполнения гистологического исследования влияет полнота предоставленной пациентом клинической информации, в том числе данных уже проведенных исследований.
Иммуногистохимия (ИГХ)
Сложное многоэтапное исследование, выполняется после гистологического исследования на том же материале. Опухолевые срезы окрашиваются антителами, которые способны связываться антигенами (белками), которые несут опухолевые клетки. Разные опухолевые клетки несут разные антигены, к каждому из которых подобно ключа к замку подходит антитело.
Один из этапов ИГХ
ИГХ исследование — это комбинаторика. 100% специфичных и чувствительных к какой-то опухоли маркеров не существует, но есть набор антигенов, которые в определенном типе опухоль должны быть и набор тех, которых там быть не должно, таким образом ИГХ-панель строится так чтобы включать несколько антител, которые должны быть позитивны и несколько, которые должны быть негативны. Для разных опухолей различаются эти наборы позитивных/негативных маркеров.
При проведении прогностической ИГХ – выявлении маркеров чувствительности к терапии определяется набор таких маркеров для конкретных опухолей, например, рака молочной железы: рецепторы стероидных гормонов (эстроген, прогестерон), рецептор эпидермального фактора роста (HER2) и индекс пролиферативной активности Ki67 (скорости деления клеток).
Стекла окрашиваются последовательно — различными антителами красятся наборы маркеров в несколько этапов, процесс окраски стекол одним антителом занимает 48 часов.
Таким образом, каждое антитело наносится на отдельный срез ткани, монтированный на отдельное стекло, как правило с соответствующим внешним контролем, количество реакций (используемых антител) и этапов окраски может существенно варьировать в зависимости от конкретной диагностической ситуации, все зависит от индивидуальных особенностей опухоли. Проводится такое количество окрасок, которое необходимо для того, чтобы выявить наиболее характерный для определенной опухоли набор позитивных и негативных маркеров.
Кому-то для этого будет достаточно 5 антител, а кому-то необходимо сделать 20 окрасок и более. Максимальное количество окрасок, которое нам приходилось делать – 212.
Поэтому точные сроки и стоимость этого исследования невозможно определить заранее. Разные по течению и прогнозу опухоли могут быть очень похожи друг на друга, только минимальные различия в окрашивании, с учетом клинических данных и данных других методов обследования, могут позволить установить верный диагноз.
Есть целый ряд доброкачественных опухолей, симулирующих злокачественные, в том числе высокоагрессивные, а некоторые злокачественные высоко дифференцированные опухоли трудно отличить от воспалительных и реактивных процессов. В таких ситуациях только опыт и квалификация патоморфолога, анализ всего комплекса доступной информации (снимки КТ, МРТ, рентген, протокол операции, и др.) позволяют поставить диагноз.
В грамотной интерпретации результатов ИГХ очень важна роль эксперта, ведь те случаи, с которыми приходится работать, в большинстве своем, сложные. Практически не существует антител, которые могут выступать в качестве 100%-х маркеров той или иной опухоли, врачу всегда приходится взвешивать различные вероятности.
Что определяется с помощью ИГХ?
Иммуногистохимия позволяет оценить потенциальный темп роста опухоли, ответ на химио-, таргетную, гормональную терапию.
Флуоресцентная гибридизация in situ (FISH-тест)
Это метод молекулярно-генетической диагностики в ткани.
FISH проводится в срезе ткани и позволяет привязать генетическую перестройку к конкретной опухолевой клетке.
В этом тесте также используются специальные красители, которые связываются только с определенными участками хромосом. Их называют зондами, которые могут быть помечены флуоресцентным или хромогенным красителем, визуализирующимися при помощи флуоресцентного или светового микроскопа.
Технические операции по подготовке гистологических стекол к этому исследованию занимает 2 рабочих дня.
Анализ препарата с помощью многоголового микроскопа.
Полученные микропрепараты очень чувствительны к внешней среде – они могут выцвести со временем, чтобы избежать потерь информации все FISH-препараты сканируются, создается их цифровая копия, которая доступна для внешнего пересмотра. Специалисты просматривают флуоресцирующий материал в темном поле, в анализе препарата принимают участие как минимум 2 специалиста. При необходимости используется и цифровой анализ.
Что определяется с помощью FISH-теста?
FISH-тест позволят диагностировать некоторые виды опухолей, определяет целесообразность использования некоторых химиотерапевтических препаратов.
Проведение гистологического исследования, и в первую очередь FISH-теста — это экспертная работа, которая зависит от квалификации специалиста. Очень многие мутации, которые выявляются в опухолях, не всегда являются метками опухолей, они могут находиться и в доброкачественных образованиях или нормальных тканях.
За год патологоанатомическое отделение НМИЦ онкологии имени Н.Н. Петрова выполняет около 20000 гистологических исследований (пациентов), из них около 5000 консультативных случаев (пересмотров), более 30000 ИГХ исследований, а также участвует в программе внешнего контроля качества ИГХ исследований NordIQ.
Специалисты отделения обладают огромным опытом проведения гистологических исследований и экспертными компетенциями.
Скорость выполнения гистологических исследований и адекватность гистологического заключения зависят от ряда факторов:
После выполнения гистологического исследования пациент получает гистологическое заключение/протокол исследования гистологического материала.
Расшифровка гистологического исследования: на что обратить внимание?
Гистологическое заключение включает в себя несколько рубрик (полей):
Макроскопическое описание
Заполняется как для биоптатов — не обязательно, так и для операционного материала, для которого имеет крайне важное значение в ряде случаев.
Микроскопическое описание
Описание изменений на микроскопическом уровне, не обязательно к заполнению, так как вся необходимая информация может быть отражена в поле «заключение».
Результаты иммуногистохимического исследования
В этом поле описано какие антитела использовались в данном случае и каков результат окрашивания: наличие окрашивание или его отсутствие, локализация в клетке при необходимости, а также процент позитивных клеток и интенсивность реакции, когда это имеет значение.
Патологоанатомическое заключение
Содержит нозологическую/классификационную единицу, если ее возможно установить по исследованному материалу, то есть дает ответы на вопросы:
Также приводятся все необходимые прогностические данные: степень дифференцировки, параметры, влияющие на стадию, состояние краев резекции, если возможно их оценить и т.п.
Дополнительные замечания и рекомендации
Поле может содержать комментарии, относительно возможного направления дальнейшего обследования, вероятности того или иного диагноза, необходимости ознакомиться с теми или иными клиническими данными и др.
Мы не рекомендуем пациентам самостоятельно заниматься расшифровкой показателей гистологического исследования, используя информацию, полученную на различных Интернет-сайтах и форумах пациентов, так как на интерпретацию данных влияет большое количество факторов, в том числе, возраст пациента, данные других исследований и др.
Расшифровкой исследования может заниматься только специалист – врач онколог по профилю заболевания!
Авторская публикация:
АРТЕМЬЕВА АННА СЕРГЕЕВНА
заведующий патологоанатомического отделения с прозектурой ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, кандидат медицинских наук
Секционный материал что это
Порядок сбора, упаковки, хранения, транспортирования
и проведения лабораторного анализа биологического
материала от больных (и умерших) пациентов с подозрением
на тяжелый острый респираторный синдром (ТОРС)
Дата введения 2004-03-04
1. Разработаны: Департаментом госсанэпиднадзора Минздрава России (М.П.Шевырева, Ю.М.Федоров); Федеральным центром госсанэпиднадзора Минздрава России (Е.Н.Беляев, И.В.Брагина, Э.Ф.Опочинский, М.В.Зароченцева, Т.В.Воронцова); ЦНИИ эпидемиологии Минздрава России (В.В.Малеев, Н.а.Семина, Г.А.Шипулин); Центром специальной лабораторной диагностики и лечения особо опасных и экзотических инфекционных заболеваний (В.И.Марков, В.А.Меркулов).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Министерстве здравоохранения Российской федерации (протокол N 22 от 30.01.04).
1. Область применения
1.1. В настоящих методических указаниях определены порядок сбора, правила упаковки, хранения, транспортирования и лабораторной диагностики биологического материала от больных (и умерших) пациентов с подозрением на тяжелый острый респираторный синдром (ТОРС).
1.2. Методические указания предназначены для специалистов органов и учреждений государственной санитарно-эпидемиологической службы и лечебно-профилактических организаций, независимо от организационно-правовых форм и форм собственности.
2. Общие требования
3. Координация деятельности учреждений,
осуществляющих диагностику ТОРС
3.1. Первичное исследование материала от пациентов (умерших) методом ОТ-ПЦР и ИФА проводят на базе учреждений Госсанэпиднадзора в субъектах РФ в соответствии с порядком, указанным в п.6.
3.2. При получении положительных результатов исследований материал направляют в референтные лаборатории (прилож.1) для подтверждающего тестирования и депонирования. При этом:
— получение отрицательных результатов в подтверждающих тестах служит основанием для исключения диагноза ТОРС. При получении положительных результатов подтверждающих тестов диагноз ТОРС считают установленным. Результаты исследований в кратчайшие сроки передают в соответствующие учреждения Госсанэпиднадзора;
— полученную в ходе исследования комплементарную ДНК, образующуюся в результате реакции обратной транскрипции ДНК с участием фермента ревертазы, направляют в Центр молекулярной диагностики инфекционных заболеваний (Центральный НИИ эпидемиологии Минздрава России) для проведения секвенирования.
3.3. При установлении диагноза ТОРС абсолютной информативностью обладает метод прямого секвенирования к ДНК по различным областям генома вируса. При возникновении дискордантных результатов исследований на этом этапе Центром молекулярной диагностики инфекционных заболеваний проводится дополнительное исследование кДНК и образцов клинического материала, полученных на различных этапах исследований.
4. Правила сбора клинического (секционного) материала
4.1. Сбор клинического материала и все последующие манипуляции с ним осуществляет медицинский работник лечебно-профилактического учреждения стерильными одноразовыми инструментами в стерильные одноразовые флаконы, пробирки, контейнеры. Все виды работ проводят в одноразовых медицинских перчатках.
4.2. Способы сбора, условия хранения и транспортирования материала для проведения лабораторной диагностики ТОРС должны соответствовать требованиям СП 1.2.036-95 «Порядок учета, хранения, передачи и транспортирования микроорганизмов I-IV групп патогенности» и настоящих методических указаний (прилож.3).
4.3. В случаях, когда использование стабилизирующей (транспортной) среды является необходимым, сбор материала производят в пробирки со стабилизирующей средой, предоставляемой фирмой-производителем тест-систем. Недопустимо использование стабилизирующих сред других фирм.
4.4. Немедленно после сбора материала емкости с материалом необходимо плотно закрыть, не касаясь их внутренней поверхности и внутренней поверхности крышек.
5. Упаковка и транспортирование образцов
5.1. Все материалы, доставляемые в лабораторию, должны быть последовательно «дважды упакованы»:
— в транспортную емкость (плотно закрывающиеся пробирки или флаконы с завинчивающимися крышками). Плотно закрытый верхний конец транспортной емкости вместе с крышкой для надежности заклеивают, например, парафинизированным полиэтиленом (парафильмом);
— в пластиковый пакет подходящего размера вместе с небольшим количеством любого адсорбирующего материала, например, ваты. Пластиковый пакет следует заклеить или запаять.
5.2. Два или более образца от одного пациента могут быть упакованы в один пластиковый пакет. Не допускается упаковывать образцы материалов от разных людей в один и тот же пакет.
5.3. Заклеенные пакеты с образцами помещают внутрь дополнительного пластикового контейнера с завинчивающейся крышкой. Строго дважды упакованные образцы материалов от разных пациентов могут быть транспортированы в одном дополнительном контейнере. В дополнительный контейнер также следует положить некоторое количество адсорбирующего влагу материала.
5.4. Описание особенностей конкретного образца, полную информацию и добавочные сведения, касающиеся образцов, а также способ транспортирования и название лаборатории назначения приклеивают к наружной стенке, дополнительного контейнера.
5.5. Плотно закрытые пластиковые контейнеры с заклеенными крышками помещают в термоизолирующий контейнер (термос), приспособленный для транспортирования биологических материалов.
5.6. Термоконтейнеры и термосы укомплектовывают охлаждающими элементами или льдом. Сроки и условия транспортирования упакованных проб клинического материала указаны в прилож.3.
5.7. Каждую пробу материала сопровождают бланком направления по форме (прилож.4), прикрепленным к наружной стенке контейнера.
5.8. Транспортирование проб клинического материала в референтную лабораторию (референс-центр) для дальнейшего исследования с целью подтверждения результатов осуществляется нарочным, информированным о правилах доставки материала.
6. Порядок проведения лабораторных исследований
6.1. Лабораторные исследования с целью диагностики ТОРС следует проводить у пациентов с респираторными заболеваниями тяжелого течения и неясной этиологии при наличии следующего комплекса симптомов:
— фебрильная лихорадка (температура тела выше 38 °С);
— затрудненное дыхание или дыхательная недостаточность;
— наличие характерных изменений на рентгенограмме грудной клетки;
— отсутствие эффекта от антибиотиков при их использовании по принятой схеме.
6.2. Исследование секционного материала от умерших на наличие вируса ТОРС проводят:
— при наличии данных, указывающих на сходство клинической картины заболевания, приведшего к летальному исходу, с описанной в п.6.1;
— при невозможности исключения такой клинической картины в анамнезе и наличии указаний о предшествовавшем посещении регионов, в которых регистрировались случаи ТОРС. Список регионов, в которых регистрировались случаи ТОРС, приведен в прилож.2.
6.3. Первоочередному обследованию при наличии указанной клинической симптоматики подвергаются лица, недавно посещавшие регионы, в которых регистрировались случаи ТОРС.
6.4. Лабораторные исследования с целью диагностики ТОРС следует проводить также у лиц без клинических проявлений заболевания при наличии тесного контакта с подозреваемым на ТОРС больным.
6.5. Исследования проводят с использованием диагностических тест-систем, разрешенных к применению в установленном порядке.
6.6. При обследовании пациента до 10 дня от начала заболевания используют метод ОТ-ПЦР двукратно с интервалом 5 дней. Для повышения результативности анализа методом ОТ-ПЦР необходимо исследовать как минимум три вида клинического материала: мазок из носоглотки (или смыв из носоглотки), мокроту и фекалии. Дополнительно также может быть исследована плазма крови. Каждую пробу клинического материала тестируют трехкратно.
При получении хотя бы одного положительного результата пробу считают первично положительной. Дополнительное тестирование проб методом ИФА в этом случае не проводят. Пробы материала и полученную кДНК отправляют в референтную лабораторию.
При получении отрицательных результатов ОТ-ПЦР проводят исследование методом ИФА с тестированием сывороток, взятых на 10, 20 и 30 дни заболевания. Результат считают положительным при выявлении сероконверсии или увеличении титра антител в фазе реконвалесценции не менее чем в 4 раза по сравнению с острой фазой. При получении положительного результата ИФА пробы клинического материала отправляют в референтную лабораторию.
6.7. При начале обследования пациента после 10 дня заболевания проводят параллельное исследование материала методом ОТ-ПЦР двукратно с интервалом 5 дней и тестирование парных сывороток, взятых на 10, 20 и 30 дни заболевания методом ИФА.
При получении положительного результата при любом методе исследования пробы клинического материала и полученную кДНК отправляют в референтную лабораторию.
При получении двукратных отрицательных результатов ОТ-ПЦР с интервалом в 5 дней и отрицательных результатах ИФА на 10, 20 и 30 дни заболевания диагноз ТОРС может быть исключен.
6.8. Лабораторное обследование контактных лиц проводят на всем протяжении инкубационного периода предполагаемого заболевания.
6.9. Секционный материал (ткани легкого, сегментарные бронхи, кровь, образцы фекалий), собранный в кратчайшие сроки после наступления смерти, тестируют методом ПЦР. Каждый вид секционного материала тестируют трехкратно. В случае получения хотя бы одного положительного результата пробу считают первично положительной и в кратчайшие сроки направляют в референтную лабораторию с целью подтверждения (верификации).
6.10. В референтной лаборатории пробу клинического (секционного) материала, давшую положительный результат при первичном тестировании методом ОТ-ПЦР, дополнительно трехкратно анализируют методом ОТ-ПЦР с использованием тест-системы, использовавшейся при первичном скрининге.






