Сердечно-сосудистые заболевания и анемия
Анемия часто диагностируется у пациентов с кардиальной патологией. Накапливаются данные о том, что она может рассматриваться при сердечно-сосудистых заболеваниях как независимый предиктор риска неблагоприятных клинических исходов.
Anemia is often being diagnosed with patients with cardial pathology. It may be considered as independent predictor of unfavorable clinical outcome risk for cardio-vascular diseases according to data gathered.
Число случаев смерти от сердечно-сосудистых заболеваний (ССЗ) в мире продолжает расти. Заключение о том, что ишемическая болезнь сердца (ИБС) «…является ведущей причиной смерти во всем мире, ее уровень постоянно растет и в настоящее время достиг размеров пандемии, не знающей границ», появившееся на сайте Всемирной организации здравоохранения (ВОЗ) в 2009 г., воспринимается как все более актуальное. В 2011 г. ИБС стала причиной гибели 7,3 млн человек [1, 2].
Анемией в мире, по оценкам ВОЗ, страдает 1,62 млрд человек [3]. Частота анемии, также как ИБС, значительно увеличивается с возрастом. Признаки анемии имеют более 10% лиц старше 65 лет и до 50% пожилых пациентов с хроническими заболеваниями, проживающих в домах престарелых [4].
В практике врача терапевта и кардиолога часто встречается сочетание сердечно-сосудистой патологии с анемией. Анемия определяется у 25–40% больных с хронической сердечной недостаточностью (ХСН) и 10–20% пациентов с ИБС [5–7].
Вышедшие в последние два года европейские и американские рекомендации по ведению пациентов со стабильной стенокардией предполагают обязательное определение уровня гемоглобина у всех пациентов и рассматривают анемию как фактор, провоцирующий коронарную недостаточность [8, 9]. В последних рекомендациях по диагностике и лечению пациентов с ХСН американские и европейские эксперты отмечают, что анемия не только усиливает симптомы ХСН, ухудшает качество жизни пациентов, снижает толерантность к физической нагрузке, может являться причиной развития острой декомпенсации ХСН и увеличения частоты госпитализаций, но и является независимым негативным предиктором прогноза [10, 11]. Риск смерти при ХСН у больных с анемией в два раза выше, чем без нее даже при учете дополнительных переменных (почечная дисфункция, тяжесть ХСН и другие) [13]. Негативное влияние на прогноз при ХСН может оказывать уже латентный дефицит железа [14], что делает целесообразным определение его маркеров у всех пациентов с ХСН.
При остром коронарном синдроме наличие анемии может в четыре раза повышать вероятность смерти пациентов и рассматривается как независимый предиктор риска неблагоприятных клинических исходов [15, 16]. Даже синдром болей в груди у женщин при его сочетании с анемией оказывается более прогностически неблагоприятным (риск смерти увеличивается вдвое) [17].
Предоперационная анемия при кардиохирургических операциях определяет высокий риск последующего переливания крови и худшие результаты лечения, что делает актуальной задачи раннего выявления анемии и качественного, своевременного ее лечения [18].
Доказана роль анемии как независимого фактора риска неблагоприятного прогноза при фибрилляции предсердий у лиц пожилого и старческого возраста [19].
Как показал анализ влияния сочетания анемии и нарушения функции почек на ИБС в популяционном исследовании ARIC (The Atherosclerosis Risk in Communities Study), анемия встречается у лиц с незначительным и умеренным снижением функции почек намного чаще, чем предполагалось. А сочетание анемии и почечной дисфункции значимо повышает риск развития ИБС даже после учета таких известных факторов риска, как сахарный диабет, уровень липидов крови, артериальное давление и применение антигипертензивной терапии. В выводах подчеркивается необходимость своевременного выявления и лечения анемии для улучшения прогноза пациентов [20].
Неблагоприятное взаимное влияние ХСН, анемии и почечной дисфункции дало основание для выделения новых синдромов: «синдром кардиоренальной анемии», «кардиоренальный железодефицитный синдром» и даже «синдром кардиоренальной анемии и дефицита железа». Последние термины подчеркивают значение дефицита железа как самостоятельного фактора риска неблагоприятного прогноза при ХСН. Возможность непосредственного влияния дефицита железа на диастолическую функцию, гипертрофию, фиброз и дилатацию миокарда, уровень циркулирующего эритропоэтина, молекулярные сигнальные пути и активацию воспаления доказана в экспериментах на животных [21]. Такой широкий спектр негативных последствий дефицита железа, вероятно, связан с ролью железа в организме. Оно не только входит в состав гемоглобина и миоглобина, но и находится в ферментах, участвующих в процессах превращения аденозинтрифосфата в аденозиндифосфат, способствует транспорту электронов в митохондриальных цепях, определяет тканевой метаболизм и поглощение свободных радикалов [19]. Железо задействовано в иммунных реакциях, необходимо для миелинизации нервных волокон, синтеза ДНК [22, 23].
Анемия у лиц с сердечно-сосудистыми заболеваниями может иметь те же этиологические факторы, что и в целом в популяции. Дополнительную роль в развитии анемии при сердечно-сосудистой патологии могут играть характерные для нее более старший возраст пациентов, что само по себе связано с более низким значением гемоглобина, возрастающая частота хронической болезни почек, высокая распространенность сахарного диабета. Предполагается, что в развитие анемии при патологии сердечно-сосудистой системы вносят вклад: хронический воспалительный процесс (повышение синтеза провоспалительных цитокинов — фактора некроза опухоли альфа, интерлейкина-6), ишемическая депрессия костно-мозгового кроветворения, снижение синтеза эндогенного эритропоэтина вследствие почечной дисфункции. При ХСН в формировании анемии может играть роль гемодилюция с задержкой натрия и воды и нарушение всасывания железа и витаминов в кишечнике. Дополнительным фактором для развития анемии может быть проводимая медикаментозная терапия, вызывающая кровопотери (при приеме Аспирина, антикоагулянтов), снижение продукции эритропоэтина и чувствительности к нему костного мозга (при использовании блокаторов ренин-ангиотензин-альдостероновой системы) и т. д.
Актуальность вопроса ранней диагностики анемии у пациентов с сердечно-сосудистой патологией определяется тем, что запоздалое ее выявление приводит к задержке или отсутствию необходимого вмешательства в отношении потенциально корригируемого состояния.
Значительная часть пациентов с сердечно-сосудистой патологией имеют латентный дефицит железа, либо железодефицитную анемию (ЖДА) или сочетание этих состояний с другими видами анемий.
При лабораторной диагностике хронической ЖДА микроскопия мазка периферической крови выявляет микроцитарную гипохромную анемию с гипопролиферацией ретикулоцитов. Для подтверждения дефицита железа необходимо сниженное содержание железа и ферритина в сыворотке крови.
Лечение ЖДА направлено на терапию заболевания, лежащего в основе дефицита железа и собственно компенсацию дефицита железа.
Хотя пациентам с ЖДА необходимы диетические рекомендации, важно четко объяснить, что диета не является основой терапии. Наибольшее количество железа содержится в мясе (гемовое железо). Все остальные продукты содержат железа меньше, а, главное, всасывается оно из них значительно меньше (1–5% из яблок, 10–15% из яиц и рыбы при 25–30% из мяса).
В медикаментозной терапии ЖДА главным направлением было и остается применение препаратов железа. Выбор лекарственного препарата железа определяется его эффективностью (количеством и биодоступностью содержащегося в нем железа) и переносимостью. Необходимо поступление от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Препараты железа на отечественном рынке представлены гидроксиполимальтозным комплексом, железосорбитоловым комплексом, протеин сукцинилатом железа, железосахарозным комплексом. Для пациентов с кардиальной патологией крайне важно при проведении дополнительной медикаментозной терапии ЖДА, кроме высокой эффективности, отсутствие негативных лекарственных взаимодействий и хорошая переносимость препарата. Этим требованиям отвечает препарат Мальтофер — полимальтозный комплекс железа сульфата (ІІІ). Мальтофер — неионный препарат железа. Его абсорбция обеспечивается активным транспортом, без предварительной диссоциации в кишечнике, что позволяет исключить раздражающее действие на слизистую оболочку и избежать большинства нежелательных реакций со стороны желудочно-кишечного тракта, типичных для ионизированных препаратов железа [25, 26]. Мальтофер не взаимодействует ни с пищей, ни с другими лекарственными препаратами, а форма выпуска в виде жевательных таблеток позволяет применять его в любое время и в любой обстановке [27–30]. В то же время всасывание железа из других препаратов железа может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ — фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе), при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли кальция и магния), что требует приема этих лекарственных средств с учетом времени употребления пищи и указанных медикаментов. Препараты солей железа содержат двухвалентное железо, которое после поступления в кровь превращается в трехвалентное для последующего его включения в молекулу гемоглобина, что может сопровождаться образованием свободных радикалов и оказывать негативное влияние на физиологические процессы в различных органах и тканях [31]. Мальтофер содержит трехвалентное железо, непосредственно использующееся для построения молекулы гемоглобина, поэтому не имеет прооксидантного действия [32]. При использовании препаратов железа в адекватных дозах уже через несколько дней может отмечаться субъективное улучшение самочувствия. Первый объективный критерий — ретикулоцитарный криз (увеличение числа ретикулоцитов в 2–10 раз по сравнению с исходным) отмечается к концу первой недели терапии. Отсутствие ретикулоцитарного криза говорит либо о неадекватной дозе препарата, либо об ошибочном назначении препарата. Повышение уровня гемоглобина и числа эритроцитов отмечается на третьей неделе терапии. После нормализации уровня гемоглобина половинную дозу препарата железа рекомендуется применять еще 4–8 недель для насыщения им депо железа.
В 2013 г. вышли первые рекомендации по лечению анемии у пациентов с сердечно-сосудистой патологией, выпущенные американским колледжем врачей [20]. Они в целом определяют тактику ведения пациента с кардиальной патологией и анемией независимо от ее этиологии. Рассматривается три стратегии лечения: использование эритропоэтин-стимулирующих агентов, переливание эритромассы и восполнение дефицита железа. Подчеркивается, что переливание эритромассы не дает пользы и может нанести вред пациентам, поэтому оно возможно только у госпитализированных тяжелых пациентов с ИБС при тяжелой анемии. Не рекомендуется применение эритропоэтин-стимулирующих средств при легкой и среднетяжелой анемии у пациентов с ХСН и ИБС из-за потенциального риска развития тромбоэмболических осложнений и отсутствия влияния терапии на прогноз и частоту госпитализаций. Положительные данные на сегодня имеются для стратегии восполнения дефицита железа введением внутривенно карбоксимальтозата железа, эта тактика улучшает толерантность к физической нагрузке, качество жизни, снижает смертность и частоту госпитализаций [33].
Таким образом, анемия является частой сопутствующей патологией при сердечно-сосудистых заболеваниях. Сегодня в кардиологии она оценивается как независимый предиктор риска неблагоприятных клинических исходов, поэтому пациенты с сердечно-сосудистой патологией нуждаются в своевременной диагностике анемии для проведения адекватной терапии.
Литература
Е. С. Темникова, доктор медицинских наук, профессор
ГБОУ ВПО ОмГМА МЗ РФ, Омск
Что такое анемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Голышевой Екатерины Николаевны, терапевта со стажем в 8 лет.
Определение болезни. Причины заболевания
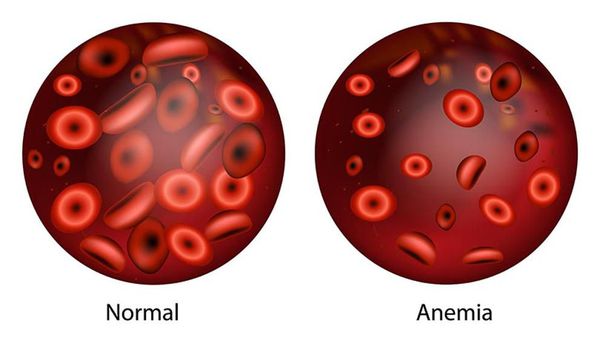
Анемия, или малокровие (Anemia) — это уменьшение количества эритроцитов и снижение уровня гемоглобина.
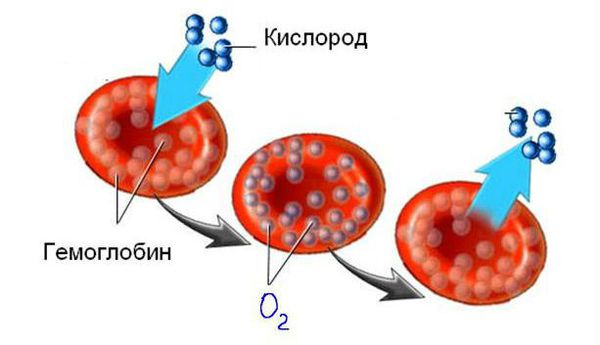
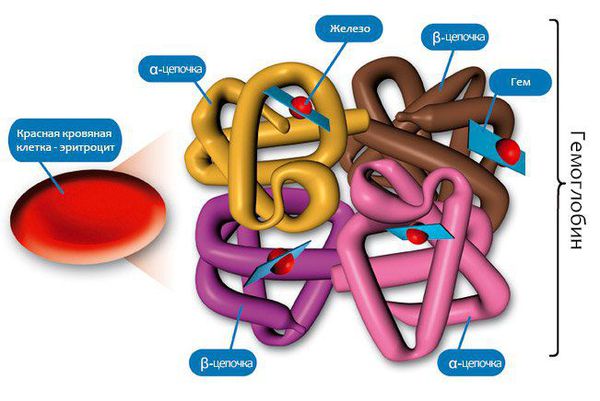
Эритроциты — это красные кровяные тельца, в них нет клеточного ядра, зато они содержат в себе особый железосодержащий белок — гемоглобин (Hb), который выполняет в организме важнейшую функцию газообмена (переносит кислород из лёгких в ткани и уносит от них углекислый газ). Следовательно, уменьшение количества эритроцитов в крови ведёт в снижению уровня гемоглобина. Есть ещё одно важное понятие — гематокрит (Hct) — это процентное соотношение эритроцитов к плазме крови.
У мужчин анемию определяют при следующий показателях:
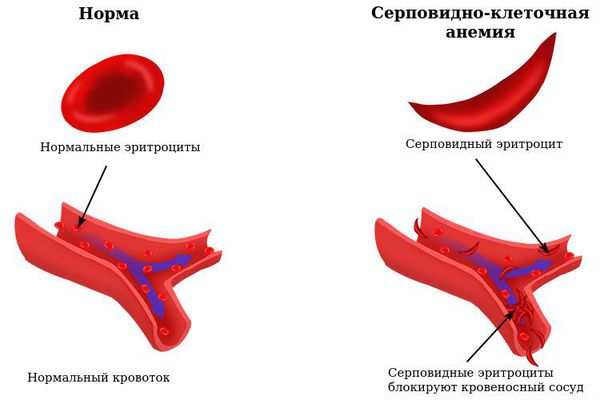
Выделяют наследственные типы анемий:
В ряде случаев причинами анемии являются недостаток определённых витаминов и микроэлементов (В12, фолиевая кислота, железо), либо проблема с их усвояемостью.
Вторичные причины развития анемии
К причинам развития железодефицитной анемии (ЖДА) относятся:
Например, высокая потребность в железе является главной причиной ЖДА у беременных и матерей, кормящих грудью. У женщин репродуктивного возраста в большинстве случаев железодефицитная анемия возникает вследствие обильных менструаций, а у детей — из-за недостаточного потребления с пищей. ЖДА может являться следствием несбалансированного питания при вегетерианской диете, так как железо из растительных продуктов усваивается хуже. В продуктах растительного происхождения содержится фитиновая кислота, которая образует с железом нерастворимые комплексы и ухудшает всасывание железа из этих продуктов. Лучше всего железо усваивается из продуктов животного происхождения, в мясе присутствует белок миоглобин, который улучшает всасывание железа в кишечнике.
Главное место среди причин анемий занимают острые и хронические кровопотери, нарушение кроветворения, ряд хронических и инфекционных заболеваний. Хронические кровопотери определяются малым объёмом теряемой крови, небольшой продолжительностью, очень часто протекают скрыто для самих больных и не всегда воспринимаются как первопричина анемии лечащими врачами разных специальностей. Такие кровопотери могут происходить, например, в случае обильных менструальных кровотечений у женщин, которые привыкают к этому и считают нормой. В этом случае неправильно и не до конца собранный гинекологический анамнез зачастую остаётся на «заднем» плане при диагностическом поиске причин анемии. При подозрении на скрытый дефицит железа, либо на любую другую анемию необходимо уточнять длительность менструального цикла, объём и продолжительность менструальных выделений. Прямо спрашивать о количестве расходуемых прокладок в сутки, необходимости замены ночью, что уже является признаком избыточной потери крови и требует консультации гинеколога для определения тактики ведения.
Анемия у детей
Анемия у детей проявляется такими же симптомами, как и анемия у взрослых: слабостью, быстрой утомляемостью, сонливостью, сухостю кожи, «заедами» в углах рта, выпадением волос, частыми головными болями, головокружениями, обмороками, шумом в ушах, снижением памяти и концентрации внимания, частыми простудными заболевания. У детей к анемии может присоединиться ночное недержание мочи (энурез). Также у детей с анемией страдает нервная система: ребёнок становится вялым, плаксивым, беспокойным, у него поверхностный сон, он плохо кушает и не набирает вес. Дети с тяжёлой анемией в возрасте до одного года могут отставать в развитии от сверстников.
Симптомы анемии
У анемий нет чётких специфичных симптомов, поэтому дифференциальная диагностика по одной лишь клинической картине невозможна. Признаки анемии появляются только тогда, когда уровень гемоглобина сильно снижается относительно индивидуального исходного показателя пациента. Симптомы в основном более выражены у больных с другими хроническими неинфекционными заболеваниями, к примеру эрозивными или язвенными болезнями желудочно-кишечного тракта, воспалительными заболеваниями тонкого кишечника (целиакия, болезнь Крона) или при стремительном развитии анемии.
При развитии анемии появляются бледность кожных покровов, общая слабость, тошнота, головокружение, загрудинные боли, тахикардия, одышка, в тяжёлых случаях бывают синкопы (потеря сознания). К ряду возможных симптомов анемии относятся: головная боль, головокружение, шум в ушах, отсутствие менструаций и расстройства пищеварения. При тяжёлой анемии развивается гипоксия тканей или гиповолемия, в этом случае возрастает вероятность наступления сердечно-сосудистой недостаточности или шока.
Симптомы, определяющие происхождение анемии
Симптомы анемии, развивающейся вследствие острой или хронической кровопотери: мелена (кал чёрного цвета, свидетельствующий о внутреннем кровотечении из верхних отделов желудочно-кишечного тракта), носовое кровотечение, обильные менструальные выделения, кровотечение из геморроидальных узлов.
Пожелтение кожных покровов и склер, моча тёмного цвета при отсутствии заболеваний печени указывают на разрушение эритроцитов с выделением гемоглобина (гемолиз).
Стремительная потеря веса без объективных причин может являться следствием онкологического процесса в организме.
Патогенез анемии
У каждой разновидности анемии имеется своя причина, но их патогенез очень схож, поэтому рассмотрим механизм развития часто встречающихся анемий.
Патогенез железодефицитной анемии складывается из двух механизмов:
Дефицит железа, как и другие анемии в организме, проходит три стадии:
Патогенез В12-дефицитной анемии
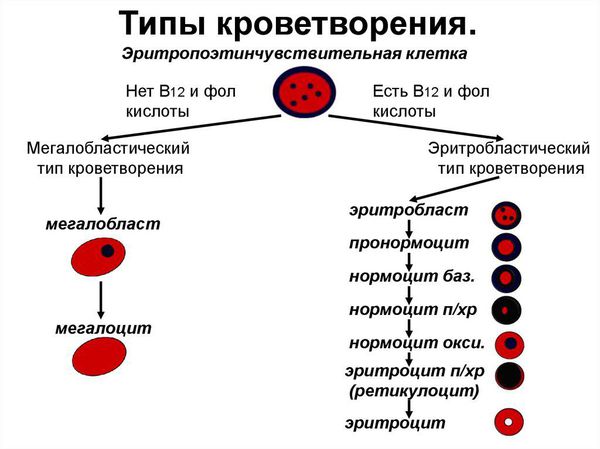
Сущность В12 дефицитной анемии заключается в нарушении процесса созревания красных кровяных клеток вследствие дефицита витамина В12 или В9 (фолиевой кислоты).
При дефиците витамина В12 прежде всего страдают: костный мозг, головной мозг и эпителий желудочно-кишечного тракта. В красном ростке кроветворения появляется мегалобластный тип кроветворения: возникает дефект синтеза ДНК, в результате чего формируются очень крупные клетки — мегалобласты, а из них мегалоциты; нарушается синхронность созревания ядра и цитоплазмы эритроцитов; красные кроветворные клетки гибнут рано. В это же время снижается гранулоцитопоэз (образование гранулоцитов, которые представляют собой самую многочисленную группу лейкоцитов) и тромбоцитопоэз (образование тромбоцитов).
Классификация и стадии развития анемии
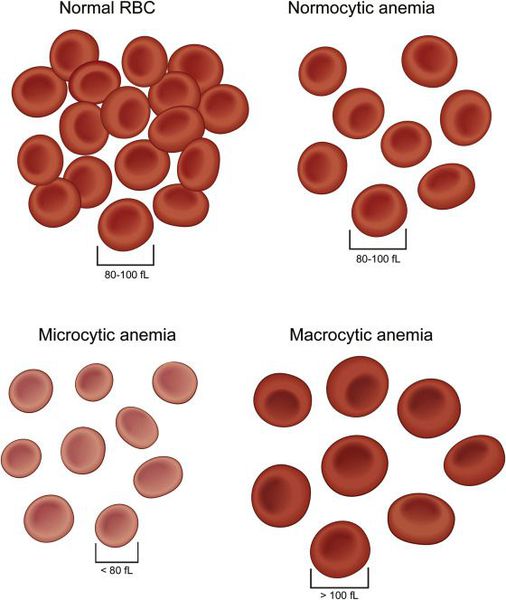
I. Классификация анемий по морфологии (размеру) эритроцитов
II. Классификация по цветовому показателю (ЦП)
III. Классификация анемий патогенетическая
Анемии вследствие кровопотери:
Анемии, вызванные нарушением образования гемоглобина и эритроцитов:
Анемии при усиленном кроверазрушении.
IV. Анемии по степеням тяжести EORTC (Европейское общество диагностики и лечения рака)
Степень тяжести анемии и количество гемоглобина:
Осложнения анемии
Больные анемией отмечают влияние ряда симптомов на их повседневную активность.
Хроническая усталость. Последствием анемии может быть постоянная общая слабость, сонливость, упадок сил, рассеянность, невозможность полноценно и регулярно заниматься спортом.
Иммунная система. По результатам исследований доказано, что анемия влияет на иммунитет, делая человека более восприимчивым к хроническим и инфекционным болезням.
Тяжёлая анемия увеличивает риск развития осложнений, направленных на сердечно-сосудистую систему или дыхательную. Могут появиться тахикардия (учащённое сердцебиение) и сердечная недостаточность (недостаточная эффективность кровоснабжения организма).
Беременность. Тяжёлые анемии у беременных женщин увеличивают риск ухудшения внутриутробного питания плода, осложнений во время родов и послеродовом периоде. Также такие пациентки более подвержены послеродовой депрессии. Ряд исследований показал, что дети, рождённые от женщин с анемией во время беременности, с высокой вероятностью:
Диагностика анемии
К какому врачу обратиться
При подозрении на анемию следует обратиться к врачу-терапевту. При необходимости может потребоваться консультация врача-гематолога и врача-гастроэнтеролога.
Лабораторная диагностика анемий
Общими критериями лабораторной диагностики всех анемий в общем анализе крови при подсчёте «ручным» методом являются один или сразу несколько показателей:
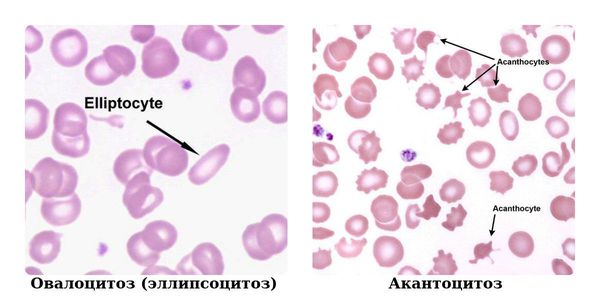
Также могут быть морфологические изменения эритроцитов (изменение формы) — анизоцитоз (изменение размеров эритроцитов или лейкоцитов) и пойкилоцитоз (деформация формы красных кровяных телец). В общем анализе крови необходимо обратить внимание на появление незрелых гранулоцитов, что может говорить о всевозможных воспалительных, аллергических процессах, аутоиммунных заболеваниях, инфекциях, вызванных вирусами или бактериями.
При выполнении общего анализа крови на автоматическом гематологическом анализаторе изменяются нормы указанных выше показателей и ряд эритроцитарных индексов. Также в общем анализе крови выявляется:
Изменения в биохимическом анализе крови определяются патогенезом анемии и могут включать:
В дополнение появилась возможность определения растворимых трансферриновых рецепторов (рТФР), концентрация которых при дефиците железа повышается (более 2,9 мкг/мл).
Дифференциальный диагноз ЖДА
Лечение анемии
Лечение в первую очередь должно быть направлено на выявление и устранение первопричины, поэтому терапия анемий длится долго, зачастую сопровождается несколькими врачами-специалистами.
Показание к лечению
Показание для медикаментозного лечения — это снижение уровня гемоглобина менее 120 г/л у женщин и ниже 130 г/л у мужчин.
В основном лечение подразумевает восстановление запасов гемоглобина, увеличение количества эритроцитов, нормализацию гематокрита. Основным эффективным методом лечения железодефицитных анемий является применение препаратов железа внутрь или парентерально (внутривенно или внутримышечно)
Чтобы восстановить уровень гемоглобина у больного железодефицитной анемией нужно, чтобы доза двухвалентного железа в сутки (эффективно всасывается только оно) составляла 100-300 мг, учитывая истощённые запасы железа (около 1,5 г).
Эффективнее назначать препараты с более высоким содержанием двухвалентного железа, их нужно принимать перорально (через рот) 1-2 раза в сутки. Для больных это самый удобный подход, следовательно, увеличивается их приверженность к терапии. В состав многих лекарственных форм железа входит аскорбиновая и янтарная кислоты, фруктоза, цистеин и др., они помогают наилучшему всасыванию железа в желудочно-кишечном тракте. Препараты железа лучше всего переносятся, если принимать их с пищей.
Лечение железодефицитной анемии парентеральными формами препаратов железа
Существуют чёткие показания для такой терапии:
Железодефицитная анемия — самый распространённый тип анемии. Однако лечение других типов малокровия отличается от лечения ЖДА. При других разновидностях анемии для нормализации показателей крови необходимо, например, восполнять запасы витамина В12, фолиевой кислоты, контролировать сопутствующие хронические заболевания и другие факторы, которые явились первопричиной анемии. Для этого необходимо своевременное обращение к врачу, который займётся диагностикой и определением тактики ведения.
Как улучшить лечение. Диета
Питаться нужно 4-6 раз в день. Для нормального переваривания еда должна быть комнатной температуры, слишком холодная или слишком горячая пища раздражают слизистую желудка, что препятствуют всасыванию полезных элементов. Количество выпитой воды в день — 30 мл на 1 кг веса, включая чай, сок, суп и т. д. Категорически запрещёно принимать алкоголь и курить. Алкоголь не только негативно сказывается на здоровье ЖКТ, но и вымывает полезные компоненты с мочой, что вредно даже для здоровых людей. Курение повышает кислотность желудка, что может спровоцировать развитие гастрита или язвы. В этом случае нарушится всасывание полезных микроэлементов.
Противопоказания при анемии
При анемии противопоказаны жёсткие диеты, рацион питания должен включать продукты с высоким содержанием железа, витамина В12 и фолиевой кислоты. Также развитие анемии возможно на фоне приёма некоторых лекарств (противоопухолевые, ряд антибактериальных, противопротозойных, противовирусных, противовоспалительных, противоревматических, противоэпилептических и антипсихотических препаратов). Поэтому приём данной группы лекарств при анемии должен проходить под контролем специалиста.
Можно ли лечить анемию народными средствами
На сегодняшний день эффективных народных средств лечения анемии не существует, потому что коррекция дефицита железа не может быть достигнута только изменением питания или использованием каких-либо трав, отваров и соков. Причина этого состоит в том, что усвоение железа из пищи ограничено (не более 3-5 % из растительной пищи), а в лекарственных препаратах оно содержится в большей концентрации.
Прогноз. Профилактика
Прогноз
Для прогноза играет важную роль причина анемии. Ранняя диагностика и быстрое определение тактики ведения постгеморрагической анемии напрямую связано с хорошим прогнозом.
Если анемия связана с дефицитом железа, витамина В12 или фолиевой кислоты, нужно дополнение диеты продуктами питания, богатыми данными микроэлементами и витаминами. Более плохой прогноз касается анемий, которые появились вследствие онкологических заболеваний, в том числе кроветворных органов, либо генетических нарушений, так как они плохо поддаются лечению.
Профилактика
Профилактика анемии включает в себя регулярные осмотры у терапевта со сдачей анализов, своевременное выявление и лечение хронических заболеваний, в том числе выявление и лечение источника хронической кровопотери (язвенные заболевания внутренних органов, геморрой и т. д.).
Для профилактики анемии, как и для лечения, важно наличие в рационе продуктов с высоким содержанием железа, витамина В12 и фолиевой кислоты.