Сероводород
Сероводород
Строение молекулы и физические свойства
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: х лорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
В избытке кислорода:
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
При кипячении сера окисляется до серной кислоты:
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
Серная кислота окисляет сероводород либо до молекулярной серы:
Либо до оксида серы (IV):
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов : меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Сероводород — новое лекарство для сосудов
Трудно поверить, что столь неприятная для нашего обоняния молекула может быть полезной.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Сероводород (H2S) наряду с другими газообразными молекулами, такими как монооксид углерода и монооксид азота, является важной внутриклеточной сигнальной молекулой, которая в последнее время стала объектом большого числа фундаментальных исследований. Как оказалось, H2S участвует в регуляции разнообразных физиологических процессов, связанных с регуляцией гомеостаза, иммунитета, передачи нервных импульсов в клетках центральной и периферической нервной системы. Однако среди огромного разнообразия биологических функций этой молекулы особое место выделяют ее роли в регуляции работы сердечнососудистой системы, в частности — формировании нормальных показателей артериального давления. Обнаружение такого свойства молекулы H2S положило начало новому направлению в фармакологии, связанному с поиском и созданием принципиально новой группы антигипертензивных препаратов, действие которых основывалось бы на высвобождении молекул H2S.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Своя работа».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Сероводород многим известен как газ, обладающий дурным запахом тухлых яиц. Первые упоминания о сероводороде датируются 16 веком, когда в 1713 году итальянский врач Бернардино Рамадзини описал влияние сероводорода на организм человека в своем труде «De Morbis Artificum», или «Заболевания рабочих». В главе «Болезни очистителей уборных и выгребных ям» он описывает болезненное воспаление глаз, которое было распространено среди таких рабочих. Воспаление это часто приводило к присоединению вторичной инфекции, а иногда и к полной слепоте. Рамадзини предположил, что во время работы из разрушенных экскрементов выделяются неизвестные летучие кислоты, которые и вызывают раздражение глаз. Как известно в настоящее время, сероводород образуется везде, где органическое вещество подвергается гниению [20].
В 1863 году Феликс Гоппе-Зейлер исследовал влияние чистого сероводорода на кровь человека и по изменениям в видимой области спектра поглощения, соответствующей гемоглобину, обнаружил зеленый пигмент. Он назвал новую форму гемоглобина сульфгемоглобином. Эта находка в дальнейшем привела к рождению гипотезы о том, что сероводород наряду с нитритом натрия и оксидом углерода (угарным газом) является кровяным ядом. Однако в условиях in vivo этот пигмент так и не был обнаружен.
Непосредственные исследования биологического действия сероводорода начались на рубеже XX века, но посвящены они были преимущественному изучению токсических свойств сероводорода [20]. Рассматривать сероводород в качестве сигнальной молекулы, которая не только является токсическим агентом, но и участвует в регуляции функциональной активности различных клеток нашего организма, стали только в конце XX века. Начало исследованиям в этой области положили японские ученые Абе и Кимура, которые в 1996 г. впервые описали возможность синтеза сероводорода в тканях головного мозга и указали на его способность регулировать функции клеток [4].
Хотя сероводород был обнаружен в тканях головного мозга еще в 1980-х годах, первоначально его сочли за артефакт, который образовался вследствие быстрого увеличения концентрации сульфидов в тканях после смерти. При этом появление сероводорода связывали с его высвобождением из дисульфидных соединений серы (так называемых «sulfane sulfur») во время препарирования тканей [16].
В настоящее время сероводород отнесен к группе так называемых газотрансмиттеров — газообразных внутриклеточных сигнальных молекул, выполняющих в клетке специфические регуляторные функции. H2S хорошо растворим в липофильных веществах. Его растворимость в липидах в пять раз превосходит растворимость в воде, что обусловливает хорошую проникающую способность H2S через мембранные структуры клетки и не требует участия специальных ион-транспортных систем. Константа проницаемости (РМ) сероводорода через бислойные липидные мембраны достаточно высока и составляет 0.5±0.4 см/с (для сравнения РМ для кислорода составляет примерно 0.0050±0.0006 см/с) [17]. Это позволяет считать сероводород высоко доступной молекулой, эффективно осуществляющей свои функции внутри клеток.
Другими молекулами, входящими в группу газотрансмиттеров, являются хорошо известный монооксид азота (NO), а также монооксид углерода (CO).
Синтез сероводорода
Внутриклеточный синтез сероводорода осуществляется в различных клетках нашего организма. В настоящее время известно три фермента, в результате работы которых синтезируется сероводород: цистотионин-β-синтаза (CBS), цистотионин-γ-лиаза (CSE) и 3-меркаптопируватсульфуртрансфераза (3-MST).
При этом CBS осуществляет синтез сероводорода преимущественно в нервных клетках. В гладкомышечных клетках кровеносных сосудов, сокращение-расслабление которых обеспечивает изменение тонуса последних, синтез сероводорода осуществляет фермент CSE [16], [22], а в эндотелиальных клетках, выстилающих изнутри просвет сосуда, — 3-MST [11], [21] (рис. 1).
Рисунок 1. Синтез сероводорода. В гладкомышечных клетках кровеносных сосудов, в кардиомиоцитах синтез сероводорода обусловлен активностью фермента цистотионин-γ-лиазы (CSE), тогда как в эндотелиальных клетках — комплекс 3-меркаптопируватсульфуртрансферазы (3-MST) и цистеин-аминотрансферазы (CAT). В клетках органов, не относящихся к кровеносному руслу, сероводород преимущественно синтезируется благодаря активности цистотионин-β-синтазы (CBS). Хотя фермент CBS локализован преимущественно в нейронах и клетках нейроглии, он также был обнаружен в клетках печени, почек, поджелудочной железы.
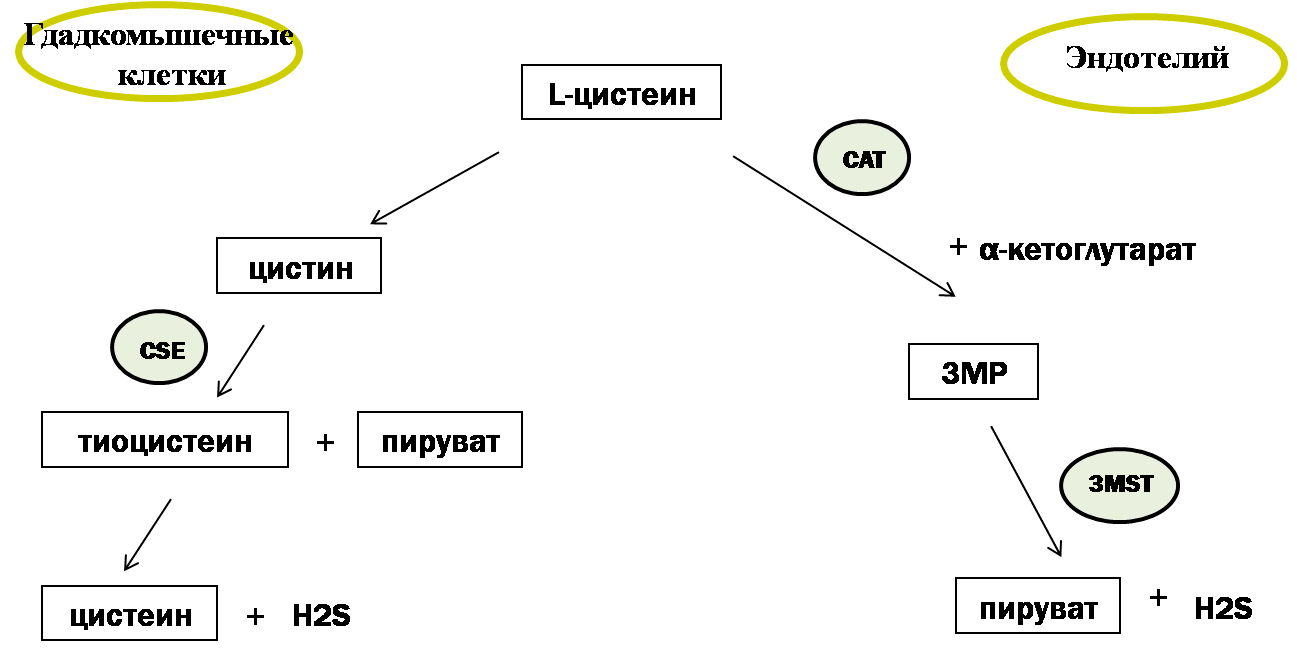
Все три фермента используют в качестве субстрата для синтеза сероводорода серосодержащую аминокислоту L-цистеин, катализируя реакцию его десульфгидратации: происходит отщепление от цистеина атома серы без последующего его окисления, что ведет к образованию H2S. Под действием CSE происходит преобразование цистина (дисульфид цистеин) до тиоцистеина, пирувата и аммиака, с последующим неферментативным преобразованием тиоцистеина до цистеина и H2S (рис. 2). В то же время, CBS использует несколько другой путь синтеза H2S, который заключается в конденсации гомоцистеина с цистеином, и последующим образованием цистатионина [16]. В качестве субстрата синтеза сероводорода могут использоваться и другие серосодержащие аминокислоты, такие как метионин и цистин.
Рисунок 2. Схема синтеза сероводорода в гладкомышечных и эндотелиальных клетках кровеносных сосудов. Условные обозначения: CAT — цистеин-аминотрансфераза; CST — цистотионин-γ-лиаза; 3МSТ — 3-меркаптопируват-сульфуртрансфераза; 3МР — 3-меркаптопируват.
Фермент 3-меркаптопируват-сульфуртрансфераза (3MST) функционирует в комплексе с другим ферментом — цистеин-аминотрансферазой (CAT). Выделяют митохондриальную и цитозольную формы CAT. Используя в качестве субстрата серосодержащую аминокислоту L-цистеин и α-кетоглутарат, CAT продуцирует 3-меркаптопируват (3МР), из которого при участии фермента 3MST синтезируется непосредственно H2S [18]. В отсутствии α-кетоглутарата синтез H2S прекращается.
Сероводород и сердечнососудистая система
Как показали многочисленные исследования, одной из систем, где сероводород играет ключевую роль как сигнальная молекула, является сердечнососудистая система, в частности — кровеносные сосуды. Осуществляя свое регуляторное действие в сосудах артериального русла, он принимает активное участие в регуляции артериального давления [23].
Исследования среди людей показали, что в группе лиц с нормальными показателями артериального давления уровень H2S в плазме крови составлял 34 мкМ, тогда как у больных артериальной гипертонией он был снижен до 20 мкМ. Назначение больным артериальной гипертонией ингаляций сероводорода способствовало снижению показателей артериального давления [29]. При проведении исследований на крысах было обнаружено, что внутривенное болюсное введение раствора сероводорода вызывало у них дозозависимое снижение артериального давления [16].
В условиях in vitro донор сероводорода гидросульфид натрия (NaHS), активно используемый в экспериментальной практике, также вызывал расслабление различных отделов артериального и венозного русла: грудной, мезентериальной, почечной артерий, аорты, воротной вены и т.д. Несмотря на существенную роль эндотелия в регуляции сосудистого тонуса, его удаление не оказывало существенного влияния на эффекты сероводорода в гладкомышечных клетках [16]. Это свидетельствует о прямом влиянии сероводорода на гладкомышечные клетки через присущие им регуляторные механизмы. Расслабляющее действие сероводорода на гладкомышечные клетки связано преимущественно с открыванием особых структур в их мембране — калиевых каналов, чувствительных к концентрации внутриклеточного источника энергии — аденозинтрифосфата (АТФ) [10], [28].
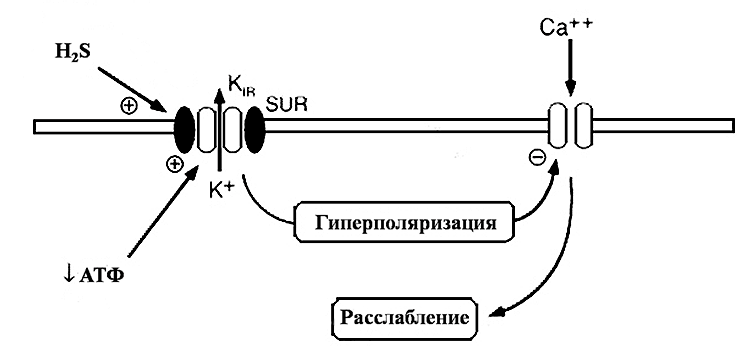
Связываясь с серосодержащими группами белков этих каналов, сероводород изменяет их пространственную конфигурацию и тем самым способствует открыванию каналов [2], [24]. Открывание калиевых каналов ведет к увеличению выхода ионов калия из клетки в межклеточную среду. В то же время, активации АТФ-чувствительных калиевых каналов сопровождается инактивацией потенциал-чувствительных кальциевых каналов L-типа, обеспечивающих поступление ионов кальция (Са 2+ ) в клетку. Высокая внутриклеточная концентрация Са 2+ является необходимым условием развития сократительного ответа со стороны мышечной клетки. Закрывание кальциевых каналов способствует снижению концентрации свободного внутриклеточного Са 2+ [29]. Эти процессы в совокупности запускают механизмы расслабления в гладкомышечных клетках, что в конечном итоге приводит к снижению тонуса кровеносных сосудов и артериального давления в целом (рис. 3).
Рисунок 3. Влияние сероводорода на мембранные процессы. Сероводород, взаимодействуя с АТФ-чувствительными калиевыми каналами, вызывает их активацию и увеличение выхода ионов калия из клетки. Вследствие этого снижается мембранный потенциал на мембране (гиперполяризация) и инактивируются кальциевые каналы. В результате прекращения поступления в клетку ионов кальция происходит расслабление гладкомышечной клетки.
В регуляции релаксирующего действия сероводорода участвуют также и другие внутриклеточные молекулярные механизмы, однако их роль не столь выражена и однозначна [23].
Физиологическая роль сократительного эффекта сероводорода до конца не ясна: является ли он побочным продуктом каких-то внутриклеточных молекулярных реакций, или же несет на себе функциональную нагрузку? В первом случае увеличение тонуса сосудов может быть результатом взаимодействия сероводорода с активными формами кислорода, что приводит как к снижению концентрации самого сероводорода, так и образованию продуктов, способных вызывать сократительный ответ со стороны гладкомышечных клеток. Второй же случай предполагает специфическую активацию сероводородом ионных механизмов, направленных на развитие кратковременного локального спазма, например, в случае нарушения целостности сосудистой стенки [12].
В сердце сероводород снижает сократимость миокарда как в условиях in vitro, так и в условиях in vivo [9], [27]. Этот эффект также частично связан с активацией АТФ-чувствительных калиевых каналов мембран кардиомиоцитов [16]. В экспериментах по моделированию инфаркта миокарда у крыс было обнаружено, что концентрация сероводорода в миокарде и плазме крови таких крыс была на 60% ниже по сравнению с контрольной группой. При этом введение NaHS снижало уровень смертности среди крыс с инфарктом миокарда за счет уменьшения его сократимости и торможения некроза кардиомиоцитов [8].
Дальнейшие перспективы
Учитывая роль сероводорода в регуляции тонуса кровеносных сосудов, ученые всего мира активно взялись за разработку лекарственных средств, действие которых основывалось бы на повышении или понижении в крови концентрации этого газотрансмиттера. В настоящее время возможные молекулы-кандидаты на роль лекарственных соединений можно разделить на две группы: молекулы, которые, растворяясь, непосредственно высвобождают сероводород (NaHS, Na2S, GYY4137) и молекулы-предикторы эндогенного синтеза сероводорода (N-ацетилцистеин, L-цистеин) [7].
N-ацетилцистеин и L-цистеин — предшественники синтеза эндогенного H2S. Увеличение внутриклеточной концентрации этих молекул вызывает дополнительную активацию ферментов CSE и CBS и, следовательно, усиление синтеза H2S. Существенным преимуществом этих молекул является практически полное отсутствие побочных эффектов. Однако трудности, связанные с регулированием конечной концентрации образующегося H2S, вносят свои ограничения на использование N-ацетилцистеина и L-цистеина в клинической практике [26].
Возможные молекулы-претенденты на роль нового лекарственного вещества должны обладать рядом свойств. Во-первых, они должны быть хорошо растворимы в воде. Во-вторых, не должны оказывать токсического действия. В-третьих, не должны быстро метаболизироваться в организме. И в-четвертых, обладать пролонгированным действием, что возможно при достаточно медленном высвобождении сероводорода молекулой-донором в условиях in vivo.
В настоящее время в экспериментальной практике наиболее часто в качестве донора сероводорода используются гидросульфид натрия (NaHS) и сульфид натрия Na2S. Однако при растворении этих молекул происходит слишком быстрое высвобождение сероводорода, что в условиях in vivo вызывает резкое падение артериального давления, вплоть до сосудистого коллапса [16]. Процесс высвобождения сероводорода в этом случае трудно контролируется, что делает NaHS и Na2S непригодными для использования в терапевтических целях.
Недавно Ли с соавторами [14] получили из реактива Лавессона новую молекулу-донор сероводорода, которую они обозначили как GYY4137 (рис. 4). В отличие от гидросульфида натрия, GYY4137 высвобождает сероводород постепенно, что делает эту молекулу более перспективной для дальнейших фармакологических исследований. В моделях на крысах в условиях in vivo и in vitro исследователи установили, что GYY4137 обладает сосудо-расслабляющими свойствами и оказывает антигипертензивное действие.
Рисунок 4. Схема синтеза GYY4137 из реактива Лавессона
Другим направлением в разработках «сероводородных» препаратов является встраивание сероводород-высвобождающих группировок в уже имеющиеся и широко используемые лекарственные молекулы. Альтернативные доноры сероводорода могут быть получены путем добавления сульфидных групп к нестероидным противовоспалительным препаратам. Например, S-диклофенак содержит тионовые группы, прикрепленные эфирными связями к молекуле-носителю, которые в растворе играют роль источника сероводорода [13]. Встраивание тиоловых группировок в молекулу силденафила приводит к развитию эффекта, связанного с существенной релаксацией гладкомышечных клеток кавернозных тел [7].
В последние годы большое внимание привлекли полисульфидные соединения чеснока. Были обнаружены их вазоактивные свойства: одно из соединений — диаллил дисульфид (DADS) — вызывало расслабление кольцевых сегментов аорты крысы. Полисульфидные соединения чеснока не только являются предшественниками H2S, но и способны самостоятельно вызывать изменения конформации молекул белков в клеточных мембранах.
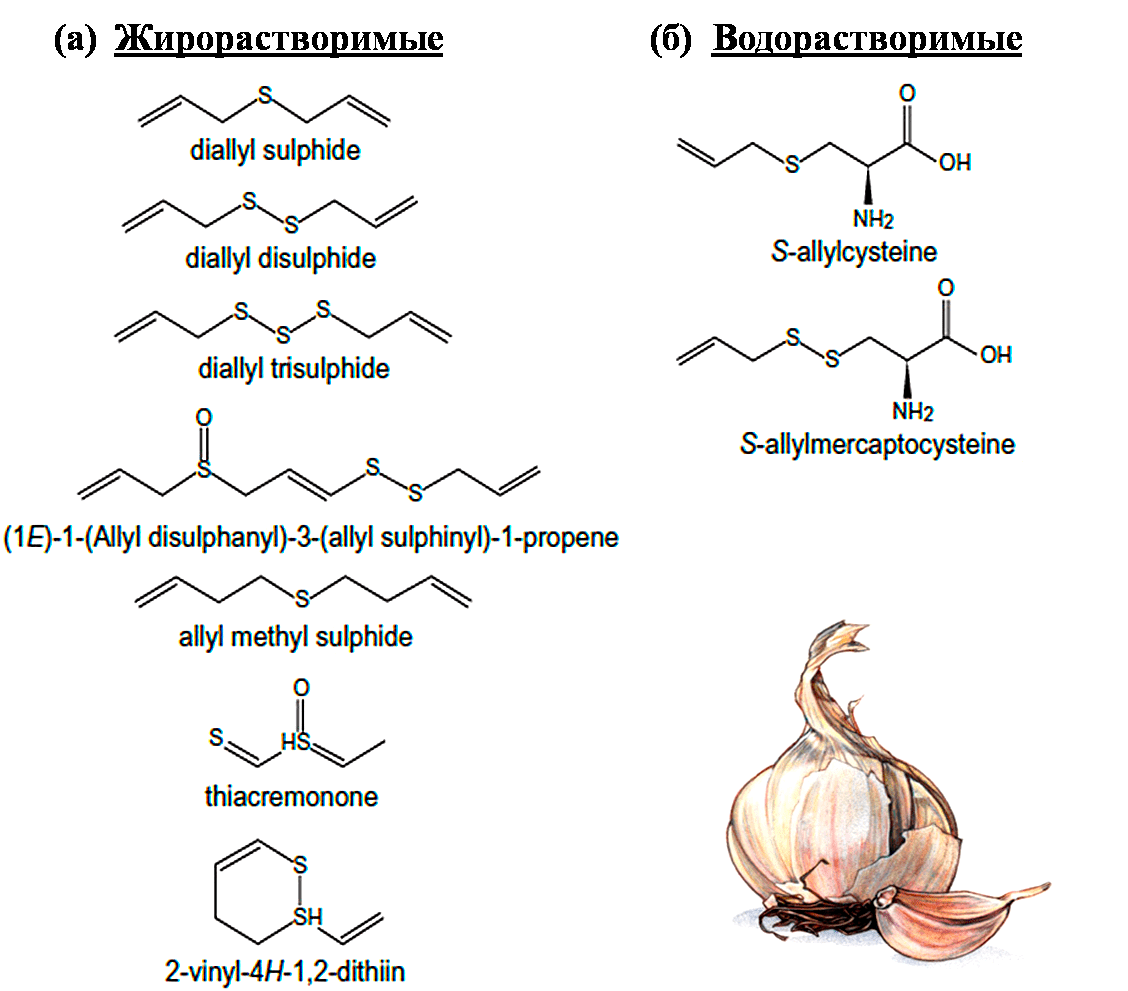
Перспективной молекулой-донором сероводорода является получаемый из чеснока S-аллилцистеин, который обладает выраженным кардиопротекторным действием (рис. 5). Однако пока не до конца ясно, является ли он предшественником сероводорода или же модулирует функцию ферментов, связанных с синтезом последнего [26].
Рисунок 5. Серосодержащие соединения чеснока. Из чеснока получают два класса органических соединений серы: жирорастворимые (а) и водорастворимые (б) аллильные соединения серы, образующиеся из гликозида аллиина. Жирорастворимые аллильные соединения серы, такие как диаллил сульфид (DAS), диаллил дисульфид (DADS) и диаллил трисульфид (DATS) освобождаются из аллиина. Эта реакция катализируется ферментом аллииназой, который высвобождается при измельчении чеснока. Водорастворимые соединения серы (S-аллилцистеин (SAC) и S-аллилмеркаптоцистеин) получают при длительной инкубации дробленого чеснока в водных растворах.
С целью снижения патологически высокой концентрации сероводорода можно использовать ингибиторы ферментов его синтеза. К ним относится DL-пропаргилглицин, который, обладая высокими липофильными свойствами, легко проникает через мембрану клетки, не вызывая видимых ее повреждений. Однако DL-пропаргилглицин ингибирует не только CSE-фермент синтеза сероводорода в сердечнососудистой системе, но и CBS, что может стать причиной появления множества нежелательных побочных эффектов, связанных с нарушением регуляции функции других органов [26].
Таким образом, существующие в настоящее время наработки в области создания доноров сероводорода, пригодных для использования в терапевтических целях, находятся на ранней стадии своего развития и явно недостаточны. Разработка, синтез и описание свойств новых доноров сероводорода и селективных ингибиторов ферментов его эндогенного синтеза имеет чрезвычайно важное значение для создания новой группы лекарственных препаратов и, возможно, позволит продвинуться вперед в борьбе с сердечно-сосудистыми заболеваниями [5].
Сероводород, свойства, получение и применение
Сероводород – бинарное химическое соединение водорода и серы, имеющее формулу H2S.
Сероводород, формула, молекула, строение, состав, вещество:
Сероводород (сернистый водород, сульфид водорода, дигидросульфид) – бесцветный газ со сладковатым вкусом с характерным неприятным тяжёлым запахом тухлых яиц (тухлого мяса).
Сероводород – бинарное химическое соединение водорода и серы, имеющее формулу H2S.
Химическая формула сероводорода H2S.
Строение молекулы сероводорода, структурная формула сероводорода:
Сероводород – наиболее активное из серосодержащих соединений.
Сероводород плохо растворяется в воде. Раствор сероводорода в воде – очень слабая сероводородная кислота. Хорошо растворим в бензоле и этаноле.
Термически устойчив при температурах менее 400 °C. При температурах более 400 °C разлагается на составляющие – простые вещества: водород и серу.
В отличие от воды, в сероводороде не образуются водородные связи, поэтому сероводород в обычных условиях не сжижается.
Сероводород является сверхпроводником при температуре 203 К (-70 °C) и давлении 150 ГПа.
Сероводород коррозионно активен, поэтому предъявляются дополнительные требования при разработке нефтяных, газовых и газоконденсатных месторождений, содержащий сероводород.
Чрезвычайно огнеопасен. Смеси сероводорода и воздуха взрывоопасны. Возможно возгорание на расстоянии. Горит синим пламенем.
Соли сероводородной кислоты (раствор сероводорода в воде) называют сульфидами. В воде хорошо растворимы только сульфиды щелочных металлов, аммония. Сульфиды остальных металлов практически не растворимы в воде, они выпадают в осадок в ходе химических реакций. Многие сульфиды ярко окрашены. Многие природные сульфиды в виде минералов являются ценными рудами (пирит, халькопирит, киноварь, молибденит).
Сероводород в природе встречается редко, в незначительных количествах в составе природного газа, попутного нефтяного газа, сланцевого газа, а также в вулканических газах, в растворённом виде – в нефти, сланцевой нефти и в природных водах. Например, в Чёрном море слои воды, расположенные глубже 150-200 м, содержат растворённый сероводород (концентрация 14 мл/л).
Образуется при гниении белков, которые содержат в составе серосодержащие аминокислоты метионин и (или) цистеин. Небольшое количество сероводорода содержится в кишечных газах человека и животных.
Физические свойства сероводорода:
| Наименование параметра: | Значение: |
| Химическая формула | H2S |
| Синонимы и названия иностранном языке | hydrogen sulfide (англ.) |
водород сернистый (рус.)
водорода сульфид (рус.)
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Получение сероводорода:
Сероводород в лаборатории получают в результате следующих химических реакций:
Данная реакция отличается чистотой полученного сероводорода
Химические свойства сероводорода. Химические реакции (уравнения) сероводорода:
Основные химические реакции сероводорода следующие:
1. реакция взаимодействия сероводорода и брома:
В результате реакции образуются бромоводород и сера. В ходе реакции используется насыщенный раствор сероводорода.
2. реакция взаимодействия сероводорода и йода:
В результате реакции образуются йодоводород и сера. В ходе реакции используется насыщенный раствор сероводорода.
3. реакция взаимодействия сероводорода и кислорода:
В результате реакции образуются сера и вода. Реакция протекает медленно на свету, в растворе или в газовой фазе. Сероводород в ходе реакции используется в виде насыщенного раствора. На данной реакции основан промышленный способ получения серы.
4. реакция горения сероводорода:
В результате реакции образуются оксид серы и вода. Реакция горения сероводорода на воздухе.
5. реакция взаимодействия сероводорода и озона:
В результате реакции образуются оксид серы и вода. Сероводород в ходе реакции используется в виде газа.
6. реакция взаимодействия сероводорода и кремния:
В результате реакции образуются сульфид кремния и водород.
7. реакция взаимодействия сероводорода и цинка:
В результате реакции образуются сульфид цинка и водород.
8. реакция взаимодействия сероводорода и алюминия:
В результате реакции образуются сульфид алюминия и водород.
9. реакция взаимодействия сероводорода и галлия:
В результате реакции образуются сульфид галлия и водород.
10. реакция взаимодействия сероводорода и молибдена:
В результате реакции образуются сульфид молибдена и водород.
11. реакция взаимодействия сероводорода и бария:
В результате реакции образуются сульфид бария и водород.
12. реакция взаимодействия сероводорода и магния:
В результате реакции образуются сульфид магния и водород.
13. реакция взаимодействия сероводорода и германия:
В результате реакции образуются сульфид германия и водород.
14. реакция взаимодействия сероводорода и кобальта:
В результате реакции образуются сульфид кобальта и водород.
15. реакция взаимодействия сероводорода и серебра:
В результате реакции образуются сульфид серебра и водород.
16. реакция взаимодействия сероводорода и оксида лития:
В результате реакции образуются сульфид лития и вода.
17. реакция взаимодействия сероводорода и оксида цинка:
ZnO + H2S ZnS + H2O (t = 450-550 °C).
В результате реакции образуются сульфид цинка и вода.
18. реакция взаимодействия сероводорода и оксида железа:
В результате реакции образуются сульфид железа и вода.
19. реакция взаимодействия сероводорода и оксида молибдена:
В результате реакции образуются сульфид молибдена и вода.
20. реакция взаимодействия сероводорода и гидроксида натрия:
В результате реакции образуются сульфид натрия и вода. В ходе реакции используется концентрированный раствор гидроксида натрия.
21. реакция взаимодействия сероводорода и гидроксида бария:
В результате реакции образуются сульфид бария и вода. В ходе реакции используется разбавленный раствор сероводорода.
22. реакция взаимодействия сероводорода и гидроксида меди:
В результате реакции образуются сульфид меди и вода. В ходе реакции используется насыщенный раствор сероводорода и гидроксид меди в виде суспензии.
23. реакция взаимодействия сероводорода и азотной кислоты:
В результате реакции образуются сера, оксид азота и вода. В ходе реакции используется насыщенный раствор сероводорода и концентрированный холодный раствор азотной кислоты.
Аналогичные реакции протекают и с другими минеральными кислотами.
24. реакция взаимодействия сероводорода и карбоната кальция:
В результате реакции образуются сульфид кальция, оксид углерода и вода.
25. реакция взаимодействия сероводорода и карбоната бария:
В результате реакции образуются сульфид бария, оксид углерода и вода.
26. реакция взаимодействия сероводорода и карбоната натрия:
В результате реакции образуются гидросульфид натрия и гидрокарбонат натрия. В ходе реакции используется насыщенный раствор сероводорода.
27. реакция взаимодействия сероводорода и нитрата серебра:
В результате реакции образуются сульфид серебра и азотная кислота. В ходе реакции используется насыщенный раствор сероводорода.
28. реакция взаимодействия сероводорода и нитрата висмута:
В результате реакции образуются сульфид висмута и азотная кислота. В ходе реакции используется насыщенный раствор сероводорода.
29. реакция взаимодействия сероводорода и нитрата свинца:
В результате реакции образуются сульфид свинца и азотная кислота. Данная реакция является качественной реакцией на сероводород. В результате реакции образуются соль свинца – сульфид свинца черного цвета, который выпадает в осадок.
30. реакция термического разложения сероводорода:
В результате реакции образуются водород и сера. В ходе реакции используется насыщенный раствор сероводорода.
Применение сероводорода:
Из-за своей токсичности сероводород находит ограниченное применение:
В последние годы рассматривается возможность использования сероводорода, накопленного в глубинах Чёрного моря, в качестве энергетического (сероводородная энергетика) и химического сырья.