Сеть Киари (Хиари)
Что представляет собой сеть Киари?
Сеть Киари является остатком эмбрионального правого клапана венозного синуса и образуется в случае его неполной резорбции.
Анатомически сеть Киари представлена сетевидной структурой неправильной формы, которая состоит из множества фиброзно-нитевидных и мембранозных компонентов.
Распространенность
Распространенность сети Киари составляет около 2%. При трансторакальной эхокардиографии сеть Киари выявляется у 0,9% населения, а при чреспищеводной эхокардиографии частота встречаемости выше из-за лучшего качества визуализации, и составляет до 1,6%.
Крепление сети Киари может варьировать в различных отделах правого предсердия:
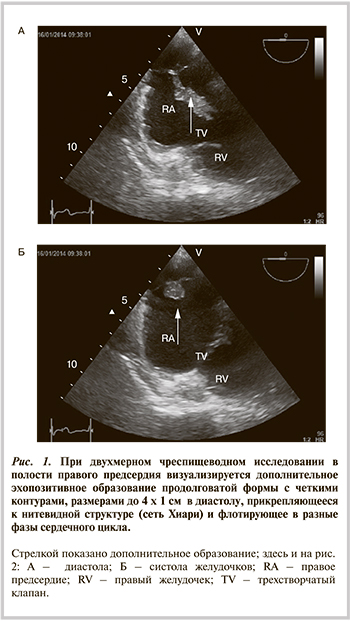
Рис.1. В правом предсердии визуализируется нитевидное образование — сеть Киари.
Диагностика сети Chiari
Часто сеть Киари диагностируют вместе с:
Для визуализации сети Киари при трансторакальной эхокардиографии используют позиции, в которых обычно исследуют правое предсердие. Для оценки места прикрепления сети Киари необходимо полипозиционнное исследование. Такое исследование из разных точек оправдано т.к. возможные места крепления сети Chiari не прослеживаются в одной плоскости сканирования.
Выявление тонких, линейных, подвижных структур в правом предсердии, которые характеризуются кнутовидными движениями и прикрепляются к евстахиеву клапану, позволяют заподозрить наличие сети Киари.
Рис. 2. Макропрепарат. Сеть Киари.
Клиническое значение сети Киари
Клиническое значение сети Киари в первую очередь определяется высокой сопряженностью с открытым овальным окном. В проведенных исследованиях у 82% с открытым овальным окном были дополнительно обнаружены евстахиев клапан или сеть Chiari.
Сеть Хиари и Евстахиев клапан могут препятствовать закрытию открытого овального окна. Они предрасполагают к формированию аневризмы межпредсердной перегородки и парадоксальной эмболии, направляя поток крови из нижней полой вены к межпредсердной перегородке (МПП). Также прослеживается связь между наличием сети Киари и мигренью с аурой у пациентов с открытым овальным окном (ООО).
Описаны случаи инфекционного эндокардита с поражением сети Хиари. Также сеть Киари может выглядеть подобно опухолевому образованию, и тем самым приводить к ложному диагнозу.
Рис. 3. В правом предсердии визуализируется нитевидное образование — сеть Хиари
Если рассматривать сеть Chiari с позиции тромбоэмболических осложнений, то мнение может быть двояким. С одной стороны, она может выступать в качестве ловушки для тромбоэмболов, предохраняя пациента от фатальной тромбоэмболии легочной артерии (ТЭЛА). С другой стороны – сеть Киари может способствовать образованию тромбов in situ.
Предположение о том что сеть Киари может препятствовать кровотоку, не нашло убедительных подтверждений.
Описаны случаи интраоперационных осложнений, обусловленных затруднением проведения катетеров в правые камеры сердца или в коронарный синус из-за наличия этого предсердного образования.
Вас также могут заинтересовать следующие статьи:
Что происходит при наличии сосудистой сети Киари
В процессе диагностики в правом предсердии обнаружили сеть Киари или Хиари, хотя я не ощущал никак особых симптомов. Что она представляет собой, опасна ли для здоровья, будут ли проблемы в будущем и что нужно делать?
Здравствуйте. Сеть Киари в правом предсердии представляет собой непатологическую подвижную тонкую сетчатую структуру в правом предсердии, которую видно на мониторе УЗИ из любой позиции там, где в предсердие впадает нижняя полая вена. То есть сетка состоит из остатков эмбрионального клапана коронарного синуса, что прикрепляются к евстахиеву клапану нижней полой вены с одной стороны, а с другой – к частям правого предсердия (ПП). Она обнаруживается действительно случайно при диагностике у 1-2% населения.
Если быть точнее, то эта врожденная аномальная структура сердца в виде сетевидной пластинки с дырками – перегородка предсердия – начинается у заслонки венечного синуса (Тебезиева клапана) и заслонки нижней полой вены (Евстахиева клапана). Она в некоторой степени может перегораживать предсердие.
Пластинка может иметь разные положения, но в основном прикрепляется чуть кпереди от Ловерова (межвенозного) бугорка. Сеть Хиари появляется в связи с недостаточной редукцией правого (реже – левого) синусового клапана или из-за ложной перегородки. Удлиненную заслонку Евстахиева клапана и Сеть Хиари считают вариантом нормы.
Диагностика
Чтобы визуализировать сеть Chiari применяют ЭхоКГ-диагностику. При этом используются позиции, в которых одновременно исследуют ПП: апикальную 4КП, модифицированную парастернальную биккавальную позицию и короткую ось на уровне Аок со стороны левого парастернального доступа, но это могут выполнять только профессиональные диагностики.
Также используют позиции субкостальные: 4КП, короткую ось на уровне Аок и длинную ось полой вены снизу. Чтобы оценить место прикрепления сети Хиари, необходимо провести полипозиционное исследование и включить промежуточные позиции прикрепления на евстахиевом и клапане коронарного синуса.
В других возможных местах в одной плоскости сеть может не визуализироваться. Тогда применяют 3D-ЭхоКГ-исследование. Лучше всего оценку устья коронарного синуса удается датчиком из пищевода, а точнее – из его средних отделов.
Клиника
Сеть Хиари высоко сопряжена с ООО (открытым овальным окном). У 82% пациентов, которым назначают эндоваскулярное закрытие ООО, имеется сеть Хиари или евстахиев клапан. Если имеется ООО, то чаще выявляют право-левое шунтирование крови, чем при отсутствии сети. Сеть, как и клапан, препятствуют закрытию открытого овального окна, тогда может развиться аневризма межпредсердной перегородки (МПП) и парадоксальная эмболия.
В этом случае поток крови будет направляться из нижней полой вены к МПП. При аневризме МПП происходит выпячивание стенки между предсердиями S-образно (изгибаться в обе стороны), вправо или влево. Симптомы при этом не проявляются, а патология через некоторое время исчезает.
В некоторых случаях при наличии сети Chiari у пациентов возникают приступы мигрени. Если у больных развивается инфекционный эндокардит, то болезнь может поразить ткани сети. Они могут иметь вид опухолевого образования, тогда не исключен ложный диагноз.
Если рассматривать сети Хиари, как тромбоэмболические осложнения, то их роль двояка:
Были случаи отрыва фрагментов ткани сети и миграции их в легкие. Аритмогенность сетей Хиари может происходить из-за тесной взаимосвязи САС (симпатико-адреналовой системы) с венозным синусом на некоторых участках, а также в связи с наличием миокардиальных волокон в ретикулярной структуре тканей сети. Исследованиями не подтвержден факт препятствия сетей Chiari кровотоку. Но были случаи, что из-за этих предсердных образований было сложно провести катетеры в коронарный синус или правые отделы сердца.
Клиническое значение
Изолированно сеть встречается реже, чем в сочетании с коммуникациями между предсердиями. Если ее выявляют, то это дает основание искать ООО и АМПП (аневризмы межпредсердной перегородки) полипозиционным исследованием, используя стандартные и промежуточные позиции.
Клинически из-за патологии возможны тромбоэмболические осложнения (тромб in situ), инфекционный эндокардит, трудности с дифференциальной диагностикой из-за различных внутрипредсердных образований (опухолей, тромбов, кист), возможны сложности при проведении эндоваскулярных доступов к сердцу.
На эхокардиографии показана сеть Хиари(CN):
На видео в этой статье можно увидеть работу сердца с наличием сети Хиари.
Вывод
Сама сеть клинически не имеет существенного значения, но ее часто ассоциируют с патологиями: открытым овальным окном (ООО), внутрипредсердным тромбозом или предсердными аритмиями. Осложняется сетка Хиари тромбозом с последующей тромбоэмболией, но лечения не назначают, поскольку она преграждает продвижение тромба, является рудиментом заслонки коронарного синуса.
Практического значения сетевидная пластинка с дырками не имеет. Но проводят для ее обнаружения необычный диагноз, что не исключает врачебной ошибки. Поэтому важно проводить тщательную эхокардиографию, что при сердечно-сосудистых вмешательствах облегчит преодолеть трудности при проведении катетеризации в коронарный синус или правые отделы сердца.
Тромбоэмболия сети Хиари и легочной артерии
ФГБУ «Центральная клиническая больница с поликлиникой» Управления делами Президента РФ, 121356 Москва, ул. Маршала Тимошенко, 15
В статье представлено клиническое наблюдение пациента c тромбоэмболией сети Хиари и легочной артерии вследствие тромбоза вен нижних конечностей. Сеть Хиари встречается в небольшом проценте случаев в правом предсердии и обычно не имеет существенного клинического значения. Однако иногда она может быть ассоциирована с такими патологическими изменениями, как открытое овальное окно, внутрипредсердный тромбоз или предсердные аритмии. В данном случае сеть Хиари выступила в качестве преграды, задержавшей продвижение тромба.
Сеть Хиари выявляется в популяции в 2% случаев и представляет собой фиброзно-нитевидную структуру в виде сетки, которая прикрепляется к клапану нижней полой вены (евстахиев клапан) с одной стороны и к различным частям правого предсердия (ПП) — с другой [1]. Наряду с евстахиевым клапаном сеть Хиари может прикрепляться к клапану основного венозного коллектора, впадающего в ПП коронарного синуса (тебезиев клапан), к терминальному гребню, расположенному в зоне устья верхней полой вены, межпредсердной перегородке и стенке предсердия [1].
Обычно сеть Хиари не имеет существенного клинического значения. Однако в литературе периодически появляются описания случаев, в которых сеть Хиари играет определенную функциональную роль. С подобным случаем довелось столкнуться и нам.
Описание клинического наблюдения
Больной М., 68 лет, поступил в отделение нарушений ритма сердца ФГБУ «ЦКБ с поликлиникой» УДП РФ в январе 2014 г. с жалобами на сердцебиение и перебои в работе сердца, общую слабость, головокружение.
Из анамнеза известно, что больной страдает рядом сопутствующих заболеваний, таких как хронический бронхит, эмфизема легких, диффузный пневмосклероз, многоузловой эутиреоидный зоб, аденома предстательной железы, хронический простатит.
При поступлении в стационар состояние средней тяжести, периферических отеков нет, температура тела 36,6 °С. Периферические лимфатические узлы не увеличены. При аускультации легких дыхание жесткое, проводится во все отделы, хрипов нет. При аускультации сердца тоны сердца приглушены, аритмичные. Частота сердечных сокращений около 140 уд/мин, дефицита пульса нет. АД 130/85 мм рт.ст. Живот мягкий, при пальпации безболезненный. Печень выступает на 1 см из-под края реберной дуги. Селезенка не пальпируется. Стул в норме. Дизурических явлений нет.
Пациент в сознании, контактен, ориентирован. Острой очаговой неврологической и менингеальной симптоматики нет.
При поступлении в клиническом анализе крови эритроцитоз (эр. 6,03×1012/л при норме до 5,6×1012/л; Hb 168 г/л при норме до 160 г/л), нейтрофилез за счет сегментоядерных форм (н. 6,16×109/л при норме до 5,9×109/л, с. 78% при норме до 72%), лимфоцитопения (лимф. 1,155×109/л при норме от 1,2×109/л; 15% при норме от 19%), тромбоцитопения (тр. 121×109/л при норме от 180×109/л), остальные показатели в пределах нормы. При динамическом наблюдении за 3 нед лечения показатели красной и белой крови нормализовались.
В анализе мочи регистрировалась протеинурия (бело.
Структурные аномалии сердца с позиций анатомоморфологического и ультразвукового исследования
Дата публикации: 04.09.2018 2018-09-04
Статья просмотрена: 1986 раз
Библиографическое описание:
Жерко, Л. В. Структурные аномалии сердца с позиций анатомоморфологического и ультразвукового исследования / Л. В. Жерко, Л. А. Давыдова. — Текст : непосредственный // Молодой ученый. — 2018. — № 35 (221). — С. 22-26. — URL: https://moluch.ru/archive/221/52510/ (дата обращения: 07.12.2021).
Термин структурные или малые аномалии сердца (САС) объединяет все гемодинамически малозначимые аномалии соединительнотканного каркаса и клапанного аппарата сердца [1]. САС являются проявлением наследственно-обусловленных, многофакторных врожденных нарушений соединительной ткани. Наследственные нарушения соединительной ткани представляют собой гетерогенную группу заболеваний, обусловленных генетическими дефектами синтеза и/или распада белков внеклеточного матрикса либо нарушениями морфогенеза соединительной ткани. Выделяют синдромальные моногенные формы с согласованными критериями и несиндромальные формы мультифакториальной природы [2]. К моногенным наследственным синдромам относят синдромы Марфана, Элерса-Данло, гипермобильности суставов, несовершенного остеогенеза, пролапса митрального клапана, семейный синдром марфаноидной внешности (синдром Луиса-Дитца) и др. У пациентов с моногенными наследственными синдромами с согласованными критериями определяются множественные САС. К мультифакториальным несиндромным формам относят марфаноподобный, элерсоподобный и неклассифицируемый фенотипы, не имеющие на сегодняшний день точного молекулярно-генетического подтверждения. Поскольку соединительная ткань есть во всех органах и тканях, многообразие клинической симптоматики при наследственных и многофакторных нарушениях соединительной ткани является следствием изменения структуры, метаболизма и, следовательно, функции соединительной ткани [1].
Выявление определенных САС не должно рассматриваться только как эхокардиографическая находка, а требует комплексной оценки пациента с позиций имеющихся фенотипических критериев наследственных нарушений соединительной ткани для своевременной их диагностики, при некоторых из которых течение САС имеет более неблагоприятный прогноз [1].
В настоящее время не существует общепринятой классификации САС, структурировать которую при современном уровне знаний крайне затруднительно. Наиболее целесообразным представляется объединение ограниченного числа САС по анатомическому, этиологическому принципу и однотипности клинических осложнений [1]. В связи с этим были выделены предсердные САС — аневризма межпредсердной перегородки, открытое овальное окно, Евстахиев клапан, сеть Киари, отдельно — пролапсы клапанов, миксоматозная дегенерация клапанов, аномально расположенные хорды. Внесение в классификацию перечисленных САС определяется их сопряженностью с риском серьезных осложнений и ассоциированных состояний.
Целью данного исследования явилось изучение распространенности, анатомоморфологических и ультразвуковых признаков структурных аномалий сердца: открытого овального окна, аневризмы межпредсердной перегородки, сети Киари, Евстахиева клапана, миксоматозной дегенерации створок митрального клапана, аномально расположенных хорд левого желудочка.
В рамках выполнения работы проведено анатомоморфологическое исследование структурных аномалий сердца на 54 анатомических препаратах сердца, полученных на кафедре нормальной анатомии БГМУ. Выполнено ультразвуковое исследование сердца у 30 пациентов кардиологического профиля учреждения здравоохранения «1 городская клиническая больница» г. Минска. Возраст исследованных пациентов составил от 31 до 73 лет, средний возраст — 57 лет. Проанализированы сканограммы и протоколы эхокардиографии, выполненной 100 пациентам, из архива кафедры ультразвуковой диагностики БелМАПО.
Использованы анатомоморфометрический и статистический методы. Ультразвуковое исследование сердца выполнялось пациентам кардиологического, ревматологического и инфарктного отделений учреждения здравоохранения «1 городская клиническая больница» г. Минска на ультразвуковых аппаратах Siemens Acuson S1000, Toshiba Aplio XG, GE Volusson 730 Expert секторными датчиками с частотой сканирования 2,5‒5 МГц.
При осмотре анатомических препаратов сердец, полученных на кафедре нормальной анатомии БГМУ, в 3,7 % случаев было обнаружено открытое овальное окно (ООО) в виде щелевидного отверстия, расположенного по передневерхней кромке овальной ямки, имевшего туннелеподобное строение и косое направление. ООО по данным эхокардиографии (ЭхоКГ) диагностировано у 3,3 % пациентов при локации кровотока в режиме цветового допплеровского картирования в виде низкоскоростного сброса крови через межпредсердную перегородку в области овальной ямки без признаков перегрузки правых отделов сердца (дилатации, повышения давления в правом предсердии и желудочке, легочной артерии). По данным архива ООО было диагностировано в 9 % случаев, в том числе в 2 % в сочетании с другими САС (сочетание аневризмы межпредсердной перегородки, открытого овального окна и сети Киари).
Наиболее часто с ООО ассоциируются парадоксальная венозная эмболия и мигрень с аурой. К более редким ассоциированным с ООО состояниям относят транзиторную глобальную амнезию, протромботические нарушения, декомпрессионную болезнь, синдром обструктивного ночного апноэ. Частота выявления ООО при криптогенном инсульте крайне высока и составляет от 24 до 66 % случаев [1,3].
Аневризма межпредсердной перегородки (АМПП) по данным морфологического исследования составила 11,1 % случаев, представляла собой мешковидное выпячивание перегородки в зоне овальной ямки в полость правого предсердия глубиной более 1 см, без признаков межпредсердной коммуникации в виде открытого овального окна или дефекта межпредсердной перегородки. АМПП по данным ЭхоКГ была диагностирована в 3 % случаев, из них в 2 % наблюдений структурные аномалии сердца носили множественный характер.
При наличии АМПП и ООО существенно повышается риск развития инсультов, причем риск для лиц младше 55 лет выше при АМПП, чем при изолированном ООО, максимально увеличивается при сочетании АМПП и ООО. Вероятность повторного криптогенного инсульта при сочетании АМПП и ООО увеличивается в 7 раз по сравнению с риском инсульта при изолированном ООО [4].
При анатомоморфологическом исследовании в 5,5 % случаев была обнаружена сеть Киари, представляющая собой сетчатую мембраноподобную структуру с множественными отверстиями и двумя вариантами крепления: с фиксацией к двум зонам ‒ к краю устья нижней полой вены и эндокарду правого предсердия или овальной ямки (3,7 % случаев); и в виде дубликатуры пристеночного эндокарда с множественными точками крепления к эндокарду правого предсердия и распространением от нижней полой вены до овальной ямки (1,8 % случаев). Сеть Киари по данным ЭхоКГ была диагностирована в 3,3 % наблюдений в виде мобильной гиперэхогенной извитой структуры, с хаотичным движением в полости правого предсердия, исходящей от устья нижней полой вены и крепящейся к МПП в области овальной ямки. По данным архива сеть Киари встречалась в 2 % исследований в сочетании с аневризмой межпредсердной перегородки и открытым овальным окном.
Клиническое значение сети Киари заключается в повышении риска развития тромбоэмболии, инфекционного эндокардита; проблемах при внутрисердечных эндоваскулярных вмешательствах.
В 7,4 % случаев при анатомоморфологическом исследовании был выявлен Евстахиев клапан (ЕК). В одном препарате сердца размер ЕК составил 2,5 см, ЕК ограничивал устье нижней полой вены, имел полулунную форму, мембранозный тип строения. В остальных случаях длина ЕК была около 1 см. По данным архива кафедры ультразвуковой диагностики БелМАПО в 1 % выполненных ЭхоКГ был диагностирован удлиненный ЕК.
При возникновении право-левого сброса крови через межпредсердную перегородку удлиненный ЕК может способствовать возрастанию риска парадоксальной эмболии, ассоциированной с ООО. При одновременном сочетании трех аномалий — удлиненного ЕК, АМПП и ООО — у молодых лиц часто отмечают клинические проявления в виде цефалгического синдрома, синкопальных состояний, которые опосредованно могут рассматриваться как следствие микротромбозов в большом круге кровообращения [1]. ЕК может являться субстратом для образования тромбов, что ассоциируется c легочным тромбоэмболизмом. Удлиненный ЕК предрасполагает к суправентрикулярным аритмиям, с наиболее вероятным рефлекторным патофизиологическим механизмом вследствие раздражения пейсмекерных образований предсердия [1,5].
В 14,8 % препаратов сердца было обнаружено миксоматозное изменение митрального клапана, из них в 5,5 % наблюдений ‒ сочетание миксоматозной дегенерации митрального и трикуспидального клапанов. Створки были увеличены, утолщены по краям, бледно-серого цвета. Края створок закручены, с множественными аневризматическими выпячиваниями в виде «парашютов» или аневризм. В 3,7 % случаев были выявлены макроскопические признаки фиброэластиновой недостаточности в виде выраженного истончения створок митрального клапана, в особенности краевой зоны среднего сегмента задней створки. В одном из случаев наблюдалось сочетание фиброэластиновой недостаточности с миксоматозным изменением клапана.
При миксоматозной дегенерации створки митрального клапана по данным ЭхоКГ выглядят парашютообразными, удлиненными, неровными, утолщенными. Характерно их патологическое пролабирование в систолу в полость левого предсердия. На створках образуются округлые выпячивания — фестоны, аневризмы. В патологический процесс вовлекаются обе створки, с преимущественным поражением задней. Наличие миксоматозной деформации оценивается на основании толщины створки митрального клапана, измеренной в фазу диастолы в средней части створки вне зоны отхождения хорд. Общепринятые нормативы толщины створок 2–4 мм, увеличение более 5 мм свидетельствует о миксоматозной дегенерации [1]. По данным архива миксоматозная дегенерация створок отмечалась в 2 % случаев. Миксоматозная дегенерация створок митрального клапана обусловила формирование у обследованных пациентов пролапсов митрального клапана II и III степеней, умеренную-тяжелую и тяжелую митральную регургитацию.
В 31,5 % случаев при анатомоморфологическом исследовании обнаружены аномально расположенные хорды (АРХ) левого желудочка. В нашем исследовании в 25,9 % наблюдений выявлены следующие варианты крепления АРХ: от основания папиллярной мышцы к трабекуле стенки левого желудочка, к трабекулам стенок левого желудочка, от створки митрального клапана к стенке. В 3,7 % наблюдений имел место вариант крепления АРХ от створки митрального клапана к стенке или от створки клапана к межжелудочковой перегородке. Типичным вариантом строения АРХ левого желудочка были многочисленные точки прикрепления (более 2) к структурам сердца. По данным ЭхоКГ частота АРХ составила 20 %, преобладали срединно расположенные поперечные хорды и срединно-апикальные диагональные хорды.
АРХ при микроскопическом исследовании в большинстве случаев имеют травматическое повреждение, локальный и распространенный фиброз, кальциноз, миксоматоз [6]. В мышечных АРХ определяются Пуркинье-подобные клетки. В зонах прикрепления АРХ по данным морфологического исследования наблюдаются нарушения регионарного кровотока: «упругие» свойства АРХ препятствуют расслаблению миокарда в период диастолы, неполноценная диастола не обеспечивает нормальный кровоток в коронарных сосудах, натяжение АРХ ухудшает субэндокардиальный кровоток; синдром гемодинамического перераспределения или «обкрадывания», обусловленный наличием в АРХ артерий различного диаметра и последующим их спазмом при тракции тяжа [7]. АРХ в большинстве случаев сочетаются с другими САС.
Таким образом, структурные аномалии сердца являются аномалиями строения сердца, отличающимися от нормального анатомического строения, диагностируемыми эхокардиографически и морфологически, с доказанной клинической значимостью. Типичен множественный характер структурных аномалий в одном сердце.







