Синдром Протея, или парциальный гигантизм
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Редкое заболевание – синдром Протея – это генетическая мультисистемная патология с выраженными клиническими проявлениями, а именно: с выборочным гигантизмом, поражением системы крово и лимфотока.
Первое упоминание о синдроме принадлежит Майклу Коэну – датировано оно 1979 годом. Через четыре года в Германии патология получила свое нынешнее название – синдром Протея, по имени древнегреческого божества Протея-многоликого.
Часто синдром Протея ошибочно диагностируют, как гамартоматозную болезнь в виде неврофиброматоза, которая передается аутосомно-доминантно.
Другие названия синдрома Протея: болезнь многоликости, заболевание человека-слона, синдром парциального гигантизма.

Код по МКБ-10
Эпидемиология
Синдром Протея считается крайне редкой патологией, так как за все время было обнаружено лишь около двух сотен подобных случаев. Такая статистика позволяет утверждать, что синдром возникает менее чем в 1 случае на 1 млн. новорожденных детей.

Причины синдрома Протея
Причина развития синдрома Протея состоит в определенной генной мутации. Все мы знаем, что человеческий организм имеет большое количество ДНК-цепочек, которые передаются нам от родителей. Но иногда во время эмбрионального развития происходит некий генетический сбой, что и приводит к появлению врожденных генетических заболеваний.
Синдром Протея обнаруживается при измененном гене АКТ: данный белок ответственен за скорость клеточного роста в организме. Если человек здоров, то его ген АКТ находится в неактивном состоянии. У больных синдромом Протея этот ген активен и ускоряет процесс роста клеток.
Тяжесть проявления патологии зависит от того, на каком именно внутриутробном этапе имела место мутация гена. Чем более ранним был этот этап, тем серьезнее будет протекать синдром Протея.
На данный момент ученые работают над такими вопросами:

Факторы риска
Точные факторы, которые влияют на развитие синдрома Протея, неизвестны. Однако ученые выделили ряд факторов, которые теоретически могут способствовать появлению у ребенка такой патологии:

Патогенез
Патогенез синдрома Протея до конца пока не изучен. Известно лишь, что к развитию патологии приводит мозаицизм соматических клеток – аномалия сочетания половых хромосом по доминантному гену, который до настоящего времени не определен.
Тем не менее, и эта теория некоторыми учеными ставится под сомнение, так как имелись одиночные случаи незначительных признаков заболевания у родителей пораженных индивидов.
Сочетанное существование гипер и гипоплазии при синдроме Протея наводит на мысль о возможной эмбриональной соматической рекомбинации, которая становится причиной появления не менее трех клеточных подвидов: нормальных, гипертрофических и атрофических клеточных структур.

Симптомы синдрома Протея
Обычно люди, больные синдромом Протея, в младенческом возрасте не отличаются от других детей: патологические изменения начинают проявляться с годами. Диагностировать синдром Протея поначалу очень сложно, так как первые признаки болезни у каждого больного могут отличаться. Единственным характерным признаком заболевания является разрастание тканей. При этом разрастаться может любая ткань человеческого организма: костная, мышечная, жировая ткань, а также сосуды системы кровообращения и лимфотока. Разрастание может поразить практически любой орган. Правда, больший процент разросшейся ткани фиксируется на конечностях и в области головы.
Синдром Протея напрямую влияет на снижение продолжительности жизни больного, и это объясняется частыми проблемами с сосудами. Среди подобных проблем обычно встречаются тромбоэмболии, тромбозы и т. п. Не менее распространены опухолевые процессы и поражения эндокринной системы.
Сам по себе синдром не оказывает влияния на снижение интеллектуального уровня больного, но патологическое разрастание нервной ткани может спровоцировать значительное отставание умственного развития.
Первые признаки синдрома могут проявляться у детей, начиная с 2-х или 4-х лет. Обычно это такие симптомы:
Осложнения и последствия

Диагностика синдрома Протея
Диагностировать синдром Протея на начальной стадии практически невозможно, так как основными критериями диагностики являются характерные симптомы заболевания:
Анализы для подтверждения диагноза синдрома Протея не проводятся. Обязательно контролируют показатели свертываемости крови, так как для болезни характерны тромбозы и тромбоэмболии.
Инструментальная диагностика может включать в себя рентгенологическое исследование, магнитно-резонансную томографию, компьютерную томографию, ангиографию, энцефалографию и пр.
Иногда при синдроме Протея, особенно при наличии опухолевых процессов, врачи назначают гистологическое исследование с предварительной биопсией.

Дифференциальная диагностика
Дифференциальная диагностика синдрома Протея проводится со следующими заболеваниями:

К кому обратиться?
Лечение синдрома Протея
Синдром Протея считается неизлечимым заболеванием. Однако ранняя диагностика болезни позволяет успешно побороть основные признаки патологии и избежать осложнений. Например, при искривлении позвоночного столба, при избыточном росте костной ткани, при несоответствии длины конечностей больному предлагается применять специальные ортопедические приспособления.
Если же расстройство наблюдается в системе кроветворения, либо обнаруживается рост опухолевых процессов, то больной синдромом Протея должен находиться под пожизненным врачебным наблюдением.
Медикаментозное лечение синдрома Протея состоит только лишь в назначении симптоматических препаратов. К ним относятся обезболивающие средства (Ибупрофен, Кетолонг), мочегонные препараты (Фуросемид, Лазикс), антикоагулянты (Гепарин, Фрагмин, Фондапаринукс, Тинзапарин), вазопрессоры (Допамин, Добутамин), тромболитики (Урокиназа, Стрептокиназа, Альтеплаза).
Лекарства, допускаемые к применению при синдроме Протея
Способ применения и дозы
При болях принимают по 600 мг 2-3 раза в сутки.
Прием может сопровождаться тошнотой, диспепсией, болями в желудке.
Ибупрофен не применяют при нарушении кроветворной функции.
При отеках принимают 20-80 мг в день, с возможным дальнейшим увеличением дозировки.
Возможно понижение давления, слабость, боли в голове, жажда, аллергия.
Прием препарата должен сочетаться с компенсацией электролитных нарушений.
Применяется в качестве антикоагулянта по индивидуальным схемам лечения.
При длительном лечении возможно развитие геморрагических осложнений.
Препарат применяют, постоянно контролируя степень свертываемости крови.
Препарат применяют по индивидуально подобранным схемам.
Длительное лечение может стать причиной появления аритмии, изменения артериального давления.
При лечении препаратом необходимо контролировать ЧСС, кровяное давление, диурез.
Препарат назначают внутривенно капельно, в средней дозировке 250 000 МЕ в 50 мл физраствора со скоростью 30 кап./мин.
Возможна гиперреакция на белок: боль в голове, тошнота, лихорадка.
Лечение проводят с контролем показателей свертываемости крови и уровня фибриногена.
Витамины
Рацион человека, страдающего синдромом Протея, должен включать в себя витаминизированные и сбалансированные по составу блюда. Кроме этого, периодически можно принимать дополнительные витамины – в основном, для укрепления сосудов, сердца, для улучшения состояния и структуры клеток и тканей.
Витаминные препараты обычно назначают индивидуально, так как у некоторых пациентов возможна непереносимость того или иного компонента.
Физиотерапевтическое лечение
Физиотерапия при синдроме Протея обычно направлена на поддержание функции сердечно-сосудистой системы, улучшение коронарного и периферического кровообращения. С улучшением циркуляции крови повышается уровень транспортировки кислорода, облегчается протекание процессов в центральной нервной системе и вегетативной нервной системе, нормализуются нейроэндокринные и иммунные реакции.
Для улучшения состояния пациента с синдромом Протея могут использоваться различные физиотерапевтические методы, в зависимости от доминирующего проявления заболевания.
Противопоказаниями к физиотерапии могут стать:
Выбор конкретной процедуры при синдроме Протея зависит от выраженности функционального расстройства сердечно-сосудистой системы, от состояния нервной и нейрогуморальной системы регуляции кровообращения, а также от наличия других неполадок в организме.
Народное лечение
Для улучшения качества крови при синдроме Протея рекомендуется регулярно употреблять напитки из ягод калины, облепихи, клюквы, черники.
Для профилактики тромбообразования при синдроме Протея полезными считаются чаи и настои на основе мать-и-мачехи, таволги, астрагала, окопника, листьев малины. Заваривают 1 ст. л. травы в ½ л кипящей воды, настаивают под крышкой до остывания. Такое лекарство пьют по половине стакана три раза в сутки.
Огромную пользу оказывает знаменитый имбирный чай: он разжижает кровь и улучшает кровообращение, препятствует скоплению токсинов. Чтобы приготовить лечебный имбирный чай, кусочек имбирного корня натирают на терке и заливают кипятком, настаивают 20 минут. После остывания в напиток добавляют немного меда и/или лимона. Для улучшения лимфотока в такой чай можно добавить щепотку корицы.
Если в пораженных тканях образовались отеки, то используют такой способ: к пораженным участкам прикладывают нарезанный на дольки томат: через 3-4 часа дольки заменяют свежими.
Пример лечения синдрома Протея при помощи мумиё:
Курс лечения можно провести повторно через 5 дней. Всего рекомендовано 4 курса.
Пораженные участки можно обрабатывать мазью, которая представляет собой 20% разведенное мумиё в смеси с вазелином.

Лечение травами
Гомеопатия
На сегодняшний день многие медицинские специалисты признали эффективность гомеопатических препаратов в лечении различных, в том числе и хронических, заболеваний. Существуют и такие гомеопатические средства, которые могут помочь, если не вылечить, то значительно ослабить проявления такой болезни, как синдром Протея.
К примеру, Лимфомиозот – это комплексный гомеопатический препарат немецкого производства, который выполняет сразу несколько полезных функций в организме:
Лимфомиозот можно приобрести в аптеках в виде капель, таблеток или инъекционного раствора. Препарат рекомендован к применению по предписанию доктора трижды в сутки (таблетки или капли), либо 1-3 раза в неделю (внутримышечные или подкожные инъекции). Курс лечения Лимфомиозотом может продолжаться долго, при необходимости до нескольких месяцев.
Для того, чтобы усилить эффективность препарата, его можно сочетать с другими гомеопатическими средствами. Чаще всего используют такие препараты: кониум, туя, кальциум флюорикум. Реже и по показаниям – солянум туберозум, сукцинум, апис и тропеолум.
Кроме этого, в течение последнего десятилетия активно используют потенцированные кейлоновые средства (препараты-регуляторы митотического клеточного деления), средства эпидермального фактора роста (EGF), средства фактора роста фибробластов (FGF).
Перечисленные препараты практически лишены неприятных побочных эффектов, однако могут существенно улучшить состояние больных синдромом Протея.
Оперативное лечение
Некоторые виды тканевых разрастаний при синдроме Протея требуют оперативной коррекции. Например, при челюстных деформациях приводятся:
При наличии кожных и подкожных разрастаний, поверхностных гемангиом, может применяться их лазерное удаление или криодеструкция. Кистозные образования и опухоли (в том числе и внутренние) удаляют оперативным путем.
Некоторые операции при синдроме Протея проводятся по эстетическим соображениям – к примеру, если разрастание ткани обнаруживается в области лица или головы.
Синдром Протея
Синдром Протея – это редкая врожденная патология, проявляющаяся аномальным ростом отдельных частей тела. Обычно выявляется увеличение участка головы, руки или ноги. Частичная гипертрофия сочетается с повышенной вероятностью развития тромбозов и тромбоэмболий, образования опухолей различной структуры и локализации. Диагноз выставляется на основании результатов осмотра, данных рентгенографии, КТ, МРТ, ангиографии, допплерографии. Радикальное лечение не разработано. Применяются ортопедические приспособления, по показаниям осуществляются операции для улучшения функций конечности, облегчения дыхания и приема пищи, выполняется хирургическое удаление неоплазий.
МКБ-10
Общие сведения
Синдром Протея (парциальный гигантизм) – очень редкое врожденное заболевание. В литературе упоминается примерно 200 случаев данной патологии, при этом специалисты не исключают, что некоторые пациенты могли страдать другими болезнями со сходной симптоматикой. Первое описание синдрома было представлено в 1979 году, однако широкую известность он получил после публикации работы немецкого педиатра Видемана в 1983 году. Название также было предложено Видеманом по ассоциации с древнегреческим богом Протеем, способным к изменению внешнего облика. Заболевание оказывает выраженное негативное влияние на качество жизни больных, как из-за внешнего обезображивания, так и вследствие нарушений функций пораженных частей тела. Нередко становится причиной ранней смерти из-за высокой вероятности развития опухолей и склонности к тромбозам.
Причины
Причиной развития заболевания является соматический мозаицизм, предположительно обусловленный случайной мутацией доминантного гена. Некоторые специалисты подвергают сомнению случайный характер мутации, опираясь на информацию о выявлении нескольких случаев легких признаков синдрома у родителей больных. Существуют исследования, согласно которым патология обусловлена мутацией гена PTEN, расположенного в локусе 10q X хромосомы. Вместе с тем, исследователи указывают, что мутации данного гена обнаруживаются всего у 20% пациентов с синдромом Протея и определяются при некоторых других заболеваниях, характеризующихся повышенной вероятностью образования злокачественных неоплазий. Таким образом, генетическая основа болезни пока окончательно не установлена.
Патогенез
В результате мутации в отдельных частях тела образуется три вида клеток – нормальные, гипер- и атрофические. На измененном участке в процесс вовлекаются кожные покровы, костная, мышечная и жировая ткань, лимфатические и кровеносные сосуды, что вызывает деформацию, увеличение длины и объема конечности или части головы, изменения сосудов. Поскольку дефектный ген является супрессором опухолей, наличие мутации резко повышает вероятность появления новообразований.
Симптомы
При рождении признаки заболевания отсутствуют. Патологические проявления возникают в раннем детском возрасте. Клиническая картина полиморфная. Характерными симптомами являются аномальное увеличение одной или нескольких конечностей, макроцефалия, сосудистые аномалии (мальформации, варикозное расширение вен). У некоторых больных выявляются офтальмологические нарушения: экзофтальм, косоглазие, миопия. При патологическом росте нижней челюсти формируется прогения. Возможно разрастание кожи в области подошв. В числе возможных вариантов патологии в литературных источниках упоминается изолированное увеличение селезенки или пальцев рук, атрофия зрительного нерва и пигментная дегенерация сетчатки в сочетании с множественными менингиомами.
Увеличение нижних конечностей влечет за собой нарушение опоры и движений. Пациенты вынуждены пользоваться ортопедической обувью и специальными приспособлениями (тростью, костылями, инвалидной коляской). При увеличении верхних конечностей наблюдаются трудности в процессе самообслуживания. Из-за деформации частей головы возникают грубые косметические дефекты, могут отмечаться затруднения при дыхании и приеме пищи. Существует высокая вероятность развития новообразований различной локализации и гистологической структуры: гамартом, липом, лимфангиом, гемангиом, аденом слюнных желез, менингиом и других.
Осложнения
Типичным признаком болезни Протея является возникновение злокачественных опухолей, существенно сокращающих продолжительность жизни больных. Другими опасными для жизни последствиями заболевания считаются осложнения сосудистых патологий. Отмечается повышенный риск тромбоза глубоких вен. Описаны случаи развития тромбоэмболии легочной артерии. Из-за увеличения и разницы в длине нижних конечностей возрастает нагрузка на суставы и позвоночник, формируется искривление позвоночного столба. Обнаруживаются вторичные артрозы, остеохондроз. Более чем у половины пациентов выявляется умственная отсталость, обусловленная сдавлением нервных тканей увеличенными костями черепа. Возможны судороги, неврологические расстройства.
Диагностика
Из-за незначительной распространенности, сходства синдрома Протея с некоторыми другими врожденными заболеваниями постановка диагноза может представлять значительные затруднения. В процессе диагностического поиска принимают участие специалисты в области онкологии, травматологии и ортопедии, сосудистой хирургии и пр. В качестве основных критериев рассматривают гемигипертрофию, сосудистые аномалии и склонность к образованию опухолей. План обследования включает:
При нарушениях со стороны органа зрения назначается офтальмологическое обследование, при умственной отсталости применяются тесты для определения уровня интеллекта, когнитивных способностей. При судорожном синдроме, расстройствах деятельности центральной и периферической нервной системы показана консультация невролога. Заболевание дифференцируют с врожденным липоматозом и синдромами Клиппеля-Треноне-Вебера, Маффучи, Баннайана-Зоннана, при которых также выявляются опухоли, частичная гипертрофия и патология сосудов.
Лечение синдрома Протея
Патогенетическая терапия не разработана, лечение только симптоматическое. По показаниям осуществляют ортопедическую коррекцию с использованием специальной обуви, ортезов, корсетов при вторичных изменениях позвоночника. Назначают медикаментозную терапию для профилактики тромбозов. Из-за вовлечения различных органов и систем оперативные лечебные мероприятия проводятся разными специалистами, в том числе – ортопедами, онкологами, нейрохирургами, вертебрологами, сосудистыми хирургами, хирургами-косметологами, челюстно-лицевыми хирургами и т. д. Можно выделить следующие группы операций при синдроме Протея:
Прогноз и профилактика
Синдром Протея является инвалидизирующим заболеванием, негативно влияет на продолжительность жизни пациентов. По данным исследований, многие больные погибают в детстве или молодом возрасте. Причинами летального исхода становятся злокачественные неоплазии, ТЭЛА, тромбозы крупных сосудов. Профилактические мероприятия не разработаны из-за врожденного характера патологии и недостаточной изученности этиологии болезни. Пациентам, страдающим данным заболеванием, необходимо регулярно проходить обследование для оценки состояния свертывающей системы крови, раннего выявления новообразований.
Синдром протея что это
Врожденное отсутствие отдельных мышц встречается достаточно часто и обычно носит асимметричный характер. Нередко наблюдается аплазия длинной ладонной мышцы на передней поверхности предплечья. Эта мышца отсутствует у 30 % здоровых людей, ее функция полностью компенсируется функцией других сгибателей запястья.
Одностороннее отсутствие грудинно-ключично-сосцевидной мышцы — одна из причин врожденной кривошеи. Отсутствие большой грудной мышцы служит компонентом синдрома Poland. При изменении иннервации мышц, например мышц нижних конечностей при тяжелых формах миеломенингоцеле, возможно нарушение развития мышц. При сакральной аге-незии аномалия сомитов приводит к дефекту формирования позвонков, что может служить причиной патологии мышц, развивающихся из той же аномальной мезодермальной пластинки; нарушение индукции вызывает сегментарную амиоплазию.
При отсутствии формирования длинных костей не происходит дифференцировки скелетных мышц конечностей из эмбриональных миомеров. Отсутствие одной длинной кости, такой как лучевая кость, ассоциируется с вариабельной степенью аплазии или гипоплазии соответствующих мышц, таких как лучевой сгибатель кисти. Конечную стадию неврогенной атрофии мышц иногда называют амиоплазией, хотя это название терминологически неточно.
Генерализованная амиоплазия обычно приводит к смерти плода; родившиеся живыми новорожденные редко выживают. Генетические исследования, проводимые на мышах, позволяют предположить, что в основе заболевания лежит мутация в одном из миогенных генов, однако в настоящее время это предположение не подтверждено в исследованиях на людях.
Мышечная дисгенезия (синдром Протея)
Синдром Протея — это нарушение клеточного роста с вовлечением эктодермальной и мезодермальной ткани. Причина заболевания неизвестна, однако синдром Протея не подчиняется менделевскому типу наследования. Заболевание проявляется в виде асимметричного избыточного роста конечностей, бородавчатых изменений на коже, ангиом различных типов, утолщения костей, гемимегалэнце-фалии и избыточного роста мышц при отсутствии мышечной слабости. При гистологическом исследовании мышц характерна мышечная дисгенезия.
Аномальные зоны прилегают к зонам нормально сформированных мышц и не соответствуют анатомическим границам. Заболевание может быть вызвано патологией секреторных ростовых факторов. Историческим примером заболевания служит «человек-слон», известный своим гротескным обликом, живший в Лондоне в конце XIX в. Этот человек вызвал настоящую сенсацию в обществе. Долгое время считалось, что он страдает нейрофиброматозом, однако в настоящее время этот случай расценивается как синдром Протея.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «неврология»
Инфекции, вызываемые возбудителями рода PROTEUS (Протей)
В последние годы инфекционисты отмечают рост заболеваний, обусловленных нетрадиционными микроорганизмами. Особое место занимает протейная инфекция. Ее кишечная форма, вызванная бакетриями рода Протей — P. vulgaris протекает тяжелее у детей раннего возраста. Не менее опасны гнойно-воспалительные заболевания мочевыводящей системы, вызываемые P. mirabilis, P. rettgeri и P. morganii.
В греческой мифологии Протей – божество, способное менять облик. Отсюда название полиморфных, мелких, нитевидных палочек, отличающихся активной подвижностью. Размеры клеток составляют 0,5 — 3 мкм. P. morganii, P. rettgeri — менее полиморфны и малоподвижны.
Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Протей – факультативный анаэроб, палочковидная, неспороносная, подвижная, грамотрицательная бактерия. В микробиологическом анализе кала протей встречается в комплексе с другими условно-патогенными бактериями семейства энтеробактерий. Кроме протея, в составе нормальной микрофлоры кишечника человека определяются: клебсиелла, энтеробактер, гафния, серратия, морганелла, провиденция, цитробактер. В 1 г кала должно быть меньше 10 4 общего количества этих бактерий. Большее количество перечисленных бактерий является признаком дисбактериоза.
В природе бактерии рода Proteus обнаруживаются: в сточных водах, в земле, в водоемах, на овощах, в разлагающихся органических веществах. Эти микроорганизмы — сапрофиты, они живут на слизистых оболочках, на коже, в кишечнике человека и животных. Протеи устойчивы во внешней среде и сохраняют жизнедеятельность в слабых растворах фенола и других средств. Выявлена также резистентность ко многим антибиотикам.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Инфицирование протеем может произойти через полуфабрикаты, сырые продукты или готовые блюда из мяса, рыбы, молока, колбасы, студня. В них происходит быстрое размножение бактерий с образованием токсинов. Реже отмечают водный путь передачи: при купании в загрязненных водоемах или употреблении инфицированной воды. Возможен и контактный путь передачи на инфицированных руках зараженного человека.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Протеи выделяют токсические вещества — эндотоксины с гемолитическими свойствами и с различной степенью биохимической активности. У штаммов P. vulgaris обнаружена лецитиназная активность. Протеи обладают способностью адгезии к уротелию при помощи ресничек. Отмечают, что резистентность к антибиотикам связана с адгезивной способностью уропатогенных протеев.
Острой кишечной протейной инфекцией, протекающей по типу гастроэнтерита, гастрита и колиэнтерита часто болеют дети раннего возраста с пониженным иммунитетом и после бесконтрольного назначения антибиотиков. Заболевание сопровождается симптомами токсикоза — повышением температуры, рвотой, метеоризмом, схваткообразными болями в животе, нарушением аппетита, кратковременными судорогами, появлением водянистого, зловонного, учащенного стула.
В тяжелых случаях могут развиться осложнения: гемолитико-уремический синдром, а также симптомы острой гемолитической тромбопении, анемии или острой почечной недостаточности.
Клинические проявления внутрибольничной инфекции протейной этиологии весьма разнообразны: поражения мочевыводящей системы, отиты, холециститы, нагноения ран и септические состояния. Попадание протеев в пупочную ранку новорожденного может привести к бактериемии или развитию менингита.
Данные заболевания могут развиться: при передаче возбудителя контактно-бытовым или воздушно-капельным путями, при заносе с катетером, другими урологическими инструментами.
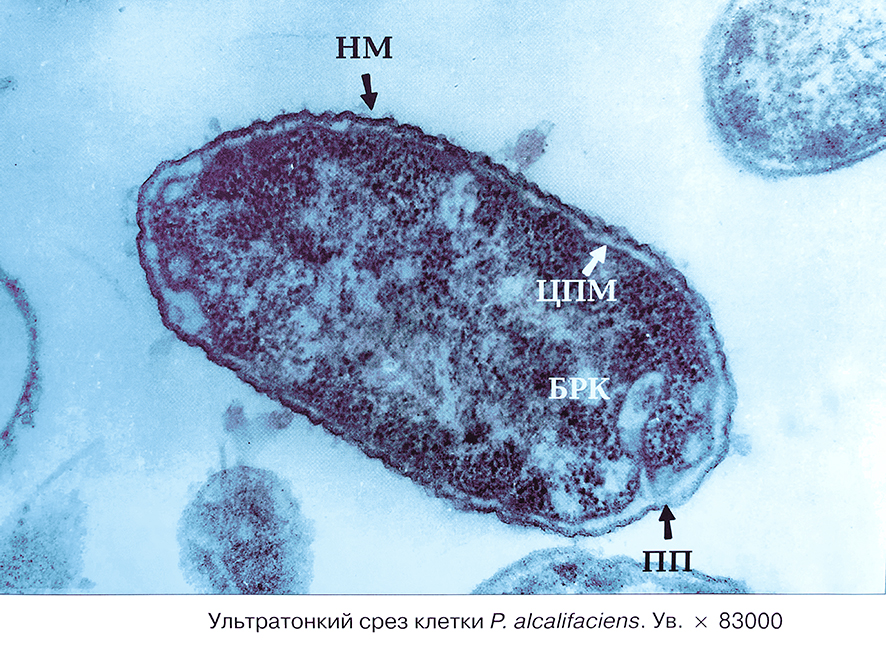
Если в мазках исследуемого материала (участки ожоговой ткани, гной, раневое отделяемое, испражнения) обнаруживаются грамотрицательные палочки, то бактериоскопический метод позволяет сделать предварительное заключение. Бактериологическим методом на средах определяют колонии протея в виде тонкого стелющегося налета. Активно размножаются протеи на белковой питательной среде вызывают гниение мяса, рыбы, других белковых продуктов.
Важнейшие профилактические меры — это соблюдение санитарного режима в детских учреждениях и стационарах, проведение общесанитарных мероприятий. Для профилактики протея каждому необходимо соблюдать правила личной гигиены, исключить потребление подозрительных продуктов в питании, избегать контактов с больными детьми и взрослыми.
При лечении протейной инфекции следует придерживаться лечебной щадящей диеты с исключением жареных, острых блюд, белковых продуктов. В острый период протейного инфицирования, при поражении желудочно-кишечного тракта — необходимо обеспечить восполнение потерянной жидкости. Полезно употреблять отвары трав – тысячелистника, алтея, зверобоя, ромашки, календулы; морсы, компоты с клюквой, черной смородиной, абрикосами, черникой, яблоками. Применять антибиотики можно только по назначению врача, в соответствии с данными анализов чувствительности бактерии протея к ним.
Обязательно нужно принимать препараты – пробиотики, пребиотики, синбиотики для восстановления нормальной флоры кишечника.
Синбиотические комплексы Нормофлорины, содержащий живые активные лакто- и бифидобактерии, секретирующие молочную, уксусную, масляную, пропионовую кислоты, оказывающие защитное, антисептическое, противовоспалительное, сорбционное действие – уменьшает интоксикацию, улучшает моторику кишечника, функцию печени, повышает иммунную реактивность. Это помогает в борьбе с протейной инфекцией, восстанавливает работу желудочно-кишечного тракта, общее самочувствие, повышает иммунитет.
Схема (возрастные дозировки для детей или взрослых): (взрослый) нормофлорин Л – 20 мл (при диарее) – 40 (при запорах) мл утром перед едой, Д — 40 мл вечером за 20 мин до еды, Б – 20-30 мл на ночь в клизме. При диарее в обед можно добавить Д – 30-40 мл, при запорах в обед + Л – 30-40 мл.
Курс приема нормофлоринов — 1 — 1,5 месяца, для выведения токсинов, патогенной микрофлоры, восстановления полезных собственных бактерий. Уникальный состав нормофлоринов, не содержащих белков коровьего молока, молочного сахара, консервантов позволяет при протейной инфекции успешно применять его у детей с первых дней жизни, беременных, кормящих, больных сахарным диабетом, аллергическими заболеваниями, т.е. у взрослых при любой сопутствующей патологии.
Опасность протейной инфекции

Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
protey_mirabilis
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.