Синдром Шегрена
Аутоиммунное заболевание – это нарушение иммунной системы, которое разрушает ее собственные клетки и ткани. При синдроме Шегрена лимфоциты атакуют слюнные железы, железы вокруг глаз и слизистые оболочки, что приводит к нарушению выработки слез и слюны и, как следствие, к воспалению. Он также может повредить суставы, кожу, нервы, легкие, печень и щитовидную железу.
Точные причины синдрома сухости неизвестны – факторы, способствующие развитию синдрома Шегрена, включают генетические условия, носитель определенных антигенов гистосовместимости и инфекцию от некоторых вирусов (например, ВИЧ, гепатит С или вирус Эпштейна-Барра). Причины синдрома Шегрена также видны при ревматических заболеваниях, поскольку эти заболевания часто возникают одновременно. Поскольку заболевание чаще всего поражает женщин в климактерическом периоде, врачи подозревают, что оно также может иметь гормональный фон.
Существует два типа синдрома Шегрена: первичный (независимый) синдром и вторичный синдром, сопровождающий другие аутоиммунные заболевания.
Синдром Шегрена – симптомы
Симптомы синдрома Шегрена можно разделить на две группы.
1. Симптомы поражения слезных желез:
2. Симптомы поражения слюнных желез:
Другие симптомы болезни Шегрена включают:
Осложнения после синдрома Шегрена включают кариес, грибковую инфекцию полости рта и нарушение зрения. Иногда болезнь проявляется неврологическими симптомами, такими как сенсорные расстройства, усталость, или психиатрическими симптомами, такими как тревога и депрессия.
Лечение синдрома Шегрена
В связи с неизученными причинами заболевания лечение синдрома Шегрена носит только симптоматический характер. Если болезнь легкая, используйте глазные капли и пейте много воды, чтобы избежать обезвоживания. Медикаментозное лечение требуется, когда синдром находится в острой фазе заболевания. Используются препараты, повышающие выработку слюны, предотвращающие воспаления и грибковые инфекции, а также препараты системного действия. Также продолжаются работы по биологическому лечению синдрома Шегрена – препараты этого типа проходят испытания.
Чтобы уменьшить сухость глаз, при синдроме Шегрена проводят хирургическое вмешательство по закрытию слезных протоков, отводящих слезы из глаз. Эта небольшая процедура включает вставку силиконовых или коллагеновых пробок в канальцы или закрытие канальцев лазером.
Вылечить больных можно с помощью различных глазных капель, увлажняющих гелей и мазей, искусственной слюны и компрессов для глаз. При синдроме Шегрена не стоит забывать носить солнцезащитные очки и защищать кожу от солнца.
Пациенты пытаются лечить синдром Шегрена естественными средствами или нетрадиционными методами лечения. Есть мнение, что детоксикация организма может помочь в лечении этого состояния. Естественное лечение синдрома также включает употребление трав и иглоукалывание.
Диета при болезни Шегрена
Диета не играет роли в лечении этого состояния, но может помочь облегчить симптомы синдрома сухости. Каждый случай индивидуален, поэтому также нужно проконсультироваться по этому поводу со своим врачом и диетологом. Однако есть некоторые общие правила, которым должны следовать люди с синдромом Шегрена. В первую очередь следует пить много воды. Необходимо исключить фаст-фуд, газированные напитки, соленые и острые продукты и большое количество сладостей, особенно тех, которые растворяются во рту, например, конфеты или шоколад. Стоит есть большое количество овощей и фруктов, а также продуктов с высоким содержанием железа и калия, а также пить разные виды соков.
Прогноз
В настоящее время синдром Шегрена не поддается лечению. Его осложнения и общий прогноз зависят от тяжести симптомов. Необходимы постоянное наблюдение за телом и частые консультации врача для проверки слюнных желез, лимфатических узлов и внутренних органов, а также регулярные лабораторные исследования.
Что такое синдром Шёгрена? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бабинцевой Марины Юрьевны, эндокринолога со стажем в 27 лет.
Определение болезни. Причины заболевания
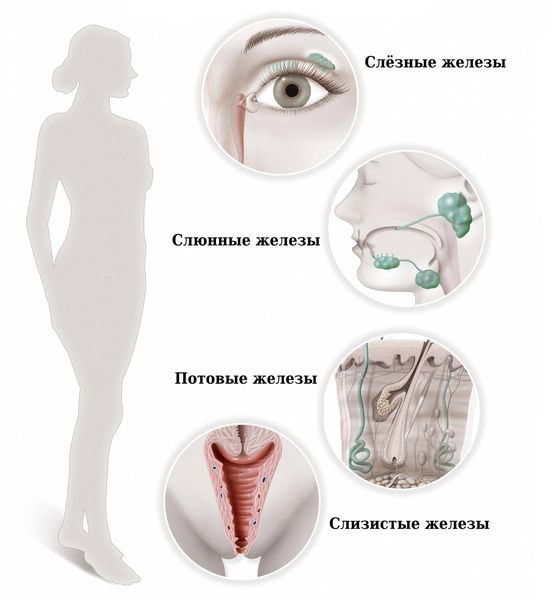
Синдром Шёгрена (Sjogren’s syndrome) — это аутоиммунное системное заболевание соединительной ткани, при котором поражаются железы внешней секреции: преимущественно слёзные и слюнные, а также потовые, сальные, слизистые и др. Характерными признаками болезни являются сухость глаз, полости рта и кожи.
Синонимы: болезнь Шёгрена, синдром Съегрена, «сухой» синдром, ксеродерматоз, синдром Предтеченского — Гужеро — Шёгрена.
Синдром Шёгрена бывает первичным и вторичным:
Распространённость
Причины развития синдрома Шёгрена
Наличие похожей патологии слюнных желёз у родственников (братьев и сестёр, родителей или детей) указывает на генетическую предрасположенность к развитию болезни Шёгрена.
Факторы риска развития синдрома Шёгрена
Симптомы синдрома Шёгрена
Проявления синдрома Шёгрена разнообразны. Среди них можно выделить две группы симптомов:
Симптомы, связанные с поражением желёз
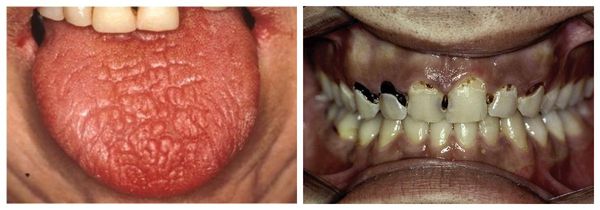
Нарушение работы слюнных желёз проявляется сухостью во рту (ксеростомией). Это второй постоянный симптомом «сухого» синдрома. Ещё до начала клинически выраженной картины болезни Шёгрена можно заметить сухость губ, «заеды» в уголках рта и стоматит. Со временем уменьшается количество слюны и появляется сухость во рту. Сначала она беспокоит только при волнении и физической нагрузке, затем постоянно. Больному приходится запивать сухую пищу и увлажнять рот во время разговора.
Поражение подслизистых желёз трахеи и бронхов вызывает у пациентов сухой лающий кашель.
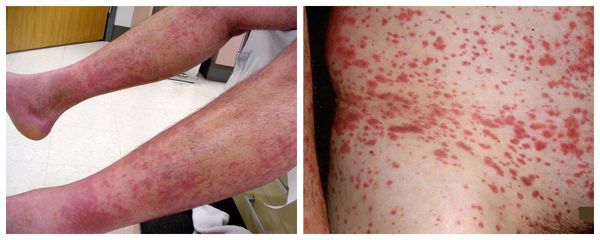
Поражение потовых и сальных желёз — причина сухости кожи при болезни Шёгрена. Нарушение работы потовых желёз наружных половых органов вызывает жжение, зуд, иногда интенсивные жгучие боли.
Поражение желудочно-кишечного тракта часто становится причиной боли в животе различной локализации, тошноты, отрыжки воздухом с тухлым запахом и др. [1] [2]
Внежелезистые системные проявления
Патогенез синдрома Шёгрена
Механизм развития синдрома Шегрена неясен. Считается, что под воздействием стресса или каких-либо факторов окружающей среды у генетически предрасположенных людей нарушается работа иммунной системы, что и приводит к развитию болезни.
Например, в слюнных железах под воздействием провоцирующих факторов повышается проницаемость клеточных мембран. Из-за этого секрет, который образуется в клетках желёз, не поступает в проток, он переполняет клетку и проникает через её оболочку в интерстициальную (соединительную) ткань. Белок, содержащийся в секрете, попадая в интерстициальную ткань, воспринимается организмом как чужеродный и вызывает образование антител против ткани железы.
Классификация и стадии развития синдрома Шёгрена
Классификация болезни Шёгрена по течению:
1. Подострый вариант. Он начинается с повышения температуры до 38–40 ˚C и симптомов одностороннего или двустороннего паротита (воспаления околоушных слюнных желёз). Пациент при этом чувствует дискомфорт, распирание или боль в проекции околоушных слюнных желёз. Эта область припухает, а при выраженном воспалительном отёке железы значительно увеличиваются в размерах.
Форма лица становится грушевидной. Кожа над поражённой слюнной железой туго натянута, лоснится, кожные складки не образуются или образуются с трудом. Также характерно выраженное поражение суставов: чаще воспаляются мелкие суставы кистей, но иногда процесс затрагивает и крупные суставы (коленные, плечевые, локтевые). Воспаление сопровождается сильной болью в суставах.
В анализах крови наблюдается увеличенная скорость оседания эритроцитов (СОЭ), повышенный уровень определённых иммуноглобулинов (антител), снижение количества лейкоцитов и высокие титры ревматоидного фактора. Подострый вариант болезни чаще развивается у молодых пациентов.
Нарушения параметров крови выражены умеренно, системные проявления, такие как регионарная лимфоаденопатия (увеличение лимфатических узлов), поражение почек и другие, отмечаются крайне редко. Этот вариант течения синдрома Шёгрена чаще встречается у пациентов старше 50 лет.
По стадиям развития:
По степени активности:
Осложнения синдрома Шёгрена
Инфекционные осложнения. Из-за сухости полости рта, носоглотки, слизистых оболочек глаз и изменения состава слюны и слёзной жидкости присоединяются бактериальные, герпесные или грибковые кератоконъюнктивиты, синуситы, трахеобронхиты и пневмонии.
Злокачественные проявления:
Поражение центральной и периферической нервной системы часто бывает опасно жизнеугрожающими осложнениями. Они возникают у 2–4 % больных. К таким осложнениям относятся острое нарушение мозгового кровообращения (инсульт), поражение ЦНС по типу рассеянного склероза, поперечный миелит, тяжёлый цереброваскулит и др. [10]
Диагностика синдрома Шёгрена
Пациент с начальными признаками болезни Шёгрена может оказаться на приёме у стоматолога, офтальмолога, оториноларинголога, терапевта и ревматолога. Диагностика основана на выявлении у больных одновременного поражения глаз и слюнных желёз, а также лабораторных признаков аутоиммунного заболевания.
Сбор жалоб и осмотр
К типичным офтальмологическим симптомам болезни относят постоянную сухость глаз на протяжении трёх месяцев и более, ощущение песка в глазах, необходимость использовать искусственные слёзы три раза в день и чаще.
При осмотре врач отмечает сухость склеры и конъюнктивы, расширение сосудов конъюнктивы, белые или желтоватые выделения крошковатого вида или густой вязкой консистенции. Из-за уменьшения слёз развивается сухой конъюнктивит или блефароконъюнктивит с дистрофией и изъязвлением слизистой оболочки глаз.
Состояние слюнных желёз сначала определяют с помощью сиалометрии, когда врач собирает слюну пациента в пробирку, затем оценивает её количество. Также слюнные железы исследуют с помощью инструментальных методов диагностики.
Инструментальная диагностика
Сиалография. Это рентгенконтрастное исследование слюнных желёз. При синдроме Шёгрена сиалография показывает характерные признаки: изменение строения долек и повреждение протоков железы. Также определяется выход контрастного вещества в ткань желёз за пределы протоков. Поэтому контуры протоков нечёткие, вокруг них определяется «облачко» контрастной массы, проникшей в окружающие ткани.
УЗИ и МРТ. Эти методы позволяют оценить структуру желёз и внутрижелезистых лимфоузлов, контролировать динамику лечения и отличить болезнь от опухоли слюнных желёз.
Лабораторная диагностика
В ходе лабораторной диагностики выполняют:
Дифференциальная диагностика
Лечение синдрома Шёгрена
Лечение проводится в зависимости от наличия железистых и внежелезистых проявлений и иммуновоспалительной активности заболевания.
В первую очередь всем пациентам с синдромом Шёгрена рекомендуется немедикаментозное лечение:
Лечение железистых проявлений
При поражении слюнных желёз используют заменители слюны. Их изготавливают на основе муцина и метилцеллюлозы, они смазывают и увлажняют полость рта, облегчая состояние пациента.
Часто удаётся стимулировать остаточную функцию слюнных и слёзных желёз, для этого используются агонисты М1 и М3 мускариновых рецепторов: Пилокарпин или Цевимелин.
Лечение внежелезистых проявлений
Основой лекарственной терапии болезни Шегрена являются две группы препаратов:
Они назначаются при системных проявлениях заболевания и высокой активности процесса, подтверждённой лабораторными показателями.
Пациентам с васкулитом назначается Циклофосфан в комбинации с Преднизолоном. Дозы подбираются в зависимости от тяжести внежелезистых симптомов. Доза Преднизолона при тяжёлых угрожающих жизни системных проявлениях увеличивается.
У пациентов с такими симптомами может использоваться также пульс-терапия Преднизолоном или комбинированная пульс-терапия Преднизолоном и Циклофосфаном. При этом в начале лечения применяются значительные дозы препаратов, затем они снижаются и пациент длительно получает умеренные или низкие дозы. Пульс-терапия позволяет уменьшить ежедневную дозу пероральных глюкокортикоидов и цитостатиков и избежать осложнений, возникающих из-за их длительного применения. Длительный приём глюкокортикоидов может привести к стероидному диабету, язве желудка или двенадцатиперстной кишки, повышению артериального давления и др. Цитостатики уменьшают количество нейтрофилов и тромбоцитов, токсично влияют на сердце, печень и почки. Кроме того, применение препаратов обеих этих групп снижает иммунитет и повышает риск присоединения инфекции.
Экстракорпоральная терапия — это метод интенсивной терапии болезни Шёгрена. К ней относится гемосорбция, криоаферез, плазмоферез, двойная фильтрация плазмы, которая проводится одновременно с пульс-терапией. Эти методы основаны на очистке крови и плазмы от циркулирующих иммунных комплексов и агрессивных аутоантилел вне тела пациента на специальном оборудовании.
Абсолютные показания для экстракорпоральной терапии:
Прогноз. Профилактика
Кроме нарастающего поражения слюнных и слёзных желёз со временем прогрессируют и внежелезистые проявления. Причиной летального исхода может быть генерализованный васкулит, опухоли (чаще всего желудочно-кишечного тракта) и аутоиммунные пацитопении (одновременное снижение лейкоцитов, эритроцитов и тромбоцитов), реже интерстициальный нефрит с почечной недостаточностью, острый инфаркт миокарда и острое нарушение мозгового кровообращения.
Факторы риска неблагоприятного исхода при болезни Шёгрена: анемия, лейкопения или тромбоцитопения, генерализованная лимфаденопатия, спленомегалия (увеличение селезёнки), значительное увеличение околоушных слюнных желёз, полиневропатия, криоглобулинемическая пурпура. Эти факторы могут возникать одновременно, или один фактор может предшествовать другому.
Профилактика синдрома Шёгрена
Первичная профилактика направлена на предотвращение болезни. Так как этиология болезни Шёгрена неизвестна, методов первичной профилактики не существует.
Вторичная профилактика проводится, чтобы предотвратить прогрессирование болезни и развитие осложнений. Для этого необходимо своевременное и адекватное лечение. Чтобы начать лечение как можно раньше, пациенту нужно обратиться к врачу при первых признаках болезни: сухости глаз и полости рта, рецидивирующей или постоянной припухлости в области слюнных желёз. Насторожить должен также прогрессирующий множественный пришеечный кариес.
БОЛЕЗНЬ ШЕГРЕНА
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Подробно рассмотрены вопросы этиологии и патогенеза, патоморфологии и диагностики, в том числе дифференциальной, болезни Шегрена. Даны рекомендации по лечению заболевания и симптоматической терапии его офтальмологических, стоматологических, гастроэнтерологических и других проявлений.
В.И. Васильев — Институт ревматологии РАМН, Москва
V.I. Vasilyev — Institute of Rheumatology Academician of the Russian Academy of Medical Sciences, Moscow
Наиболее информативными лабораторными показателями при БШ являются высокая СОЭ, лейкопения, гипергаммаглобулинемия (80–70%), наличие антинуклеарных и ревматоидных факторов (90–100%), а также антител к растворимым ядерным антигенам SS-A/Ro и SS-B/La (60–100%). У трети больных обнаруживаются криоглобулины, которые могут быть поликлональными или моноклональными в зависимости от иммуноглобулинов, входящих в их состав. Моноклональные иммуноглобулины (IgM и IgA) с легкими цепями обнаруживаются в криопреципитатах и биоптатах слюнных желез в ранних стадиях заболевания, что затрудняет проведение дифференциальной диагностики между БШ с трансформацией в злокачественную лимфому и доброкачественной лимфопролиферацией при этом заболевании.
В поликлинических условиях целесообразно учитывать различные сочетания следующих симптомов:
• артралгии или (реже) неэрозивный артрит мелких суставов кистей;
• рецидивирующий паротит и постепенное увеличение околоушных желез;
• сухость слизистой оболочки полости рта (носоглотки) и быстрое развитие множественного, преимущественно пришеечного, кариеса зубов;
• рецидивирующий хронический конъюнктивит;
• синдром Рейно;
• стойкое повышение СОЭ (свыше 30 мм/ч);
• гипергаммаглобулинемия (свыше 20%);
• наличие ревматоидного фактора в крови (титр более 1: 80).
Хотя ни один из этих признаков, взятый в отдельности, не является специфичным для БШ, наличие четырех признаков и более позволяет в 80–70% случаев заподозрить и в дальнейшем с помощью специальных методов исследования подтвердить диагноз БШ.
Критерии диагноза БШ
• Сухой кератоконъюнктивит:
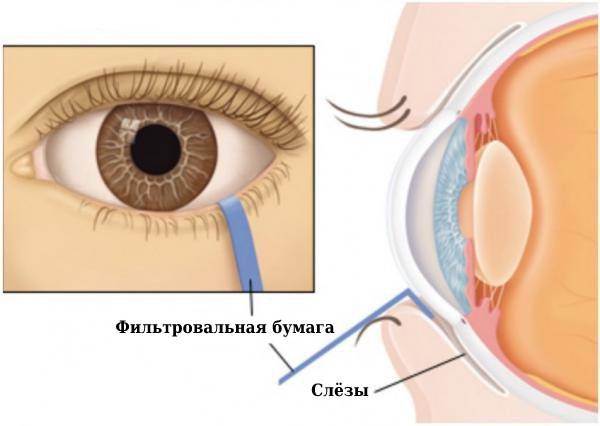
а) снижение слезовыделения после стимуляции нашатырным спиртом, тест Ширмера (менее 10 мм/5 мин);
б) окрашивание эпителия конъюнктивы и роговицы бенгальским розовым или флюоресцеином с последующей биомикроскопией.
• Паренхиматозный паротит:
а) обнаружение полостей более 1 мм при сиалографии;
б) уровень стимулированной секреции слюны менее 2,5 мл/5 мин;
в) очагово-диффузная, диффузная лимфоплазмоклеточная инфильтрация в биоптатах слюнных желез нижней губы.
• Лабораторные признаки системного аутоиммунного заболевания:
а) положительный ревматоидный (антинуклеарный) фактор;
б) обнаружение Ro/La антиядерных антител.
Диагноз определенной БШ может быть поставлен при наличии трех критериев и исключении других диффузных болезней соединительной ткани, ревматоидного артрита и аутоиммунных гепатобилиарных заболеваний.
Дифференциальный диагноз при БШ проводят с ревматоидным артритом, системной красной волчанкой, аутоиммунными заболеваниями печени и желчных путей в сочетании с синдромом Шегрена. Несмотря на длительное существование артралгии для БШ в отличие от ревматоидного артрита, нехарактерно наличие стойкого артрита и деформаций суставов; на рентгенограммах не обнаруживаются признаки эрозивного поражения суставов; артрит при БШ обычно полностью исчезает на 2-3-й день после назначения небольших доз кортикостероидов. Для системной красной волчанки характерны эритематозные высыпания на лице в виде “бабочки”, эндокардит, экссудативный серозит, нефротический синдром, наличие в крови ЛЕ-клеток и др. При хроническом активном гепатите, билиарном циррозе печени в отличие от БШ нарушения функциональных проб печени являются постоянным признаком, в крови обнаруживаются маркеры вируса гепатита В; в материале, полученном при биопсии печени, выявляются присущие этим заболеваниям морфологические изменения.
Отдельные симптомы, имеющие место при БШ, могут наблюдаться при различных других заболеваниях. Так, увеличение слюнных желез отмечается при опухолях желез, болезни Микулича, злокачественных лимфомах, саркоидозе, туберкулезе, актиномикозе, остром бактериальном и вирусном сиалоадените, хроническом паренхиматозном паротите, сиалодохите, гиперлипидемии и сахарном диабете, а также при нейроэндокринных заболеваниях (дисфункции половых и щитовидных желез). Использование критериев для диагностики БШ, отсутствие при этих состояниях признаков аутоиммунного заболевания, а также проведение биопсии малых слюнных желез нижней губы позволяют исключить БШ у большинства больных с названными состояниями.
Основное место в лечении БШ принадлежит кортикостероидам и цитостатическим иммунодепрессантам (хлорбутин, циклофосфамид).
В начальной стадии заболевания при отсутствии признаков системных проявлений и умеренных нарушениях лабораторных показателей целесообразно длительное лечение преднизолоном в малых дозах (5–10 мг/день). В выраженной и поздней стадиях заболевания при отсутствии признаков системных проявлений необходимо назначение преднизолона (5–10 мг/день) и хлорбутина (2–4 мг/день) с последующим длительным, в течение нескольких лет, приемом поддерживающих доз преднизолона (5 мг/день) и хлорбутина (6–14 мг/нед). Такая схема может быть использована для лечения больных в начальных стадиях заболевания при наличии выраженных нарушений лабораторных показателей активности процесса, а также криоглобулинемии без четких признаков системных проявлений.
При наличии системных проявлений, независимо от стадии заболевания, гормональные и цитотоксические препараты используются в значительно более высоких дозах с учетом тяжести системных проявлений.
Пульс-терапия высокими дозами преднизолона и циклофосфана (1000 мг 6-метилпреднизолона внутривенно ежедневно в течение трех дней подряд и однократное внутривенное введение 1000 мг циклофосфана) с последующим переводом на умеренные дозы преднизолона (30–40 мг/день) и цитостатиков (хлорбутин 4-6 мг/день или циклофосфамид 200 мг внутримышечно 1–2 раза в неделю) при отсутствии гепатотоксического воздействия является наиболее эффективным методом лечения больных с тяжелыми системными проявлениями БШ, как правило, хорошо переносится больными и позволяет избежать многих осложнений, связанных с длительным приемом высоких доз преднизолона и цитостатиков. Экстракорпоральные методы лечения (гемосорбция, криоадсорбция, плазмаферез, двойная фильтрация плазмы) в комбинации с пульс-терапией наиболее эффективны при лечении больных БШ с язвенно-некротическим васкулитом, гломерулонефритом, полиневритом, миелополирадикулоневритом, цереброваскулитом, обусловленными криоглобулинемией.
Опыт предыдущих исследований свидетельствует о необходимости использования программных, т.е. проводящихся на протяжении длительного периода времени, методик экстракорпоральной терапии, особенно у больных БШ с моноклональной криоглобулинемией. По достижении выраженного клинического эффекта (улучшение общего состояния, регресс полисерозита, нефрита, полиневрита, васкулита и т.д.) и снижения лабораторных показателей активности процесса больных постепенно переводят на поддерживающие дозы глюкокортикостероидов и цитостатиков.
Параллельно проводят симптоматическую терапию офтальмологических, стоматологических, гастроэнтерологических и других проявлений заболевания.
Местная терапия при сухом кератоконъюнктивите направлена на преодоление гиполакримии, предотвращение вторичной инфекции, ускорение процессов регенерации эпителия конъюнктивы и роговицы. Гиполакримия является показанием к назначению искусственных слез. Они восполняют дефицит водного слоя прекорнеальной слезной пленки и удерживают ее в стабильном положении. Частота применения препаратов зависит от тяжести поражения органа зрения и колеблется от 3 до 10 раз в сутки. Во многих составах искусственных слез в качестве полимерного ингредиента используются эфиры целлюлозы: гидроксилпропилцеллюлоза – lacrisert, lacril, tiarisol, гидроксилцеллюлоза – cle rz, lyteers, гидроксиметилцеллюлоза – лакрисин, лакрисифи. Широко используются другие гидрофильные полимеры: поливиниловый спирт – ligufilm, поливинилпирролидон. С целью сохранения остаточной слезной секреции применяются различные способы блокирования слезных путей: прижигание, введение желатина или клейких тканей (N-бутилцианокрил) непосредственно в слезные канальцы, а также силиконовые пробки (punctum plug) для перманентной тампонады слезной точки и создания физиологического блока.
С целью защиты роговицы применяются лечебные мягкие контактные линзы. Для профилактики вторичной инфекции используют растворы фурацилина (в разведении 1:5000), 0,25% раствор левомицетина, ципрофлоксацина и др. Уменьшению вязкости прекорнеального слоя способствует применение трипсина, хемотрипсина (2 мг на 10 мл изотонического раствора натрия хлорида), фибринолизина и лекозима. С целью воздействия на регенерацию эпителия роговицы и конъюнктивы инстиллируют цитраль с рибофлавином, закладывают на ночь 0,5% тиаминовую, 10% метилурациловую, солкосериловую мази.
Терапия хронического сиалоаденита направлена на преодоление гипосаливации, укрепление стенок протоков слюнных желез, профилактику обострений сиалоаденита, улучшение регенерации эпителия слизистой оболочки полости рта и борьбу со вторичной инфекцией. С целью нормализации трофики и секреции слюнных желез используют новокаиновые блокады. В случаях обострения хронического паротита (и для профилактики его рецидивов) применяют аппликации 10–30% раствора димексида. В случаях развития гнойного паротита в протоки слюнных желез вводят антибиотики и местно назначают противогрибковые препараты (нистатин, леворин, нистатиновую мазь). Для уменьшения проницаемости протоков внутривенно или внутримышечно вводят препараты кальция.
Ускорить эпителизацию слизистой оболочки полости рта и красной каймы губ при возникновении эрозий и трещин удается с помощью масел шиповника и облепихи, солкосериловой и метилурациловой мазей, а также путем обработки слизистой оболочки рта препаратом ЭНКАД (активные дериваты нуклеиновых кислот). Антибактериальными свойствами обладает также декаминовая карамель. При сухости слизистой оболочки носа применяют частые аппликации изотонического раствора натрия хлорида (с помощью турунд). Сухость влагалища уменьшается при использовании калиево-йодистого желе. При сухости трахеи и бронхов рекомендуется длительный прием бромгексина (8–16 мг 3 раза в сутки в течение 2–3 мес). При наличии симптомов хронического гастрита с секреторной недостаточностью в течение длительного времени проводят заместительную терапию (соляная кислота, натуральный желудочный сок, пепсидил). Недостаточность панкреатической секреции требует приема ферментов: панзинорма, креона, фестала курсами по 2–3 мес или постоянно, проводится также лечение солкосерилом (по 2 мл внутримышечно 2 раза в день в течение 15–30 дней).
Прогноз для жизни благоприятный. При своевременно начатом лечении удается замедлить прогрессирование заболевания, восстановить трудоспособность больных. При позднем начале лечения обычно быстро развиваются тяжелые офтальмологические, стоматологические, а также системные проявления заболевания, происходит инвалидизация больного. У больного БШ с моноклональной криоглобулинемией и в случаях развития злокачественных лимфопролиферативных заболеваний прогноз менее благоприятный.
Профилактика направлена на предупреждение обострений и прогрессирования заболевания. Она предусматривает раннюю диагностику и своевременное начало адекватной терапии. Некоторые больные нуждаются в ограничении физических нагрузок и нагрузок на органы зрения, в исключении аллергизирующих воздействий. Больным противопоказана вакцинация, с большой осторожностью должны применяться тепловые процедуры. Необходимы санация рта и своевременное протезирование зубов.