Видео
ЛЕЧЕНИЕ БОЛИ. ОСТРАЯ И ХРОНИЧЕСКАЯ БОЛЬ
Еще фото
В статье описаны виды оценки и распознавания боли и способы ее лечения. In the article methods of pain estimation and recognition and ways of its treatment are described.
По классификации Международной Ассоциации по Изучению Боли (International Association for the Study of Pain (IASP), боль – неприятный чувствительный или эмоциональный опыт, ассоциированный с имеющейся или потенциальной травмой ткани.
Для правильного понимания принципов лечения боли необходимо не только знание особенностей физиологических процессов, анатомии нервной системы, фармакологии, принципов оценки болевого синдрома. На первый план должно выходить само признание наличия боли как проблемы у пациента ветеринарного врача, понимание актуальности адекватного обезболивания как необходимого компонента успешного лечения огромного количества болезней.
В медицинской практике существует специальный алгоритм RAT – Recognize Assessment Treatment – распознавание, оценка и лечение боли. Как и в любом алгоритме, соблюдение шагов является принципиальным моментом. Если мы пропустим первый шаг (распознавание) – мы не сможем начать лечение болевого синдрома, так как не будем знать о его наличии. Если мы не будем оценивать боль (ее тип, интенсивность), то мы не сможем назначить правильные методы лечения и оценить динамику коррекции болевого синдрома. В ветеринарной практике мы руководствуемся, в первую очередь, рекомендациями WSAVA Pain Management guidelines.
В данной статье мы рассмотрим методы, которыми мы можем распознавать боль, принципы оценки типа болевого синдрома, тактики лечения разных типов болевых синдромов.
Этот этап является одним из самых сложных в работе ветеринарного врача. Во-первых, не все врачи признают саму вероятность наличия болевых синдромов у животных. Во-вторых, для распознавания боли необходимо проводить ряд тестов во время осмотра пациента, которые не всегда могут дать очевидную информацию. Наши пациенты не могут точно сказать, в каком месте у них есть боль. Часто пациенты небольшого размера, и точно определить локализацию боли при пальпации может быть очень сложно. Иногда боль излишне проявляется у пациентов с нестабильным эмоциональным фоном.
Для успешного распознавания наличия боли мы можем использовать хорошо исследованные методики.
В руководстве WSAVA Pain Management guidelines представлены таблицы по патологиям с предполагаемой тяжестью течения болевого синдрома. Это очень удобные таблицы для того, чтобы можно было быстро сориентироваться и о вероятности боли у пациента с конкретной патологией или, например, после планируемой операции. Такое понимание позволит быстро определиться, потребуется ли пациенту активная анальгезия в послеоперационный период, насколько длительная может потребоваться госпитализация по поводу болевого синдрома, нужна ли мультимодальная анальгезия. Представленные патологии разделены по тяжести болевого синдрома, начиная с умеренной боли и заканчивая тяжелой-изматывающей болью.
нетяжелые травмы мягких тканей
диагностическая артроскопия и лапароскопия
Средняя тяжелая боль
капсулярная боль из-за органомегалии
растяжение половых органов
травматическая диафрагмальная грыжа
травма (ортопедия, голова, обширные травым мягких тканей)
обструкция мочеточника, холедоха
заворот брыжейки, желудка, семенного канатика
рак ротовой полости
обширная резекционная или реконструктивная хирургия (остеотомия, открытая артротомия, хирургия ПКС)
Также для выявления болевого синдрома можно использовать специальные тестовые системы – шкалы оценки боли. Работа с такими шкалами в медицине очень хорошо организована, потому что возможна объективная оценка тяжести боли непосредственно от больного. В ветеринарной практике мы сталкиваемся с проблемой невозможности объективной оценки боли. Поэтому должны пользоваться максимально расширенными шкалами, таким образом увеличивая их чувствительность.
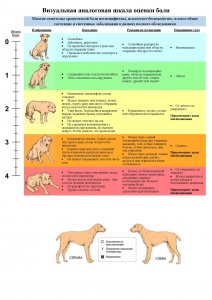
Наиболее удобной для практического использования является Визуальная аналоговая шкала боли, разработанная для собак и кошек. С помощью этой шкалы можно оценивать тяжесть болевого синдрома по бальной оценке от 0 до 4 с помощью: 1) визуального совпадения; 2) описания поведенческих изменений; 3) описания данных осмотра (преимущественно, с помощью пальпации).
Тяжелая изматывающая боль
синтез обширных переломов с обширной травмой мягких тканей
переломы суставов или патологические переломы
некротизирующий панкреатит или холецистит
нейропатическая боль (в том числе ГМПД)
воспалительные заболевания (перитонит, целлюлит, пиодерма глубокая)
Идея работы с такой шкалой следующая: при первичной оценке болевого синдрома регистрируется балл боли (например, 4). Исходя из чего пациенту назначается анальгезирующая терапия. Далее происходит переоценка боли по шкале, в зависимости от тяжести проявления болевого синдрома, через 1–4 ч. В случае если при новой оценке балл остается таким же, разумно расширить анальгезирующую терапию, увеличить дозировки препаратов, рассмотреть немедикаментозные методы обезболивания. Если при новой оценке балл снижается до удовлетворительного (0–1), то можно признать анальгезию успешной и продолжить ее в прежнем темпе еще какое-то время, исходя из логики болезни у данного пациента. Также важным пунктом работы со шкалой оценки боли является обязательная оценка одним оператором максимально долгое время, это снижает риск увеличения субъективности оценки.
Все эти таблицы и шкалы подходят для оценки острой боли в условиях клиники и должны проводиться обученным персоналом (врачом, технишеном или ассистентом).
Оценка хронического болевого синдрома является намного более сложным процессом. Огромное количество проявлений хронической боли у людей описано именно ощущениями – например, подергивания в пальцах, или похолодание кончика носа, давящая круговая боль в голове. Понятно, что оценить подобные проявления у животных мы не можем. Для оценки течения хронической боли у животных необходимо: 1) определить саму вероятность наличия хронической боли. Для этого нужно помнить о патологиях и болезнях, которые сопровождаются хронической болью или могут приводить к ее появлению; 2) использовать для оценки болевого синдрома тесный контакт с владельцем. Для некоторых заболеваний есть разработанные шкалы по оценке хронической боли. Например, самое большое количество исследований на данный момент касаются остеоартроза собак. Для контроля боли у этих пациентов используют дневники для домашнего заполнения владельцем или персоналом, который постоянно занимается с конкретным пациентом. При посещении врача владелец представляет подобный краткий дневник, на основании которого можно сделать вывод об эффективности выбранной терапии.
Существуют разработанные шкалы оценки качества жизни у онкологического больного, но они пока не находятся в свободном доступе для работы.
Для наблюдения в домашних условиях за пациентом, который получает обезболивающую терапию, можно давать рекомендации для владельцев о поведенческих изменениях, согласно руководству WSAVA Pain Management guidelines. Для кошек важно оценивать общую мобильность (легкость движения, плавность), наличие активности и деятельности (игры, охота, прыжки, использование инвентаря), способность есть и пить, наличие ухода за собой (когтеточка, вылизывание), способность к расслаблению, отдыху, осуществление социальных мероприятий с участием людей и других домашних животных, изменения темперамента (обычно в худшую сторону). Для собак несколько иные рекомендации. Важно оценивать активность и мобильность (энергичность в движениях, счастье при движении, игривость, легкость в перемене позы, переносимость движений и упражнений), настроение и поведение (настороженность, беспокойство, грусть, игривость), определять уровень контроля стресса (вокализация, депрессия, реакция на других собак и людей). Также у собаки могут быть и видимые признаки боли – наличие хромоты, снижение уровня комфорта, например, при перемене позы.
Заболевания, сопровождающиеся хронической болью у собак и кошек
Остеосаркома, хондросаркома, злокачественные новообразования оболочек периферических нервов
Хронические воспалительные заболевания
Хронический отит, хронический панкреатит, цистит кошек
Хронические ортопедические заболевания
Остеоартрит, пояснично-крестцовая нестабильность
Хронические повреждения мягких тканей
Скальпированная рана, индуцированная ионизирующим излучением боль
Повреждение нервных тканей
Боль после ампутации, после торакотомии, болезнь межпозвоночных дисков
Оценка типа боли: острая и хроническая
Острая боль – это болевой синдром, который развивается в ответ на острое повреждение тканей и несет, в первую очередь, защитную и адаптивную эволюционную функцию. Например, если человек схватит горячую сковородку, то в силу формирования острого болевого синдрома, он: 1) отбросит сковородку и таки образом осуществит защитную функцию; 2) передаст информацию своим потомкам и обществу для осуществления адаптивной функции. С другой стороны, если этот ожог не будут лечить правильно, будет развиваться глубокий некроз кожи и подлежащих тканей, разовьется травма нервных окончаний в этой области, импульсы по нервным волокнам будут проходить неправильно, разовьется изменение функции и структуры нервной ткани на местном уровне – у этого человека разовьется хроническая боль.
Таким образом, острый болевой синдром мы определяем как быстро развившийся процесс с острыми симптомами в ответ на прямое повреждение (механическое, термическое, химическое). А хронический болевой синдром – это процесс длительный по времени и связанный с вторичным повреждением ткани и нервных окончаний. Еще важное различие заключается в локализации боли. При острой боли мы можем локализовать точно источник боли (например, перелом конечности). При хронической боли точная локализация невозможна (например, при заболевании межпозвоночных дисков мы можем только примерно определить боль в шее или пояснице, но не в конкретном позвонке). При остром болевом синдроме боль прекращается вместе с заживлением и устранением причины. В то время как при хронической боли причину чаще всего устранить невозможно.
Во многих случаях мы можем избежать формирования хронического болевого синдрома при условии удачного контроля боли в острый период. По данным некоторых исследований в медицине, значительное число постоперационных больных испытывают хроническую боль:
– торакотомия более 67%;
– ампутация более 90%.
Тяжелая острая боль является предиктором хронической боли.
Безусловно, возможна и другая ситуация, когда на фоне хронической боли развивается острый болевой синдром. Такие ситуации наиболее сложны для лечения, потому что симптоматически мы видим именно острые проявления, а для лечения будут требоваться в том числе препараты, которые влияют на течение хронической боли. Как основной пример такого типа комбинированного болевого синдрома можно привести тяжелую абдоминальную боль при обострении хронического панкреатита.
Хроническая боль, в свою очередь, может быть охарактеризована как воспалительная (из-за длительного влияния воспалительных компонентов при травме ткани или воспалении на нервные окончания – например, боль при панкреатите) и нейропатическая (боли, которые возникают непосредственно при травме нервной системы – опухоли головного мозга, заболевания межпозвоночных дисков, перерезание крупных нервов при операциях и т.д.). Заподозрить хроническую боль можно у пациентов, у которых есть длительные воспалительные заболевания или заболевания центральной нервной системы. Или если пациент проявляет навязчивые разлизывания, расчесы, неадекватно реагирует на минимальные болевые манипуляции или вовсе на простые прикосновения (проявления гиперальгезии и аллодинии). Также при плохом ответе пациента на лечение НПВС и опиоидами стоит заподозрить наличие хронической боли. Подход к лечению разных типов хронической боли также должен быть разным.
Для лучшего понимания самих процессов развития боли и принципов мультимодальной анальгезии необходимо знание основ формирования болевого сигнала в организме.
На данный момент в мире признана теория формирования ноцицептивной дуги, которая подразделяется на несколько этапов.
Непосредственно в синапсах задних рогов спинного мозга наибольшее значение для формирования острого болевого синдрома имеют некоторые рецепторы и медиаторы возбуждения – NMDA-рецепторы, AMPA-рецепторы, калиевые каналы, глутамат. При формировании патологических изменений в синапсе большую роль играет большое количество глутамата (из-за непрекращающегося возбуждения нервных волокон из зоны повреждения ткани), NMDA-рецепторы, магниевые каналы, протеин С, оксид азота, кальций в межсинаптической щели, субстанция Р. В случае длительного влияния на синапс и постоянного выброса большого количества глутамата в синаптическую щель, магниевый канал NMDA-рецептора оказывается постоянно открытым, и через него приникает большое количество кальция из синаптической щели. Этот кальций, влияя на протеин С, вызывает формирование большого количества оксида азота, который, в свою очередь: 1) закрывает калиевые каналы (через которые осуществляют свою работу опиоидные анальгетики, поэтому при лечении хронической боли они неэффективны; 2) высвобождают большое количество субстанции Р, которая взаимодействует с генной структурой синапса, вызывая его морфологические безвозвратные изменения. Таким образом, хронический болевой синдром является проявлением морфологической, патологически измененной структуры нервной ткани и, по сути, отдельной болезнью.
Принцип мультимодальной анальгезии состоит в том, чтобы для обезболивания применять техники и препараты, которые позволяют прервать ноцицептивную дугу на 2 и более этапах, или которые действуют на одном этапе, но на 2 или более различных рецепторов.
Лечение острой боли
Так как мы знаем, что острая боль – это всегда быстрый ответ на прямое повреждение, то основной принцип лечения – использование мультимодальности и устранение повреждения. Для купирования острого болевого синдрома можно использовать различные препараты и техники.
В лечении острой боли важно придерживаться принципа максимальной анальгезии для того, чтобы не допустить страдания пациента, улучшить его функциональность, предотвратить развитие хронического болевого синдрома. Поэтому при купировании острой боли важно максимально обезболить пациента в первые 12–24 ч и лишь после этого снижать интенсивность анальгезии, используя шкалы оценки тяжести болевого синдрома.
Метод, основанный на введении в эпидуральное пространство анестетиков местного действия (или комбинации анестетиков) для формирования блока выше или на уровне повреждения ткани. Этот метод можно применять как для купирования боли во время операции (когда боль связана с острым хирургическим повреждением ткани), так и в лечении пациентов с различными патологиями в рамках стационарного лечения. Например, при переломах конечностей или таза, тяжелых травм мягких тканей с области промежности или тазовых конечностей, при острой боли со стороны органов малого таза или брюшной полости, при тяжело протекающих перитонитах любой этиологии. Для применения можно использовать периодическое введение с помощью пункции в эпидуральное пространство или с помощью установки эпидурального катетера.
В качестве дополнительных обезболивающих техник можно использовать фиксации (например, бинтование при травме грудной клетки, фиксации хирургические – вывихов суставов или переломов конечностей), применение термотерапии (например, массаж кубиками замороженного хлоргексидина 1% областей с отеками или послеоперационных областей).
Препараты для лечения острой боли относятся к разным фармакологическим группам: диссоциативные анестетики (Тилетамин, Кетамин), альфа-агонисты (медетомидин, дексмедетомидин), нестероидные противовоспалительные средства, миорелаксанты, центральные неопиоидные анальгетики, опиоидные препараты (доступны в ветеринарной практике при наличии лицензии).
Тилетамин+золазепам – комбинированный препарат, который состоит из тилетамина (обеспечивает анальгезию) и золазепама (обеспечивает седацию). С точки зрения прерывания дуги боли, препарат действует на уровне перцепции в головном мозге. У собак период полувыведения золазепама меньше, чем тилетамина, поэтому при пробуждении у собак наблюдают иногда тонические судороги, вокализацию, беспокойство. У кошек период полувыведения золазепама больше, чем тилетамина, поэтому часто кошки пробуждаются очень долго. Этот препарат можно использовать в практике интенсивной терапии при купировании острой боли в монорежиме при умеренной-средней боли (например, при острой задержке мочи, при плеврите для торакоцентеза, при коротких хирургических обработках ран и т.д.). Или в составе мультимодальной анальгезии при тяжелой-изматывающей боли (после торакотомии, при лечении тяжелого панкреатита или энтерита, после объемных удалений мягких тканей, при тяжелой травме). Также большую помощь этот препарат дает в первичной диагностике пациента с травмой, когда можно достигнуть одновременно и уменьшения боли, и умеренной седации, достаточной для проведения быстрых диагностических тестов (УЗИ, рентген, центезы). Дозировки для болюсного введения – 0,5–2мг/кг внутримышечно или внутривенно. Для инфузии с постоянной скоростью можно использовать дозы 0,5–1 мг/кг/ч, но стоит помнить об особенностях метаболизма препарата у разных видов животных.
Медетомидин и дексмедетомидин имеют весьма широкое применение для лечения болевого синдрома в острый период. Эти препараты рекомендованы для использования в ИПС (инфузия с постоянной скоростью) у пациентов с тяжелой-изматывающей болью в составе мультимодальной схемы анальгезии. В таком случае область их действия с точки зрения прерывания дуги боли – перцепция и модуляция. Также их можно использовать для введения в эпидуральное пространство, в таком случае они будут действовать на уровне трансмиссии. Оба они могут обладать седативным эффектом, могут оказывать влияние на артериальное давление, поэтому мониторинг пациента, получающего такое лечение в виде ИПС, должен быть расширен. Дексмедетомидин в меньшей степени влияет на сознание и гемодинамику, поэтому является более безопасным и перспективным для использования в клинической практике. Для ИПС можно использовать дозы: медетомидин 0,5–2 мкг/кг/ч, дексмедетомидин 0,25–1 мкг/кг/ч.
Нестероидные противовоспалительные средства обладают анальгезирующим эффектом за счет влияния на формирование воспаления (блокируя циклооксигеназу и действуя на другие воспалительные медиаторы) в области повреждения и реализуют свое действие на уровне трансдукции. Область применения весьма широкая, но в монорежиме могут применяться только при умеренной-средней боли (например, цистит или простой перелом после остеосинтеза). Также используют их в составе мультимодальной анальгезии при более выраженных болевых синдромах. В силу вероятных побочных действий (развитие эрозий или язв в кишечнике и желудке, развитие острой почечной недостаточности, влияние на свертывающую систему крови) их применение возможно только у гемодинамически стабильных пациентов с нормальной температурой тела и только в рекомендованных дозировках и с соблюдением рекомендованной кратности. У пациентов в шоке, со свежей политравмой, дегидратацией применение этих препаратов ограниченно. Ниже приведена таблица с рекомендованными WSAVA препаратами, дозами и кратностью применения.
Поражение органов пищеварения у пациентов, принимающих нестероидные противовоспалительные препараты: факторы риска, тактика ведения
Представлена сравнительная характеристика нестероидных противоспалительных препаратов (НПВП). Рассмотрены применение НПВП в клинической практике, побочные эффекты их применения, методы диагностики поражения верхних отделов желудочно-кишечного тракта и так
The comparative characteristic of non-steroid anti-flammation preparations (NPVP) are presented. The application of NPVP in the clinical practice, side effects of their application, methods of the upper divisions of gastrointestinal tract affection diagnostics and tactics of conducting patients, taking NPVP are examined.
Благодаря широкому спектру показаний нестероидные противовоспалительные препараты (НПВП) стали популярным классом лекарственных средств и на сегодняшний день являются лидерами по продажам в аптечной сети.
По данным проведенного в Европе опроса НПВП назначают 82% врачей общей практики и 84% ревматологов. В России в 2007 г. было продано 105,8 млн упаковок НПВП [1]. Самостоятельное потребление НПВП пациентами в 7 раз превышает объем врачебных назначений [1]. С учетом масштаба применения НПВП, вопросы их эффективного использования и безопасности данной терапии чрезвычайно актуальны.
Сравнительная характеристика нестероидных противоспалительных препаратов
Класс НПВП представлен примерно 20 различными по химической структуре препаратами: производными салициловой, индоловой, гетероарилуксусной, энолиоковой и других кислот, имеющими общие фармакологические эффекты. Основной механизм фармакологического действия всех НПВП заключается в блокаде фермента циклооксигеназы (ЦОГ), регулирующего биотрансформацию арахидоновой кислоты в простагландины (ПГ), простациклин (ПГI2) и тромбоксан А2 (ТхА2). Ингибиция ЦОГ-2 рассматривается как один из важных механизмов противоспалительной и анальгетической активности данного класса препаратов (рис.).
Применение НПВП в клинической практике
В клинической практике НПВП применяются в ряде ситуаций [1–3].
1. Ургентное обезболивание и купирование лихорадки при:
2. Комплексное анестезиологическое пособие.
3. Купирование боли при заболеваниях опорно-двигательной системы.
Перспективно использования НПВП в практике онкологов. Эффективность НПВП в профилактике развития и рецидивов злокачественных новообразований желудочно-кишечного тракта (ЖКТ) хорошо обоснована теоретически и подтверждена данными эпидемиологических и когортных наблюдательных исследований. Длительное применение НПВП (сулиндак, целекоксиб) позволяет снизить темпы прогрессирования заболевания при семейном аденоматозном полипозе и уменьшить риск рецидивов спорадических аденоматозных полипов толстой кишки. НПВП являются эффективным средством для купирования хронической боли у онкологических больных. Имеются данные, свидетельствующие об эффективности НПВП в качестве дополнительного компонента традиционной химиотерапии.
Побочные эффекты применения НПВП
Терапевтические эффекты, обусловленные ингибированием различного типа ЦОГ (табл. 1), сопряжены с развитием ряда побочных эффектов.
Подавление активности ЦОГ-1 ассоциируется с высокой частотой поражения ЖКТ. Подавление ЦОГ-2-зависимого синтеза ПГ I2-клетками сосудистого эндотелия при отсутствии влияния на контролируемый ЦОГ-1 синтез ТхА2-тромбоцитами на фоне применения селективных НПВП обусловливает высокий риск развития тромбоэмболических осложнений. Помимо этого регистрируются и другие класс-специфические побочные эффекты (табл. 2).
Патология органов пищеварения, ассоциированная с приемом НПВП
Прием НПВП, в первую очередь неселективных в отношении ЦОГ-1, ассоциируется с широким спектром поражения органов пищеварения, от функциональных нарушений до тяжелой органической патологии, способной привести к летальному исходу. Прием селективных НПВП, напротив, сопряжен с высоким риском тромбоэмболических осложнений. Возможно поражение любого отдела ЖКТ — от полости рта до прямой кишки. Различные желудочно-кишечные симптомы (изжога, тошнота, рвота, тяжесть в эпигастрии, гастралгии) испытывают от 10% до 40% больных, при эзофагогастродуоденоскопии (ЭГДС) гастропатии (эрозии, язвы) регистрируется у 15–30% обследованных, тяжелые осложнения в виде прободений, перфораций, кровотечений — у 0,5–3%, поражение тонкой, толстой кишки, печени отмечается у 1–5% пациентов, принимающих НПВП.
Особенностью НПВП-ассоциированных язв являются следующие характеристики:
Риск желудочно-кишечных кровотечений становится максимальным при приеме большинства НПВП к 84-му дню лечения, а для индометацина — в течение первых 7 дней (T. Lee, 2007).
Негативное влияние на ЖКТ не ограничивается только верхними отделами. В последние годы все большее внимание уделяется проблеме лекарственного поражения тонкой кишки, прежде всего т. н. НПВП-энтеропатии. Эта патология характеризуется нарушением проницаемости кишечной стенки с экссудацией белка и диапедезом эритроцитов, приводящей к железодефицитной анемии и гипоальбуминемии, а также повреждению слизистой оболочки с развитием эрозий, язв и их осложнений — кровотечения и перфорации, появлением циркулярных стриктур и нарушением проходимости ЖКТ.
Бессимптомное повышение трансаминаз отмечается у 1–5% больных, регулярно принимающих НПВП, серьезные гепатотоксические реакции отмечаются в 1 случае на 10 000 больных, регулярно принимающих НПВП (U. Boelsterli и соавт., 2002; A. Walker, 1997). Патогенез этой патологии неизвестен. Определенную роль могут играть: поражение митохондрий гепатоцитов, как результат блокады ферментных систем цикла Кребса и разобщения окислительного фосфорилирования, блокада фосфодиэстеразы, нарушение экскреции желчи вследствие образования комплексов с желчными кислотами и энтерогепатической рециркуляции НПВП, иммуногенетические нарушения и др. Поражение печени — редкая, но потенциально угрожающая жизни патология, связанная с приемом НПВП, имеющая характер метаболической или иммунологической идиосинкразии.
Методы лабораторной и инструментальной диагностики патологии ЖКТ
Основными методами диагностики поражения верхних отделов желудочно-кишечного тракта является ЭГДС, которую в группах риска необходимо провести в первый месяц от начала лечения. Вспомогательное значение может иметь исследование кала на скрытую кровь чувствительным методом.
Проведение диагностических мероприятий для выявления патологии тонкой кишки показано больным, регулярно принимающим НПВП, в случае наличия у них клинических симптомов (диарея, метеоризм, абдоминальная боль), признаков кишечного кровотечения или железодефицитной анемии, гипоальбуминемии. Для диагностики поражения слизистой тонкой кишки используют эндоскопические методы, позволяющие визуализировать тощую и подвздошную кишку — энтероскопию, для диагностики стриктур — энтерографию с контрастным веществом, для диагностики воспаления — кал на кальпротектин. Обязательным является исследование кала на скрытую кровь высокочувствительными методами (иммунохимический метод или тест на трансферрин и гемоглобин в кале).
С целью диагностики гетатотоксических реакций необходим мониторинг биохимических показателей печени (табл. 3).
Тактика ведения пациентов, получающих НПВП
При ведении пациентов, получающих НПВП, необходимо:
При наличии факторов риска необходимо проведение соответствующей профилактики. При риске ЖКТ-осложнений назначаются ингибиторы протонной помпы, при кардиоваскулярном риске — низкие дозы ацетилсалициловой кислоты.
Динамическое наблюдение за пациентами с различной степенью риска гастропатий [1]
1. Степень риска гастропатий отсутствует.
Если факторов риска нет, но длительность приема НПВП составляет более 4 недель, следует назначить селективные НПВП + ингибиторы протонной помпы (ИПП).
Контроль за нежелательными эффектами. Необходимые исследования: общий анализ крови (ОАК), определение уровней АЛТ, АСТ, креатинина; контроль артериального давления (АД) — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах; оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите. При появлении признаков патологии ЖКТ необходимо провести эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь чувствительным методом, кал на кальпротектин.
Лечебная тактика. Возможно назначение неселективных НПВП: ацеклофенак, диклофенак, ибупрофен, кетопрофен (2-я линия: индометацин, пироксикам, напроксен) или могут быть назначены селективные НПВП.
В группах риска применение ИПП должно продолжаться на протяжении всего курса лечения НПВП или низкими дозами Аспирина.
2. Риск умеренный.
Имеется 1 фактор риска (пожилой возраст без дополнительных факторов риска (нет тяжелой сопутствующей патологии), или прием кортикостероидов, или курение и прием алкоголя, или инфицированность Н. рylori, или диспепсия в анамнезе).
Контроль за нежелательными эффектами. Необходимые исследования: ОАК, определение уровней АЛТ, АСТ, креатинина; контроль АД — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах; оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите, при появлении признаков патологии ЖКТ необходимо эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь чувствительным методом, кал на кальпротектин; дополнительно ЭГДС через 1 месяц после начала приема НПВП, при появлении признаков НПВП-гастропатий определить наличие Н. рylori любым методом в соответствии со стандартами, общий анализ крови 1 раз в месяц.
Лечебная тактика. Может назначаться любой селективный НПВП или неселективный НПВП + ИПП (следует стремиться к назначению НПВП в малых дозах, коротким курсом).
3. Риск высокий.
Имеется 1 фактор риска (язвенный анамнез, или прием Аспирина, или тяжелая сопутствующая патология).
Контроль за нежелательными эффектами. Необходимые исследования: ОАК, определение уровней АЛТ, АСТ, креатинина; контроль АД — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах, оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите, при появлении признаков патологии ЖКТ — эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь чувствительным методом, кал на кальпротектин; дополнительно: ЭГДС через 1 месяц после начала приема НПВП, при появлении признаков НПВП-гастропатий определить наличие Н. рylori любым методом в соответствии со стандартами, общий анализ крови 1 раз в месяц.
Лечебная тактика. Назначить по выбору: селективный НПВП + ИПП (стремиться к назначению в малых дозах, коротким курсом).
4. Риск очень высокий.
У пациента есть язвы, осложненные кровотечением или перфорацией в анамнезе, или часто рецидивирующие язвы, или комбинация двух факторов риска и более.
Контроль за нежелательными эффектами. Необходимые исследования: ОАК, определение уровней АЛТ, АСТ, креатинина; контроль АД — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах, оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите. При появлении признаков патологии ЖКТ необходимо эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь, кал на кальпротектин; дополнительно: ЭГДС через 1 месяц после начала приема НПВП, при появлении признаков НПВП-гастропатий определить наличие Н. рylori любым методом в соответствии со стандартами, общий анализ крови 1 раз в месяц.
Лечебная тактика: назначить селективный НПВП + ИПП. У лиц с язвенным анамнезом и лиц, получающих препараты, влияющие на свертываемость крови, использование селективных НПВП без ИПП не является эффективным методом профилактики гастропатий и осложнений. В группах риска применение ИПП должно продолжаться на протяжении всего курса лечения НПВП или низкими дозами Аспирина.
При сочетании ЖКТ-факторов риска и кардиоваскулярных осложнений следует назначить селективный НПВП + ацетилсалициловую кислоту + ИПП.
Тактика ведения пациентов с различным сердечно-сосудистым риском в настоящей статье не рассматривается.
При приеме нимесулида контроль показателей, отражающих состояние печени (АЛТ, АСТ, щелочной фосфатазы), необходимо осуществлять 1 раз в месяц.
Лечение язв, ассоциированных с приемом НПВП [1, 4]
Прекращение приема НПВП само по себе не приводит к рубцеванию язв, но может повышать эффективность противоязвенной терапии.
Ингибиторы протонной помпы (40 мг в сутки омепразола (Омез®), или рабепразола, или 60 мг лансопразола) являются основным средством лечения гастродуоденальных язв и эрозий, превосходящими по лечебному действию Н2-гистаминоблокаторы и мизопростол (уровень доказательности рекомендаций А). Длительность курсовой терапии при локализации небольших язв в двенадцатиперстной кишке должна быть не менее 4–6 недель, а при больших размерах и локализации язв в желудке — 8–12 недель. Эффективность противоязвенной терапии может быть повышена комбинацией ИПП с препаратами висмута (уровень доказательности рекомендаций С).
С профилактической целью в группах риска используются ИПП (20 мг в сутки омепразола (Омез®) или рабепразола или 30 мг лансопразола) на протяжении всего приема любых НПВП, включая низкие дозы Аспирина.
Лечение НПВП-энтеропатий
Подходы к медикаментозному лечению НПВП-энтеропатии не разработаны. Применение ИПП не уменьшает риск развития НПВП-энтеропатии. Использование селективных НПВП снижает риск развития или рецидива патологии тонкой кишки. По сравнению с неселективными НПВП селективные НПВП существенно безопаснее в плане развития НПВП-энтеропатии. По некоторым данным, прием сульфасалазина и коллоидного субцитрата висмута способствовал уменьшению кровопотери при приеме НПВП. Одновременное назначение НПВП и сульфасалазина в дозе 2 г/сутки редуцировало увеличенную проницаемость кишечного эпителия, индуцированную приемом индометацина (J. Hayllar, 1994). Дополнительное назначение метронидазола в дозе 400 мг 2 раза в сутки 7 дней способствовало редукции изменений кишечной проницаемости, вызванной приемом индометацина (G. Davies, 1993).
Особенности применения нимесулида
Один из наиболее популярных в России селективных НПВП — нимесулид (Найз®). Эффективность нимесулида подтверждена длительным периодом (более 20 лет) клинического использования. Немаловажно, что генерики нимесулида в нашей стране по цене доступнее других представителей группы селективных НПВП.
Продемонстрировано преимущество нимесулида перед другими НПВП по быстроте действия и выраженности анальгетического эффекта. Благодаря своим биохимическим особенностям, нимесулид легко попадает в область воспаления (в частности, в пораженные суставы при артрите), накапливаясь в большей концентрации, чем в плазме крови. Через 30 мин после перорального приема концентрация препарата в крови достигает
50% от пиковой и отмечается отчетливый обезболивающий эффект. Через 1–3 ч наступает пик концентрации препарата и, соответственно, развивается максимальное анальгетическое и противовоспалительное действие.
Молекула нимесулида в отличие от многих других представителей лекарственной группы НПВП имеет свойства основания. Это затрудняет ее проникновение в слизистую верхних отделов ЖКТ, тем самым уменьшая возможность контактного раздражения слизистой желудка и развития диспепсии. Нимесулид в целом лучше переносится, чем неселективные НПВП. На сегодняшний день отсутствуют данные метаанализа о безопасности нимесулида, как и ряда других селективных НПВП, в отношении серьезных осложнений со стороны ЖКТ [5].
Все НПВП, включая селективные, способны вызывать эндоскопическое поражение ЖКТ, развитие тяжелых ЖКТ-осложнений.
При наличии факторов риска, к которым относится пожилой возраст, наличие соматической патологии и др. использование только селективных НПВП недостаточно профилактики гастропатий и ЖКТ-осложнений. Назначение ингибиторов протонной помпы требуется на весь период лечения НПВП.
В каждом случае выбор нимесулида, как препарата для длительного применения, должен сопровождаться тщательным анализом факторов риска и последующим активным контролем нежелательных эффектов.
Противопоказанием для назначения являются: наличие эрозивно-язвенных изменений слизистой оболочки желудка и двенадцатиперстной кишки, активное кровотечение, воспалительные заболевания кишечника, нарушения свертывания крови, печеночная почечная недостаточность, активное заболевание печени или сопутствующее применение любых потенциально гепатотоксичных средств.
У лиц с язвенным анамнезом и лиц, получающих препараты, влияющие на свертываемость крови, использование нимесулида необходимо на фоне сопутствующего приема ИПП. Применение нимесулида у больных с хроническими заболеваниями сердечно-сосудистой системы, как и других НПВП, возможно только на фоне их эффективной медикаментозной коррекции. В силу обсуждаемой проблемы гепатотоксических осложнений, нимесулид, как и все НПВП, не следует назначать больным с хроническими заболеваниями печени, сопровождающимися нарушением функции, или лицам, имеющим в анамнезе лекарственные гепатотоксические реакции.
Таким образом, во всех клинических ситуациях, даже если планируется кратковременное применение препаратов в низких дозах, выбор НПВП должен осуществляться индивидуально, исходя из фармакологических особенностей препарата, клинической ситуации и наличия факторов риска появления нежелательных эффектов. Врач должен осуществлять контроль за нежелательными эффектами. Пациенту также должна быть предоставлена необходимая информация о возможных нежелательных эффектах и методах самоконтроля в процессе лечения.
Литература
* ГБОУ ВПО ОмГМА МЗ РФ, Омск
** ГБОУ ВПО НГМУ МЗ РФ, Новосибирск
.gif)
.gif)
_575.gif)
.gif)