Сит что это за обследование
Специфическая иммунотерапия является методом патогенетической терапии и его действие направлено на патогенетические звенья аллергического процесса. Высказывается мнение, что IgE, образующиеся в процессе иммунотерапии, не просто относятся к каким-либо подклассам или специфичны к аллергенам, а имеют антиидиотипическую направленность. Показано, что эти антитела относятся к классу G и могут оказывать как анафилактогенное (подобно аллергену связывая две молекулы IgE, и запуская выделение гистамина и других медиаторов), так и блокирующее антиаллергическое действие.
В настоящее время критерии СИТ связывают с показателями воздействия лечебных аллергенов на Т-клетки иммунной системы, которым отводится при аллергопатологиях главная роль в стимуляции синтеза IgE-антител и аллергическом воспалении. В этом случае при наличии эффективного лечения больного можно наблюдать:
— воздействие препарата на клеточную и медиаторную организацию аллергического воспаления и его снижение;
— торможение аллерген-специфической пролиферации Т-клеток;
— спонтанную экспрессию мРНК интерферона-у (ИФН-у), изменение спектра цитокинных маркеров, отражающих внутриклеточные процессы (12, 134).
Как указывают W. Wheeler et al, 1997, инъекции аллергенов сопровождаются изменением иммунных показателей. Во время первого курса может повышаться уровень IgE-антител, а в дальнейшем — постепенное падение его уровней. Однако, несмотря на подъем IgE в 1-й год лечения, пациенты отмечают хороший результат.
Отношение IgE/IgG является критическим параметром, который может быть показателем успешной терапии. В качестве возможного показателя в случае успешной СИТ отмечается снижение уровня IgE рецепторов на эозинофилах и других клетках-мишенях.
Установлено, что в том случае, когда у пациентов на аллерген зарегистрирована поздняя фаза реакции немедленного типа (LPR), лечение будет осуществляться (СИТ) более успешно, чем в тех случаях, когда отмечена только реакция волдырного типа на аллерген. Становится очевидным наличие клеточной инфильтрации в процессе LPR, в которой эозинофилы играют центральную роль мишени аллергической реакции.
В этом случае Тh1-вариант сопровождается образованием соответствующих цитокинов lL2, IFN-y. Преимущества метода обусловлены воздействием специфической терапии на все этапы аллергического ответа.
В связи с изученными механизмами СИТ можно отметить, что клинический эффект СИТ сопровождается рядом показателей, которые выявляются при соответствующем обследовании больного; происходит нормализация цитокинного профиля, реверсирование Т-клеток от Th2 > ТЫ к ТЫ > Th2, увеличены показатели «блок»-антител.
Переключение дифференцировки Т-хелперов с Th2 на Тh1. Последние секретируют гамма-интерферон, тормозящий синтез IgE В-лимфоцитами, уменьшение Тh2 приводит к снижению продукции воспалительных цитокинов (IL 3,4,5), что сопровождается снижением интенсивности воспаления.
Клиническое исследование эффективности СИТ при поллинозах оценивается по следующим показателям:
— длительность периода обострения поллиноза;
— интенсивность проявления симптомов заболевания (удушье, кашель, заложенность носа, слезотечение, зуд век и др.);
— потребность больного в медикаментах (антигистаминные местные, антигистаминные системные, Гкс местные и Гкс системные);
— состояние больного до цветения и в период цветения.
Таким образом, рассматривая различные аспекты применения метода аллергенспецифической иммунотерапии в практической аллергологии, можно отметить, что СИТ — единственный надежный способ противоаллергической защиты. Результаты многочисленных работ по использованию СИТ при лечении пыльцевой, инсектнои, «пылевой» аллергии показывают, что можно также сделать следующие выводы:
1. Аллерген-специфическая иммунотерапия направлена на патогенез аллергического заболевания.
2. СИТ — единственный метод противоаллергического лечения атопических заболеваний.
3. Противопоказаниями к назначению СИТ являются:
— период обострения аллергического заболевания;
— наличие необратимых изменений легочной формы ткани (энфиземы легких и др.);
— коллагенозы;
— злокачественные новообразования;
— беременность.
4. Терапевтический эффект СИТ проявляется:
— в полном отсутствии (или частичном уменьшении) симптомов аллергического заболевания, увеличении сроков ремиссии болезни, снижении потребности больного в антигистаминных препаратах, сохранении трудоспособности;
— в снижении чувствительности эффекторных тканей к специфическому аллергену, в нормализации цитокинного профиля, увеличении показателей специфических IgG-«блок»-антител.
— Вернуться в оглавление раздела «Пульмонология.»
Специфическая иммунотерапия атопических заболеваний
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Профессор Н.Г. Астафьева
Саратовский медицинский университет
А нтигенспецифическая иммунопрофилактика впервые описана А.М. Безредка, как состояние, развивающееся у животных путем повторных инъекций постепенно повышающихся сублетальных доз антигена; им же предложено дробное введение чужеродной лечебной сыворотки, как способ снижения чувствительности организма человека.
В практической аллергологии иммунотерапия аллергенами была впервые использована в 1911 г. Нуном и Фрименом при пыльцевой аллергии, при астме – Кауфилдом в 1921 г. В России развитие методов гипосенсибилизации связано с именем академика А.Д. Адо и его школы, организацией научно–исследовательской аллергологической лаборатории (НИАЛ АМН СССР).
Всемирная Организация Здравоохранения совместно с ведущими ассоциациями аллергологов рекомендует вместо терминов: «специфическая гипосенсибилизация», «специфическая иммунотерапия», «аллергенспецифическая иммунотерапия» использовать для названия метода иммунотерапии аллергических заболевания следующие определения: иммунотерапия аллергенами, специфическая вакцинация аллергии, специфическая аллерговакцинация (WHO Position paper in Allergen Immunotherapy: Therapeutic vaccines for allergic diseases, 1997).
Специфическая иммунотерапия аллергенами (СИТ)
Лечение аллергических заболеваний включает элиминацию аллергенов, фармакотерапию, специфическую иммунотерапию аллергенами и обучение больных. При показаниях иммунотерапия должна быть использована в сочетании с фармакотерапией для достижения бессимптомного состояния больного, насколько это представляется возможным.
Иммунотерапия аллергенами показана больным, у которых доказано присутствие специфических IgЕ–антител к клинически значимым аллергенам. Назначение иммунотерапии аллергенами зависит от эффективности фармакотерапии, от вида и количества препаратов, необходимых для контроля над симптомами, и от возможности эффективной элиминации аллергенов.
Эффективность иммунотерапии специфична для применяемых аллергенов. СИТ проводится только этиологически значимым аллергеном.
Аллергологи–иммунологи должны знать местную и региональную аэробиологию и воздействия на больного в условиях дома и работы.
Качество аллергенной вакцины имеет решающее значение как для диагностики, так и для лечения. По возможности для иммунотерапии аллергенами должны быть использованы стандартизированные вакцины с известной силой действия и с учетом срока годности.
Применение стандартизированных вакцин с известными характеристиками позволяет определить оптимальную поддерживающую дозу в пределах 5–20(g основного аллергена в каждой инъекции для определенного количества основных аллергенов.
Основной опасностью иммунотерапии аллергенами являются анафилактические реакции. Следовательно, иммунотерапия аллергенами должна производиться под непосредственным наблюдением аллерголога–иммунолога, который может распознать ранние симптомы и признаки анафилактической реакции и назначить соответствующую неотложную терапию.
Аллергенспецифическое снижение иммуного ответа достигается путем введения больному причинно–значимой аллергенной вакцины (аллергенов).
Аллергенные вакцины (терапевтические вакцины для аллергических заболеваний) представляют собой очищенные водно–солевые экстракты аллергенов или выделенные из них отдельные аллергенные компоненты. В соответствии с требованиями Европейской Фармакопейной конвенции, позицией ВОЗ и Комитета по стандартизации аллергенов при Международном Союзе иммунологических обществ терапевтические вакцины для аллергических заболеваний стандартизируются по своей биологической активности (международные единицы – МЕ). С целью контроля качества аллергенов для лечения используются международные эталоны или внутренние референс–препараты (in house reference – IHR). Стандартизация аллергенной активности основана на тестах in vitro, определяющих IgE ответ, и на тестах in vivo – кожные пробы с учетом гистаминового эквивалента.
Для дозирования лечебных доз применяют единицы NOON (объем АГ, который экстрагируют из 1 мкг пыльцы), общего (TNU) или белкового азота (PNU). 1 PNU равна 0,00001 мг белкового азота в 1 мл. Примерная эквивалентность: 1 PNU = 2,6 TNU = 2 ед. NOON. С целью усиления иммуногенных свойств лечебных вакцин для лечения аллергических заболеваний используют аллергены пролонгированного действия с использованием природных и синтетических носителей, депонированные на L–тирозине, гидроокиси алюминия; аллергоиды (аллергены, модифицированные полимеризацией формальдегидом, глутаровым альдегидом и др.). В последние годы для проведения специфической вакцинации используют конъюгаты очищенных аллергенов с синтетическими высокомолекулярными носителями (например, полиоксидонием – Р.В. Петров и соавт.), сукцинилированные (обработанные янтарной кислотой) и потенцированные ферментами (В–глюкоуронидазой) препараты; изучаются возможности применения аллерген–IgG–содержащих комплексов, IgE–связывающих аллергенных гаптенов, Fab–фрагментов моноклональных анти–IgE–антител, фрагментов молекул аллергенов, сохраняющих Т–клеточные эпитопы (использование десенсибилизации, потенцированной ферментом – enzyme–potentiated desensitization – EPD).
Механизмы СИТ (иммунотерапии аллергенами) весьма сложны и продолжают уточняться. Большинство исследователей связывают эффект СИТ с увеличением концентрации IgG4, IgG1 и уменьшением синтеза IgE.
В соответствии с современными представлениями продукция IgE или IgG при иммунном ответе определяется хелперными Т–лимфоцитами (Th или CD4+ лимфоциты), которые в результате распознавания антигена могут дифференцироваться из Th-0 в Th–клетки 1 типа или 2 типа. Th–1 опосредованный вариант ответа приводит к продукции IgG-антител. Цитокины Th–1 (интерлейкин-2 и интерферон) способствуют дифференцировке Th-0 в Th–1 и подавляют образование Th–2. При атопии наблюдается преимущественная дифференцировка пролиферирующих Th-0 лимфоцитов в Th–2. Th–2 клетки участвуют в запуске и поддержании продукции IgE–антител. Th–2, тучные клетки, эозинофилы с помощью сходного профиля цитокинов (IL–4, IL–5, IL–13), мембраносвязанных молекул (gp 39) и секретируемых В–лимфоцитами IgE–антител создают сеть взаимонаправленных позитивных сигналов, поддерживающих аллергическое воспаление. Цитокины Th–2 (IL–4, IL–13, IL–5) способствуют дифференцировке Th–2 и подавляют Th–1.
При СИТ отмечается повышение содержания клеток, продуцирующих IL–12, усиление экспрессии HLA–DR (антиген–представляющие клетки), появление рецепторов для IL–2, появление Th–1 клеток, переключение Th–2 ответа на Th–1 ответ, что приводит к запуску и поддержанию продукции IgG–антител (блокирующих) или формированию Т–лимфоцитарной толерантности. Степень соответствия СИТ классическим моделям толерантности остается предметом изучения и дискуссий. СИТ действует практически на все патогенетически значимые звенья аллергического процесса, оказывает тормозящее действие на клеточный и медиаторный компоненты аллергического воспаления, тормозит раннюю и позднюю фазу IgE–опосредованной аллергии. СИТ оказывает действие на вызванную аллергеном продукцию цитокинов воспаления, включая IL–4 и интерферон. При СИТ угнетаются эффекторные звенья аллергического процесса: уменьшается содержание тучных клеток, угнетается накопление клеток воспаления (эозинофилов и нейтрофилов), что, в свою очередь, приводит к угнетению накопления в тканях организма больного медиаторов воспаления, высвобождаемых из этих клеток, к уменьшению секреции хемотаксических посредников, инициирующих позднюю фазу аллергического воспаления и неспецифическую тканевую реактивность. Возникающие при СИТ изменения характера представительства цитокиновых маркеров, снижение тканевой (органной) чувствительности к экспозиции аллергена, снижение неспецифической тканевой гиперреактивности, угнетение признаков аллергического воспаления сохраняются на протяжении длительного времени. Преимущества СИТ обусловлены терапевтическим действием, которое распространяется на все этапы аллергического ответа; такая широта отсутствует у известных фармакологических препаратов.
Способы применения СИТ
СИТ проводят препаратами аллергенов только в аллергологических кабинетах под наблюдением врача–аллерголога. В зависимости от способа введения аллергена различают подкожный, внутрикожный, аппликационный метод и метод кожных квадратов; оральную, сублингвальную, интраназальную, конъюнктивальную, ингаляционную СИТ. В зависимости от продолжительности курсов – круглогодичную, предсезонную, сезонную СИТ. Выбор метода (предсезонная, сезонная, круглогодичная) определяется этиологией аллергического заболевания.
При бытовой аллергии проводят круглогодичное лечение. Инъекцию бытового аллергена делают обычно 2 раза в неделю до достижения оптимальной дозы, а затем переходят на поддерживающую терапию, при которой эту дозу аллергена вводят 1 раз в 10–14 дней в течение 3–5 лет.
Предсезонную СИТ используют преимущественно при поллинозах и всегда при аллергических реакциях на укусы насекомых. Круглогодичное введение пыльцевых аллергенов (с уменьшением дозы вводимого аллергена в период поллинации) дает лучший клинический эффект.
Существуют методы ускоренной СИТ, например:
Последние два метода в России не применяются.
Для уменьшения антигенной нагрузки на период СИТ рекомендуются мероприятия, направленные на элиминацию аллергена (очистка воздуха), исключение неспецифических раздражителей (курение активное и пассивное, раздражающие запахи и т.п.).
СИТ можно сочетать с базисной и симптоматической терапией аллергических заболеваний (антигистаминные препараты, кромогликат, недокромил, ингаляционные глюкокортикостероиды, b 2-агонисты, холинолитики, метилксантины).
Лица, получающие СИТ, могут быть вакцинированы по эпидемиологическим показаниям АДС–М, АДС, противополиомиелитной вакциной через 2–4 нед после очередной дозы аллергена с последующим продолжением СИТ через 4–5 нед после вакцинации в дозе, предшествующей профилактической прививке. Кожные пробы могут быть поставлены за 10–15 дней до или через 1,5–2 мес после введения вакцинных противоинфекционных препаратов.
• Невозможность прекращения контакта больного с аллергеном
СИТ проводится при поллинозе, атопической форме бронхиальной астмы, аллергическом рините, конъюнктивите, инсектной аллергии в фазу ремиссии.
При лекарственной аллергии СИТ назначается крайне редко, в тех случаях, когда препарат жизненно необходим больному (например, инсулин при сахарном диабете). При пищевой аллергии – когда исключение пищевого аллергена ведет к тяжелым последствиям (например, молоко у детей). При эпидермальной аллергии СИТ показана в тех случаях, когда исключение контакта с животным связано с изменением профессии (зоотехники, ветеринары, лаборанты и т.п.) или тяжелой психологической травмой при расставании с животным.
Низкая индивидуальная мотивация пациента, большая продолжительность аллергического заболевания (после 6 месяцев непрерывного обострения или 2 сезонов пыльцевой аллергии эффективность снижается), возраст старше 50 лет; значительные вентиляционные нарушения (показатели ниже 70% от должных величин); клинические проявления в виде хронической крапивницы, атопического дерматита; сенсибилизация к пищевым, лекарственным, химическим аллергенам; одновременное использование в курсе СИТ четырех и более аллергенов. Длительность лечения и большое число инъекций ограничивают свободу перемещения пациента в период лечения.
Противопоказания к проведению СИТ
Обострение основного аллергического заболевания, наличие выраженных осложнений основного аллергического процесса (эмфизема легких, пневмосклероз), легочное сердце с явлениями хронической дыхательной или сердечной недостаточности, беременность, опухоли, хронические инфекции в стадии обострения (туберкулез, бруцеллез, сифилис и др.), аутоиммунные заболевания (ревматизм в фазе обострения, коллагенозы и т.д.), тяжелые заболевания внутренних органов, нервной и эндокринной систем с нарушением их функций (например, язвенная болезнь желудка и двенадцатиперстной кишки, панкреатит, гепатит, цирроз печени, гломерулонефрит, декомпенсированный сахарный диабет, облитерирующий эндартериит, рассеянный склероз), психические заболевания в фазе обострения, острые инфекционные заболевания, заболевания крови.
Различают местные и общие побочные реакции. Общие побочные реакции обычно связаны с нарушением правил проведения СИТ: превышение дозы вводимого аллергена, проведение лечения необученным персоналом, неправильная техника введения аллергена, попадание аллергена непосредственно в сосуд, введение аллерговакцины на фоне недиагностированной интеркуррентной инфекции, отсутствие контроля за жизненно важными показателями перед вакцинацией (АД, пульс, фоновый уровень пика экспираторного потока).
Общие реакции могут быть конституциональными и системными. Последние развиваются через 10–40 минут после инъекции аллергена и проявляются симптомами разной степени тяжести: от умеренно выраженных кашля, чихания, головной боли, крапивницы, отека лица до синдромной реакции со стороны шоковых органов – конъюнктивита, ринита, приступа бронхиальной астмы. Частота общих реакций колеблется от 0,1 до 21%. Конституциональная реакция может проявляться анафилактическим шоком. В ряде клиник при курсах СИТ случаи системных анафилактических реакций редки (в Саратовском аллергоцентре на 146 010 инъекций 1 анафилактический шок – 0,0007%) или не зарегистрированы (аллергологические кабинеты Москвы, аллергологическое отделение Национального университетского госпиталя в Копенгагене).
Летальные случаи при правильном проведении СИТ – казуистика. Но в Великобритании, где СИТ проводили врачи общей практики, а не аллергологи, с 1957 по 1986 г.г. описано 26 летальных исходов вследствие СИТ. Наступление летальных исходов связано с несвоевременным началом антианафилактических мероприятий, отсутствием противошокового набора.
Местные побочные реакции выражаются образованием на месте инъекции отека, иногда обширного, безболезненного, с явлениями легкого зуда и гиперемии. Опасности для пациента не представляют, проходят самостоятельно под действием антигистаминных средств и/или локальных глюкокортикостероидов в течение нескольких часов. Частота возникновения – 25–35% (А.Д. Адо).
Необходима тщательная регистрация местных реакций для принятия решения о повторении дозы вводимого аллергена до исчезновения местной реакции.
Принципы профилактики осложнений:
Каждое лечебное учреждение, где проводится СИТ, должно иметь противошоковый набор препаратов.
Неотложная помощь при побочных реакциях:
В случае проявлений анафилактического шока начинают в/в введение солевых растворов. Пациент должен лежать горизонтально так, чтобы его голова находилась ниже ног. Адреналин в разведении 1:100 000 вводят медленно (5–10 мкг/мин). Следят за АД, общим состоянием. В случае, если введение жидкости с адреналином не приводит к нормализации АД, начинают осторожное введение вазопрессорных препаратов, затем вводят антигистаминные (например, димедрол, тавегил 2 мл) и глюкокортикоиды (60–90 мг преднизолона или эквивалентные дозы бетаметазона, метилпреднизолона и др.). При наличии бронхоспазма – внутривенно применяют 10,0 мл 2,4% раствора эуфиллина.
Эффективность СИТ доказана в двойных слепых плацебо–контролируемых испытаниях, однако может быть весьма вариабельной в зависимости от:
Наилучшие результаты СИТ достигаются, как правило, при достижении оптимальной суммарной концентрации аллергена после 3 курсов СИТ (средний балл 4,3). Следует отметить, что круглогодичное введение аллергена более эффективно, чем периодические курсы даже при сезонных формах атопии.
После завершения успешных курсов СИТ сохраняется длительная ремиссия (ретроспективный анализ показывает, что до 75% больных астмой с успешной СИТ не имели симптомов более 20 лет); не происходит расширения спектра непереносимых аллергенов; не наблюдается трансформации легких клинических проявлений в более тяжелые (например, ринита в астму); уменьшается потребность в противоаллергических лекарственных препаратах; сохраняется достаточно полноценная физическая и социальная активность пациента.
1. Адо А.Д. Частная аллергология. М.: Медицина, 1976: 57–111.
2. Горячкина Л.А., Астафьева Н.Г. Специфическая иммунотерапия аллергических заболеваний. – РМАПО, Саратовский медицинский университет, 1998: 1–8.
3. Емельянов А.В. Специфическая иммунотерапия. // Общая аллергология. Т.1 под ред. Г.Б.Федосеева. С.–Пб., Нормед–Издат, 2001: 682–93.
4. Abramson M., Puy R., Weiner J. Immunotherapy in asthma: an updated systematic review. // Allergy, 1999; 54: 1022–41.
5. Akdis C., Dlaser K. Mechanism of allergen–specific immunotherapy. // Allergy, 2000; 55: 522–30.
6. Van Nerrven R. The role of allergen–specific T–cells in the allergic immune response relevance to allergic vaccination. // Allergy, 1999; 54: 552–61.
7. Bousquet J. Specific immunotherapy in asthma. // Allergy, 1999, 51: 37–8.
АЛЛЕРГЕН-СПЕЦИФИЧЕСКАЯ ИММУНОТЕРАПИЯ (гипосенсибилизация)
В чем преимущество СИТ перед другими методами терапии аллергических заболеваний? На чем основан метод СИТ? Каковы пути совершенствования СИТ? Аллерген-специфическая иммунотерапия ведет свою историю с 1911 года, когда она была использована для лечен
В чем преимущество СИТ перед другими методами терапии аллергических заболеваний?
На чем основан метод СИТ?
Каковы пути совершенствования СИТ?
Аллерген-специфическая иммунотерапия ведет свою историю с 1911 года, когда она была использована для лечения поллиноза (сезонного аллергического ринита). Этот метод лечения состоит во введении в организм пациента возрастающих доз водно-солевого экстракта того аллергена, к которому у больного выявлена повышенная чувствительность и который ответствен за клинические проявления заболевания. Целью лечения является снижение чувствительности пациента к естественной экспозиции данного аллергена — специфическая гипосенсибилизация. Именно под таким названием этот метод существовал долгое время. С накоплением сведений о том, что в основе лечебного действия этого метода лежат (преимущественно) иммунологические механизмы, его стали именовать специфической (аллерген-специфической) иммунотерапией. Поскольку введением аллергена достигается иммунологически (преимущественно) опосредованное повышение «устойчивости» к действию антигена (аллергена), то в этом было усмотрено сходство самой процедуры с вакцинацией, а аллергенных экстрактов — с вакцинами. Поэтому в настоящее время довольно часто вместо терминов «аллергенные экстракты» или «лечебные аллергены» стали использовать термин «аллергенные вакцины» («аллерговакцины»). Не вдаваясь в обсуждение оправданности и удачности подобных терминологических усовершенствований, эти сведения следует привести лишь для того, чтобы практический врач был осведомлен о смысле существующих терминов.
Со времени появления аллерген-специфической гипосенсибилизирующей терапии (аллерген-специфической иммунотерапии — СИТ) накоплен огромный опыт клинического применения СИТ. Она стала одним из наиболее научно оправданных и широко используемых эффективных методов лечения аллергических заболеваний, в первую очередь тех, которые связаны с IgE-опосредованным механизмом аллергии.
Лечебные аллергены
На протяжении всей истории существования клинической аллергологии для аллерген-специфической диагностики и лечения использовали преимущественно препараты, получаемые экстракцией водно-солевым раствором активных действующих начал из различного сырья (растительного и животного происхождения), при контакте с которым возникают аллергические болезни и реакции. Такие водно-солевые экстракты помимо аллергенных содержат иные компоненты, которые отражаются на качестве препарата. Поэтому аллергенные препараты подвергают специальной очистке, методы которой все время совершенствуются. Важнейшая проблема качества аллергенных препаратов, которая не решена до настоящего времени, заключается в их стандартизации [8]. На разных континентах и в разных странах существуют свои принципы и методы стандартизации аллергенов. Понятно, что при таком подходе невозможно сопоставить аллергенную активность препаратов разных производителей, а несовершенство идентификации самих аллергенных начал в препаратах затрудняет сопоставление аллергенной активности препаратов разных серий даже одного производителя. Поэтому в настоящее время формируется общая всемирная стратегия стандартизации аллергенных препаратов, предусматривающая обязательную стандартизацию аллергенов по следующим трем признакам:
В европейских странах суммарная аллергенная активность препарата стандартизуется по степени вызываемой им кожной аллергической реакции (проба уколом) на чувствительных к данному аллергену пациентах, соотнесенной с кожной реакцией на гистамин. Состав аллергенного препарата характеризуют при помощи использования таких методов, как изоэлектрофокусирование, электрофорез в додецилсульфате натрия — полиакриламидном геле, IgE-иммуноблоттинг, перекрестный радиоиммуноэлектрофорез. IgE-связывающие свойства препарата оценивают в реакции торможения РАСТ (радиоаллергосорбентная техника). В настоящее время стало принципиально возможным для разных производителей определять содержание в препарате главных аллергенов, преимущественно ответственных за повышенную чувствительность организма к сложному по составу аллергену. Для этой цели в распоряжение разных стран передают международные референс-стандарты (ВОЗ), содержащие известные количества соответствующих аллергенов.
Новые технологии клонирования белковых молекул уже сейчас позволили получить многие важные аллергены (аллергены пыльцы растений, постельного клеща, эпидермиса некоторых животных, насекомых, ядов перепончатокрылых и пр.) в виде индивидуальных рекомбинантных белков, имеющих сравнимую аллергенную активность с соответствующими природными белковыми аллергенами. Такая новая технология облегчит стандартизацию аллергенных препаратов, позволив строго количественно определять главные аллергены в производственных сериях лекарственных форм.
Выпускаемые в настоящее время отечественными производителями диагностические и лечебные аллергены стандартизуют по содержанию в препарате единиц белкового азота, а их аллергенную активность устанавливают по результатам кожного тестирования на чувствительных к этому аллергену пациентах, но количественно не оценивают ни в испытаниях in vitro, ни на пациентах. Понятно, что отечественная технология получения и стандартизации аллергенов должна быть приведена в соответствие с современным мировым уровнем, для чего необходимо обеспечение и выполнение соответствующих национальных научно-технических программ.
Механизм СИТ
Чтобы представить себе механизм действия аллерген-специфической иммунотерапии, следует напомнить основные патогенетические звенья аллергического процесса.
Классические и распространенные проявления аллергии, которые подлежат СИТ, представлены заболеваниями, связанными с образованием в организме аллергических антител, принадлежащих к иммуноглобулину Е (IgE). В случае поступления во внутреннюю среду организма аллергена последний фрагментируется в антиген-представляющих клетках до упрощенных пептидов, которые затем представляются этими клетками Т-клеткам-помощникам (Th-клеткам), имеющим профиль Th2-клеток. Этот профиль характеризуется продукцией клетками таких цитокинов, как интерлейкин (IL)-4, IL-13 и IL-5, но не IL-2 или интерферон (IFN)-γ. Th2-клеточный профиль имеет отношение к гуморальному иммунному ответу и, в частности, к IgE-ответу. Th1-клеточный профиль характеризуется продукцией клетками IFN-γ и IL-2, но не IL-4, IL-13 или IL-5. Между Th1- и Th2-клетками существуют реципрокные отношения, и IFN-γ (цитокин Th1-клеток) тормозит (сдерживает) активность Th2-клеток, необходимых для осуществления IgE-ответа.
Образовавшиеся IgE-антитела фиксируются на имеющих к ним очень высокое сродство специализированных рецепторах (высокоаффинные рецепторы для Fc-фрагмента иммуноглобулина Е — Fc(RI), расположенных на тучных клетках слизистых оболочек и соединительной ткани. Таким образом, вооруженные IgE-антителами, тучные клетки оказываются готовы к распознаванию аллергена, если он повторно сможет поступить во внутреннюю среду организма. При повторном поступлении аллерген связывается IgE-антителами, происходит активация тучных клеток, в результате чего из них секретируются медиаторы (гистамин, простагландин D2, лейкотриены C4, D4, E4), фактор активации тромбоцитов — FAT (триптаза и др.), которые вызывают повышение сосудистой проницаемости и отек ткани, сокращение гладкой мускулатуры, гиперсекрецию слизистых желез, раздражение периферических нервных окончаний. Эти изменения составляют основу быстрой (ранней) фазы аллергической реакции (см. рисунок), развивающейся в течение первых минут после действия аллергена. Помимо указанных действий, высвобожденные медиаторы привлекают в зону аллергической реакции другие клетки-участники: базофилы, эозинофилы, моноциты, лимфоциты, нейтрофилы. Пришедшие в эту зону дополнительные клетки-участники аллергической реакции активируются, в результате чего также секретируют проаллергические (провоспалительные) медиаторы. Действие этих клеток и их медиаторов формирует позднюю (или отсроченную) фазу аллергической реакции. Поздняя фаза обусловливает поддержание аллергического воспаления в ткани, хронизацию процесса, формирование и усиление аллерген-неспецифической тканевой гиперреактивности, выражающейся в повышении чувствительности уже не только к конкретному аллергену, но и к разнообразным неспецифическим раздражающим воздействиям (дымы, газы, резкие запахи и пр.; см. рисунок).
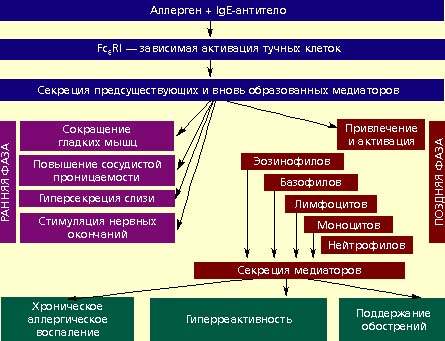 |
| Звенья ранней и поздней фаз IgE-опосредованной аллергической реакции |
Аллерген-специфическое лечение имеет принципиальные преимущества перед всеми другими методами терапии аллергии, так как не действует на симптомы заболевания, а видоизменяет характер реагирования организма на аллерген, вмешивается собственно в патогенез заболевания и потому влияет на все патогенетические звенья аллергического процесса [2].
Клиническая эффективность СИТ выражается в торможении внешних проявлений заболевания и уменьшении потребности в лекарственных препаратах, что обусловлено следующими, по крайней мере тремя особенностями действия СИТ. Во-первых, формируется снижение тканевой (органной) чувствительности к аллергенной экспозиции, что многократно подтверждено, помимо клинических наблюдений, проведением провокационных проб с аллергеном. Во-вторых, возникает снижение неспецифической тканевой гиперреактивности, что, в частности, устанавливается по снижению чувствительности к разным медиаторам аллергии. В-третьих, клинически эффективная СИТ сопровождается угнетением признаков аллергического воспаления.
Снижение неспецифической тканевой гиперреактивности и противовоспалительное действие, так же как и специфическая гипосенсибилизация, удерживаются на протяжении длительного (многолетнего) периода наблюдений после завершения СИТ. Легко заметить, что эти эффекты СИТ объединяют в себе способы действия разнообразных современных противоаллергических фармакологических препаратов, лишь избирательно воздействующих на то или иное звено аллергического процесса.
Каковы же основные точки приложения действия СИТ?
Известно, что у атопических больных в период естественной аллергенной экспозиции (например, в период цветения растений, к пыльце которых имеется повышенная чувствительность) возникает прирост содержания в крови IgE-антител. СИТ сопровождается торможением такого прироста IgE-антител, а после повторных курсов СИТ наступает и некоторое уменьшение уровня IgE-антител по сравнению с исходным. Однако прямой связи между степенью торможения продукции IgE-антител и выраженностью положительного клинического эффекта все же не существует.
Давно сформировалась точка зрения, согласно которой основной механизм СИТ заключается в перестройке характера иммунного ответа на действие аллергена, состоящей в образовании так называемых блокирующих антител, принадлежащих к IgG и лишенных способности сенсибилизировать ткани, но обладающие аллерген-связывающей активностью, за счет чего они предотвращают (вернее, уменьшают) вероятность взаимодействия аллергена с IgE-антителами. И все же далеко не всегда значительное увеличение содержания аллерген-специфических IgG-антител совпадает с выраженным клиническим улучшением состояния больных. В последнее время появились сведения о том, что и образование анти-IgE-антител может быть вкладом в лечебное действие СИТ.
Более всего вероятно, что образование IgG-антител, анти-IgE-антител и угнетение продукции IgE-антител опосредуют механизм СИТ лишь частично и в комплексе как друг с другом, так и с иными процессами. В последние годы накоплены сведения, указывающие на то, что СИТ, сопровождающаяся выраженным клиническим улучшением состояния пациентов, характеризуется угнетением вовлечения в искусственно провоцируемую или вызванную естественной экспозицией аллергена аллергическую реакцию тех клеточных единиц, которые опосредуют эффекторную стадию аллергии. Так, в тканях после СИТ уменьшается содержание тучных клеток, уменьшается накопление клеток воспаления (эозинофилов, нейтрофилов), тормозится высвобождаемость медиаторов из клеток-мишеней аллергии (тучных клеток, базофилов) при стимуляции их специфическим аллергеном или неспецифическими активаторами. Действие СИТ затрагивает также и лимфоидные клетки таким образом, что происходит смещение их профиля от Th2-клеток в сторону Th1-клеток. Все это может объяснять влияние СИТ не только на раннюю, но и на позднюю фазу аллергического процесса.
Итак, СИТ обладает таким терапевтическим действием, которое распространяется на все этапы аллергического процесса и отсутствует у известных фармакологических препаратов, в том числе у имеющих полифункциональную активность. Действие СИТ охватывает собственно иммунологическую фазу и приводит к переключению иммунного ответа с Th2-типа на Th1-тип, тормозит как раннюю, так и позднюю фазы IgE-опосредованной аллергической реакции, угнетает клеточную картину аллергического воспаления и неспецифическую тканевую гиперреактивность. Еще раз следует подчеркнуть, что СИТ принципиально отличает от фармакотерапии длительно сохраняющийся лечебный эффект после завершения курсов лечения.
Клиническая эффективность СИТ
За 90-летний период применения СИТ накоплен огромный клинический опыт, свидетельствующий о ее высокой лечебной эффективности. По данным многочисленных исследований, в том числе проведенных в нашей стране, положительный терапевтический эффект СИТ достигается в 80-90% случаев и более. Столь высокого уровня терапевтической эффективности удается добиться при следующих условиях:
Данные предыдущих лет о высокой лечебной эффективности СИТ подтверждены в последнее время в специальных работах, выполненных на основе принципов доказательной медицины.
Эти исследования представляли собой двойные слепые, плацебо-контролируемые испытания на рандомизированных группах пациентов, подобранных на основании четких клинических критериев и результатов аллергологической специфической диагностики, с использованием стандартизованных очищенных аллергенов при достижении оптимальной поддерживающей дозы (порядка 5-20 мкг главного аллергена на инъекцию для таких аллергенов, как пыльца сорняков, трав, кошачья шерсть, яды перепончатокрылых) и при условии достаточной продолжительности (завершенности) курсов лечения.
Основные выводы этих исследований, характеризующие клиническую эффективность СИТ, могут быть сведены к следующему.
По вопросу о клинической эффективности СИТ, проводимой бактериальными аллергенами, существуют разные точки зрения, но, по данным целого ряда исследователей, и в этом случае может быть получен выраженный положительный клинический эффект.
Место СИТ в системе противоаллергического лечения
Давно признанным и обоснованным положением аллергологии является то, что первым обязательным этапом противоаллергического лечения должно быть проведение комплекса мероприятий, направленных на исключение или ограничение аллергенного воздействия на пациента. Если элиминационные меры недостаточны, то проведение СИТ становится необходимым, разумеется при соблюдении упомянутых выше условий.
Фармакотерапия аллергических заболеваний проводится в настоящее время несколькими группами противоаллергических лекарственных препаратов, позволяющих эффективно контролировать симптомы заболевания (Н1-антигистаминные средства, антилейкотриеновые препараты, стабилизаторы клеток-мишеней аллергии — препараты кромоглициевой кислоты и недокромил натрия, ксантиновые производные, β2-агонисты, топические и системные кортикостероидные препараты). Однако, с одной стороны, применение фармакологических препаратов не должно заменять СИТ, а с другой — СИТ предусматривает дополнительное использование и фармакологических средств, если в том возникает потребность. Содержащееся в целом ряде международных и национальных рекомендаций предложение приступать к СИТ только в тех случаях, когда фармакотерапия неэффективна, не может быть принято. Это объясняется тем, что СИТ тем эффективнее, чем раньше она начала проводиться.
Кроме того, как указано выше, своевременно проведенная СИТ позволяет, во-первых, предотвратить переход заболевания в более тяжелые формы, а во-вторых, снижает (или даже полностью устраняет) потребность в лекарственных препаратах. Наконец, после завершения СИТ удается добиться многолетней ремиссии, чего нельзя достичь лекарственными средствами.
К сказанному следует добавить и еще один аргумент, который обоснован механизмом действия СИТ. Напомним, что СИТ распространяет свое действие на все звенья аллергического процесса: на собственно иммунологическое звено, на эффекторные клетки (на тучные клетки) ранней фазы, на клетки-участники поздней фазы аллергического ответа, снижает не только аллерген-специфическую тканевую чувствительность, но и неспецифическую тканевую гиперреактивность, предупреждает расширение спектра аллергенов, к которым формируется повышенная чувствительность. Ни одно фармакологическое лекарственное средство не обладает таким полифункциональным действием. Именно в силу этих важных обстоятельств в отечественной аллергологии давно сложилось мнение о необходимости как можно более раннего начала проведения аллерген-специфического лечения, обеспечивающего профилактику обострений заболевания.
Безопасность СИТ
В ходе проведения СИТ в ответ на введение аллергена могут возникать нежелательные побочные эффекты в виде местных или системных реакций.
К местным реакциям относят те, которые возникают в месте введения аллергена и характеризуются местной гиперемией, иногда чувством зуда в области инъекции, признаками отека ткани. Эти реакции обычно возникают в первые 30 минут, хотя следует иметь в виду, что они могут проявиться и в более отдаленные сроки. Возникновение местных реакций является поводом для коррекции дозы аллергена (ее уменьшения) в последующее введение.
Системные реакции — это реакции, возникающие вне области введения аллергена. Обычно они появляются в пределах нескольких минут после инъекции аллергена и в редких случаях — спустя 30 минут. Обоснованным является подразделение системных реакций на те, которые не угрожают жизни пациента, и угрожающие (анафилактический шок, отек жизнено важных органов — отек гортани). К системным реакциям могут быть отнесены такие, как головная боль, боли в суставах, ощущение дискомфорта. К умеренным признакам системных реакций относят легкие проявления ринита или бронхиальной астмы (пиковая скорость выдоха не ниже 60% от должной величины или от показателя пациента в период стойкой ремиссии), хорошо контролируемые соответствующими лекарственными препаратами (Н1-антагонистами или ингаляционными β2-агонистами). Более выраженной степени реакции соответствуют признаки крапивницы, отеки Квинке, нарушение бронхиальной проходимости (показатели пиковой скорости выдоха ниже 60% от должной величины или от показателя пациента в период стойкой ремиссии), контролируемые соответствующим лечением. Угрожающие жизни реакции требуют проведения интенсивной терапии. При возникновении системных реакций обязательным является пересмотр программы СИТ для данного пациента.
Хотя существуют указания на то, что время наступления системных реакций коррелирует с их тяжестью, следует иметь в виду, что эти реакции могут возникать и через 30-60 минут после инъекции аллергена. Интенсивность местной реакции не является надежным индикатором проявления системной реакции. В ряде исследований, обобщающих большое число наблюдений, показано, что, как правило, системные реакции возникали в отсутствие предшествующей сильной местной реакции.
Анализ системных реакций показывает, что в большинстве случаев они возникали вследствие отклонения от принятых правил проведения СИТ. В частности, выявлены следующие факторы:
Перед исследователями, занимающимися изучением клинической эффективности и безопасности СИТ, неоднократно вставал вопрос о возможности снижения риска возникновения системных реакций путем предварительного использования противоаллергических фармакологических средств. Как вариант предлагали проводить премедикацию комбинацией метилпреднизолона и кетотифена, препаратами теофиллина длительного действия. Такие предложения небезупречны, поскольку теофиллин может обладать нежелательным действием на сердечно-сосудистую систему, а кетотифен — седативным эффектом. Что касается стероидных препаратов, то их применение в данном случае не может быть оправданным, так как нельзя исключить угнетающего действия именно на Th1-тип иммунного ответа, с которым связывают лечебный эффект СИТ.
Имеются специальные данные, в том числе двойных слепых, плацебо-контролируемых исследований, свидетельствующие о том, что антигистаминные препараты (Н1-антагонисты) уменьшают частоту возникновения системных и тем более местных реакций при СИТ. Ранее, в период применения Н1-антагонистов первого поколения, их использование для данных целей считалось неоправданным. Такие ограничения были связаны с опасениями, что применение этих препаратов, не предотвратив самой системной реакции, может сделать незаметными ее клинические предвестники, вследствие чего будут пропущены начальные признаки системной реакции. Эти опасения вполне обоснованны, так как Н1-антагонисты первого поколения, с одной стороны, имеют относительно слабое сродство к Н1-рецепторам гистамина, а с другой — обладают седативным действием, вследствие которого пациент теряет адекватную оценку своего состояния. Кроме того, другие побочные действия антигистаминных препаратов первого поколения (прежде всего это действие на сердечно-сосудистую систему) могут усилить проявления системных реакций.
Положение существенно изменилось с появлением Н1-антагонистов второго и третьего поколений, обладающих высоким сродством к Н1-рецепторам (т. е. очень высокой избирательной антигистаминной активностью), не имеющих седативного действия (или имеющих слабо выраженный седативный эффект) и нежелательных побочных действий, присущих их предшественникам. Эти препараты эффективно предотвращают появление местных реакций при СИТ и снижают частоту возникновения системных реакций [7]. Понятно, что предпочтение в этом случае должно быть отдано препаратам, имеющим наилучший профиль безопасности, высокую антигистаминную активность и не обладающим седативным действием. Таким препаратом, как известно, является Н1-антагонист третьего поколения — фексофенадин (телфаст), представляющий собой фармакологически активный метаболит препарата второго поколения (терфенадина). Он имеет безупречный профиль безопасности, у него отсутствуют кардиотропные (кардиотоксические) свойства и он совершенно не обладает седативным действием [3 ].
По сравнению с многомиллионным числом инъекций аллергенов, осуществляемых ежегодно во всем мире, частота возникновения нежелательных системных реакций является низкой. Проблемы, связанные с возникновением осложнений СИТ в виде тяжелых системных реакций, появляются в тех странах, в которых к проведению СИТ допускают не специалистов-аллергологов, а врачей других специальностей и врачей общей практики. Так было, например, в Великобритании, где с 1957 по 1986 год зарегистрировано 26 смертельных случаев, которые могли быть связаны с проведением СИТ. При анализе этих случаев оказалось, что они были обусловлены непрофессиональным выполнением СИТ. Напротив, в странах, в которых СИТ выполняют только специалисты, имеющие опыт и узаконенное право проведения такого лечения, а само лечение осуществляется в специализированных медицинских учреждениях, имеющих необходимые средства для лечения возможных побочных эффектов, системные реакции если и возникали, то не приводили к серьезным последствиям. Так, в Дании при анализе проведенных 10 тыс. лечебных инъекций в аллергологическом отделении Национального университета в Копенгагене не установлено ни одного случая системных анафилактических реакций. Аналогичные данные получены в аллергологических кабинетах Москвы [1], которые сейчас располагают уже 40-летним опытом применения СИТ. Поэтому обязательным является соблюдение следующего правила: аллерген-специфическая иммунотерапия (аллерген-специфическая гипосенсибилизация) должна выполняться только обученными специалистами (врачами-аллергологами), имеющими опыт проведения этого лечения, в условиях аллергологического кабинета или стационара.
Именно в специализированном аллергологическом подразделении предусмотрено наличие необходимых средств не только для проведения СИТ, но и для купирования побочных реакций, если они возникают [4]. Такие правила соблюдались в нашей стране с момента создания в ней аллергологической службы в начале 60-х годов, благодаря чему отечественная аллергология смогла избежать печального опыта стран, в которых к проведению СИТ допускали иных специалистов, в частности врачей широкого профиля. Обязанностью врача широкого профиля является направление пациента с установленным диагнозом аллергического заболевания или с подозрением на такой диагноз к врачу-аллергологу для решения, в частности, вопроса о проведении СИТ.
Совершенствование СИТ
Совершенствование СИТ и лечебных форм аллергенов направлено, с одной стороны, на снижение способности лечебных препаратов вызывать аллергические реакции, а с другой — на сохранение или усиление их иммуногенных свойств. Это необходимо для повышения терапевтической эффективности СИТ и улучшения профиля безопасности лечебных форм аллергенов.
Для достижения такой цели используются как изменение способов введения и доставки лечебных аллергенов, так и разнообразные методы модификации самих аллергенных начал.
Помимо инъекционного введения аллергенов испытываются разные варианты местной (топической) СИТ в виде приема аллергенов через рот, интраназального, ингаляционного введения, введения аллергенов в составе липосом. Пока что не получены окончательные доказательства достаточной эффективности подобных приемов.
Модификация аллергенов достигается разными способами: полимеризацией аллергенов (формальдегидом, глутаровым альдегидом и пр.), получением сорбированных форм (на L-тирозине, на гидроокиси алюминия), применением разнообразных природных и синтетических носителей, аллерген-IgG-содержащих комплексов, использованием вместо самих аллергенов кодирующей их плазмидной ДНК, IgE-связывающих аллергенных гаптенов (неспособных активировать клетки-мишени аллергии, но связывающихся с IgE и предупреждающих тем самым последущее соединение антитела с аллергеном), полученных биотехнологическими приемами отдельных молекул аллергенов и их фрагментов. Приведенный перечень научных направлений, разрабатываемых в настоящее время, свидетельствует о том огромном интересе, который проявляют исследователи всего мира к проблеме аллерген-специфического лечения аллергических заболеваний.
Правда, большинство этих разработок находятся пока что на стадии экспериментальных исследований, но некоторые уже сейчас внедрены в широкую медицинскую практику, в том числе в нашей стране. Так, осуществляется выпуск коммерческих полимеризованных аллергенов (аллергоидов), которые имеют сниженную аллергенную активность, но сохраненную иммуногенную. Благодаря этому аллергоиды могут быть использованы в более высоких поддерживающих дозах, но с менее частым введением лечебных доз, чем водно-солевые экстракты. Это обеспечивает большую терапевтическую эффективность, лучший профиль безопасности и большее удобство проведения СИТ.
В Институте иммунологии МЗ РФ на протяжении ряда лет выполнялись работы по направленной модификации иммуногенных и аллергенных свойств распространенных аллергенов путем получения комплексных соединений молекул аллергенов и иммуностимуляторов. Результатом этих работ явилось создание лечебных препаратов на основе аллергоидов пыльцевых аллергенов и иммуностимулятора полиоксидония. Эти препараты в настоящее время подготовлены для проведения клинических испытаний [5, 6].
Разработка этих новых и высокоактуальных научных направлений обеспечит повышение эффективности аллерген-специфической терапии, еще более расширит ее использование в комплексе противоаллергических лечебных и профилактических мероприятий.