Радионуклидные препараты что это
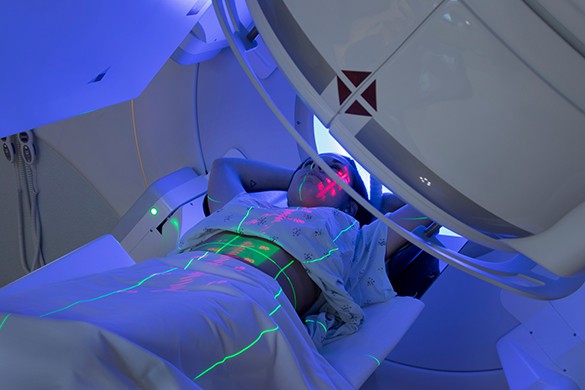
Как проходит исследование методом радионуклидной диагностики
Эти исследования связаны с ионизирующим излучением и/или введением в организм радиофарм-препаратов, которые позволяют получить данные о функциональных изменениях.
Пациенту внутривенно вводят радиофармпрепарат. В качестве радионуклидной «метки» используется Tс 99m с периодом полураспада 6,01 часа. Для полного выведения из организма радиоактивности необходимо 10 периодов полураспада, то есть около 2,5 суток. Первые сутки не рекомендуется находиться рядом с детьми до 18 лет.
Подготовка к исследованию: специальной подготовки к исследованию не требуется, также нет ограничений в приеме пищи.
После введения радиофармпрепарата пациент обязан находиться в комнате для ожидания и выполнять требования среднего медицинского персонала. Запрещено покидать отделение без разрешения.
Время исследования занимает от 1 до 6 часов.
Обследование
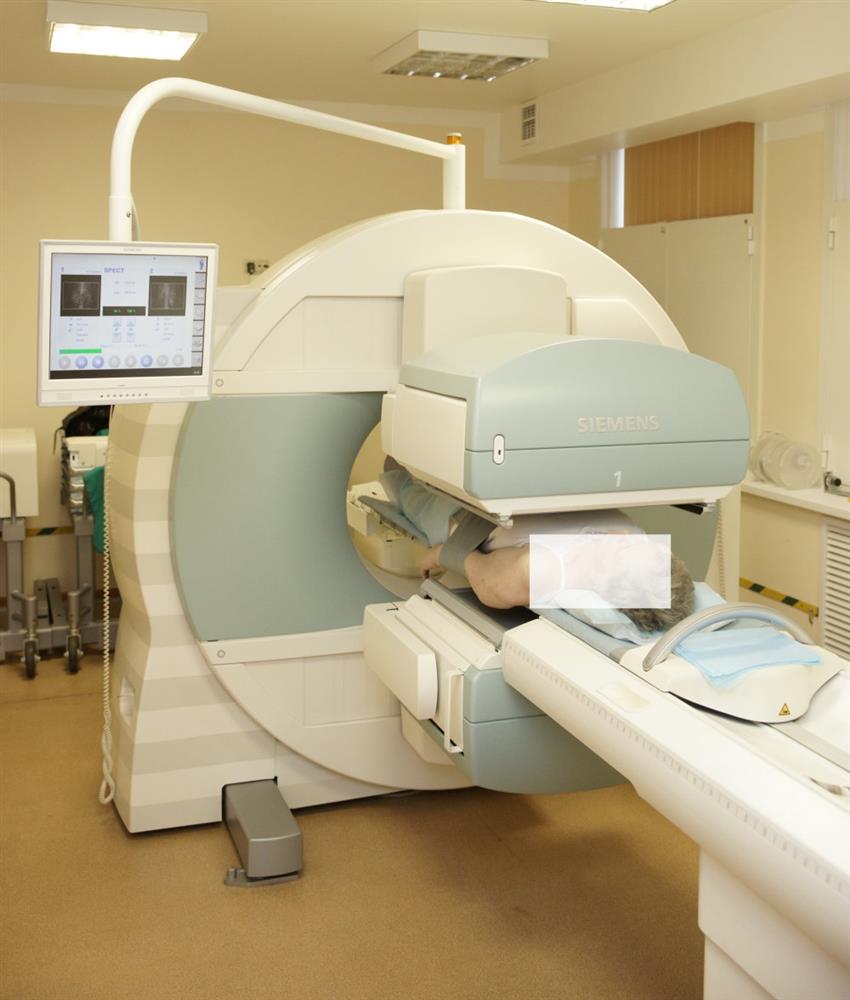
Для проведения обследования пациента укладывают на стол и помещают внутрь гамма-камеры. Во время всего исследования врач ведет наблюдение с помощью телекамеры или визуально. Основным условием для качества получаемых изображений является возможность неподвижно в течение 20 минут находиться внутри гамма-камеры. При обследовании маленьких детей, а также взрослых с болевым синдромом, которые не могут лежать спокойно, необходимо заранее обсудить вопрос о возможности выполнения процедуры с врачом-анестезиологом.
Обычно процедура не сопровождается какими-либо неприятными ощущениями или побочными реакциями.
В зависимости от исследования, полученная пациентом эффективная доза составляет от 0,3 до 15 мЗв. Результаты обследования готовы через 24 часа после окончания процедуры. Возможна запись на CD-диск (оговаривается отдельно).
Первые сутки после обследования мы не рекомендуем находиться рядом с детьми до 18 лет. При пересечении Государственной границы РФ, а также в пунктах досмотра пассажиров необходимо будет представить справку о проведенном радионуклидном исследовании, которую можно получить в регистратуре отделения.
Диагностика и лечение раковых опухолей с использованием радиоактивных изотопов
Лучевая терапия уже давно является одним из основных способов лечения злокачественных новообразований. Однако среди ее недостатков — широкая зона облучения, которая поражает не только саму опухоль, но и окружающие здоровые ткани.
Современная медицина постепенно отказывается от традиционной лучевой терапии, поскольку появляются новые, более эффективные и безопасные методы ядерной медицины. Одним из таких является лечение радиоизотопами, которое активно применяют специалисты медицинского центра «Анадолу».
Какие виды такой терапии существуют?
Терапия «Лютеций-177-ПСМА»
Это лечение основано на использовании радиоактивного изотопа элемента лютеция. Его применяют для борьбы с раком предстательной железы на поздних стадиях. Терапия основана на том, что раковые клетки железы имеют на своей поверхности большое количество рецепторов к особому белку — простат-специфическому мембранному антигену (ПСМА). Комплексы, состоящие из изотопа лютеция-177 и ПСМА, с высокой избирательностью присоединяются именно к этим рецепторам, а значит основная часть излучения будет воздействовать именно на опухолевые клетки.
Терапия «Лютеций-ДОТАТАТ»
Принцип действия этого метода лечения схож с терапией «Лютеций-177-ПСМА», только здесь в качестве мишени выступают клеточные рецепторы к гормону соматостатину. Они в большом количестве присутствуют на мембранах клеток нейроэндокринных опухолей желудочно-кишечного тракта и поджелудочной железы.
Терапия «Актиний-225-ПСМА»
Данный способ основан на тех же принципах, что и терапия «Лютеций-177-ПСМА», и точно так же предназначен для уничтожения радиоактивным излучением раковых клеток в предстательной железе. Отличие тут в применении другого радиоизотопа — актиния-225. Если лютеций-177 при распаде излучает бета-частицы, то есть высокоэнергетические электроны, то актиний-225 при распаде излучает альфа-частицы — ядра гелия. Терапию «Актиний-225-ПСМА» применяют в случаях, когда пациент не демонстрирует хорошего ответа на радионуклидное лечение лютецием-177.
Терапия радием
Основана на природной радиоактивности данного элемента, который производит альфа-излучение, а в организме человека ведет себя подобно кальцию. Это означает, что более 80% попадающего в наше тело радия накапливается в костях. А следовательно, его удобно использовать для местного радиационного воздействия на метастазы злокачественных опухолей в костной ткани.
Каковы цели радионуклидной терапии?
В первую очередь, задача такого лечения — уничтожить максимальное количество опухолевых клеток в организме больного. Уменьшение размера злокачественных очагов, а также уничтожение отдельных метастазов позволяет затем прибегнуть к радикальной операции по удалению новообразования. Кроме того, сокращение числа опухолевых элементов благотворно отражается на самочувствии пациента и облегчает симптомы развернутого онкологического заболевания. Снижение выраженности болевого синдрома и других проявлений особенно важно, поскольку обычно радионуклидную терапию назначают на поздних стадиях опухолевого процесса или при слишком сильных побочных эффектах от химиотерапии.
Безопасно ли лечение радиоизотопами?
Строго говоря, и рецепторы к простат-специфическому мембранному антигену, и рецепторы к соматостатину имеются и на здоровых клетках. Но на мембранах злокачественно перерожденных клеток их количество в разы больше. А значит именно к этим клеткам и присоединится подавляющее большинство молекулярных комплексов с радиоактивными элементами. Следовательно, и доза излучения, полученная опухолью, будет намного выше. Это свойство радионуклидной терапии называют таргетностью (от слова target, или «цель»), оно означает высокую точность воздействия именно на злокачественное новообразование, а не на здоровые ткани.
Кроме того, важную роль для безопасности лечения играют типы радиационного излучения, которые при нем используются. Лютеций-177 производит бета-излучение, а актиний-225 и радий — альфа-излучение. Проникающая способность бета-частиц довольно невелика — их останавливают всего 2–2,5 сантиметра живой ткани. То есть воздействовать это излучение будет исключительно на местном уровне. Проникающая способность альфа-частиц еще меньше — оно способно пройти всего через 5–10 соседних клеток. А значит здесь таргетность воздействия на опухолевые клетки будет максимально высокой.
Радионуклидные методы лечения на современном этапе
А.Ф. Цыб, академик РАМН, профессор
ГУ – Медицинский радиологический научный центр РАМН,
Обнинск, ул. Королева 4, 249036 г., Калужская область, Российская Федерация
Адрес для переписки: Анатолий Федорович Цыб; e-mail:
Новые достижения в области ранней диагностики и эффективного лечения больных как онкологическими, так и неонкологическими заболеваниями во многом обязаны появлению современных радиологических технологий диагностического и лечебного назначения.
Радиологические методы диагностики и лечения, как известно, пронизывают всю систему оказания медицинской помощи населению. Сегодня уже никого не удивляет то, что, начиная с районной больницы, на службе здравоохранения имеются кабинеты рентгеновской и ультразвуковой диагностики, в крупных городах и областных центрах можно провести как компьютерно-томографическое обследование, так и важные функциональные радиоизотопные исследования в целях раннего выявления заболеваний и нарушений функций органов и систем еще до появления клинических признаков. Кроме того, практически в каждом субъекте Федерации имеется как минимум один онкологический диспансер, оснащенный современным радиологическим оборудованием для проведения лучевой терапии больным со злокачественными опухолями.
Однако современные высокотехнологичные радиологические методики, способные успешно конкурировать с традиционными методами лечения, включая хирургический, разрабатываются и развиваются главным образом в крупных научных центрах, где имеется необходимая инфраструктура, высококвалифицированные подготовленные специалисты и надлежащая научная проработка.
Медицинский радиологический научный центр РАМН (ГУ – МРНЦ РАМН) является в Российской Федерации учреждением по разработке и применению в медицине радиологических методов диагностики и лечения больных. В МРНЦ РАМН разрабатываются и внедряются новые высокотехнологичные медицинские стандарты оказания медицинской помощи, способные в короткие сроки решить ряд социально важных проблем отечественного здравоохранения, особенно в онкологии.
В качестве примера можно привести такие радиологические технологии, как лечение радиоактивным йодом-131 больных токсическим зобом и раком щитовидной железы с отдаленными метастазами (радиойодтерапия), брахитерапия с использованием микроисточников 125 I при раке предстательной железы, применение нейтронного излучения атомных реакторов и ускорителей (дистанционная нейтронная и нейтрон-захватная терапия), а также калифорния-252 (внутритканевая терапия), лазерная фотодинамическая терапия, лучевой компонент в технологии органосберегающих операций, локальная гипертермия. Эти технологии являются относительно малоизвестными и малодоступными для широких слоев населения России.
Ниже представлены некоторые из высокотехнологичных радиологических методов, применяемых в МРНЦ РАМН для эффективного лечения больных с заболеваниями опухолевого и неопухолевого характера.
Радионуклидная терапия открытыми источниками излучения
В настоящее время Клиника МРНЦ РАМН имеет комплекс необходимого оборудования и опыт применения с диагностической и лечебной целями открытых источников излучения. Ежегодно в таком лечении нуждаются около 50.000 больных РФ. Фактически его получают около 2.000, что примерно в 25 раз ниже потребностей. В России имеется всего два таких отделения – в МРНЦ РАМН (28 специализированных коек) и в РМАПО (Российская медицинская академия последипломного образования), где задействованы всего 4 специализированные койки.
Наличие в РФ около 300 лабораторий радиоизотопной диагностики и всего лишь двух отделений радионуклидной терапии связано с тем, что в последних, в отличие от лабораторий радиоизотопной диагностики, применяются не индикаторные, а существенно более высокие активности радионуклидов, требующие дорогостоящих очистных сооружений, защитных приспособлений, специально обустроенных палат с изолированными системами воздухообмена и специальной канализации. К сожалению, Россия пока отстает от других стран в оказании этого вида медицинских услуг.
В МРНЦ РАМН широко применяется наиболее распространенный вид радионуклидной терапии – радиойодтерапия при таких заболеваниях, как рак щитовидной железы и токсический зоб.
Радиойодтерапия при токсическом зобе
Использование йода-131 эффективно при лечении больных доброкачественными заболеваниями щитовидной железы, в том числе диффузным и узловым токсическим зобом, сопровождающимися тиреотоксикозом.
Применяемые методы лечения: медикаментозный, хирургический и радиоактивным йодом. Медикаментозное лечение может длиться годами, дает частые осложнения, его эффективность не превышает 15-20%. Хирургическое лечение длится 2-3 недели, возможны тяжелые осложнения, излечение достигается в 80-90% случаев.
Эффективность радиойодтерапии составляет 90-95%. Она хорошо переносится больными и возможна даже при тяжелом течении заболевания. Во многих странах проводится амбулаторно, а при более строгих нормах радиационной безопасности требует госпитализации на 2-3 дня. Осложнения редки и легкие по своим проявлениям. Радиоактивный йод избирательно накапливается и повреждает активно функционирующие клетки щитовидной железы, избыточно продуцирующие тиреоидные гормоны (рис.1). В течение 2005 г. пролечено около 700 больных диффузным и узловым токсическим зобом с симптомами тиреотоксикоза. Ежегодно в радиойодтерапии нуждается около 25 тысяч таких больных, что свидетельствует о том, что из-за недостаточной мощности специализированных отделений этот вид лечения получает лишь минимальное количество пациентов.
Рис. 1. Сцинтиграмма щитовидной железы. Повышенное накопление радиойода
при диффузном (слева) и узловом (справа) токсическом зобе.
Радиойодтерапия при раке щитовидной железы с отдаленными метастазами
Методика особенно эффективна и не имеет альтернативы при лечении больных дифференцированным раком щитовидной железы с отдаленными метастазами (рис.2). В России ежегодно нуждается в радионуклидной терапии около 4000 таких больных. С каждым годом увеличивается потребность в этом методе лечения, так как большинство больных не получают его своевременно (непосредственно после оперативного лечения).
Рис. 2. Результаты радиойодтерапии ( 131 I) папиллярного рака щитовидной железы
с метастазами в легкие (больной 10 лет, сцинтиграфия всего тела).
За последние 10 лет в МРНЦ РАМН пролечено более 6.000 больных раком щитовидной железы, среди которых более 200 детей, в том числе дети, проживающие на территориях, загрязненных радионуклидами вследствие чернобыльской аварии. Эффективность радиойодтерапии при метастатическом поражении легких достигает 70%.
Лечение самарием-оксабифором 153 Sm при метастатическом поражении костей и ревматоидном артрите
Показана высокая эффективность радиофармпрепарата самария ( 153 Sm-оксабифор) при лечении онкологических больных с метастазами в кости и выраженным болевым синдромом, а также больных ревматическими заболеваниями со стойкими артралгиями. Положительный эффект отмечен у 75% из более 300 пролеченных пациентов. В целом по стране число нуждающихся в таком лечении составляет ежегодно около 7 тысяч с заболеваниями опорно-двигательного аппарата и 14 тысяч онкологических больных.
Удовлетворение потребностей в радионуклидной терапии может быть достигнуто за счет расширения фонда уже существующих специализированных подразделений, а также создания новых центров ядерной медицины в отдаленных регионах, подготовке квалифицированных кадров для них и тиражировании разработанных в МРНЦ РАМН лечебных технологий.
Развитие ядерно-медицинских методов диагностики и лечения тесным образом связано с выпуском и созданием специального оборудования (например, гамма- и ПЭТ-камер, томографов и др.) и производством современных радиофармпрепаратов (РФП). В мире отмечается тенденция к бурному развитию рынка радиофармпрепаратов.
В России также ведутся работы в данном направлении. В частности, на базе научных центров Москвы и Обнинска получены новые оригинальные РФП, которые уже сейчас пользуются спросом за рубежом (например, генераторы радионуклида рения-188, который может найти широкое применение не только в онкологии, но и при лечении больных сердечно-сосудистой патологией, микроисточники йода-125, получившие широкое применение при раке предстательной железы, самарий-153-оксабифор, применяемый для воздействия на метастазы злокачественных опухолей в кости и при ревматоидном артрите, альфа-излучающие РФП на основе генератора 225 Ас/ 213 Bi для лечения микрометастазов при опухолях различных локализаций, а также ревматоидного артрита, ВИЧ-инфекции и другие РФП). Однако успешное развитие этого направления невозможно без серьезной государственной поддержки.
Брахитерапия рака предстательной железы
Рак предстательной железы является одним из наиболее распространенных видов злокачественных новообразований в мире. По заболеваемости населения он занимает первое место в США, второе – в странах Западной Европы и четвертое – в России.
Освоенный в МРНЦ РАМН метод брахитерапии основан на внедрении закрытых микроисточников (сидов) излучения йода-125 непосредственно в ткань предстательной железы. Брахитерапия является современным, высокотехнологичным и эффективным методом лечения, он позволяет проводить радикальное лечение онкологических больных с сопутствующими заболеваниями, сократить госпитализацию до 2 дней и обеспечить высокое качество жизни пациента. В некоторых случаях процедура введения микроисточников йода-125 может быть выполнена амбулаторно.
Если по эффективности брахитерапия сравнима с радикальным оперативным лечением, то по количеству осложнений имеет неоспоримые преимущества. Пациент выписывается из клиники на следующий день после процедуры и может приступать к работе и вернуться к нормальному образу жизни. Данная технология эффективна также при рецидивном раке предстательной железы, когда другие методы лечения неприемлемы или малоэффективны.
В клинике МРНЦ РАМН используется техника имплантации микроисточников под контролем ультразвука (с учетом опыта немецких специалистов 1 ) и спиральной компьютерной томографии со стереотаксической приставкой (с учетом опыта специалистов США 2 ) (рис.3), что значительно расширяет возможности брахитерапии и позволяет проводить радикальное лечение вне зависимости от объема железы, наличия кальцинатов и при распространении опухоли за пределы капсулы.
На сегодняшний день успешно пролечено более 150 больных. Всего же в России в таком лечении нуждаются ежегодно около 8-10 тысяч пациентов.
Рис. 3. Микроисточники, имплантированные в предстательную железу.
Отсутствие на данный момент налаженного производства микроисточников йода-125, стоимость которых составляет до 90% затрат на лечение, не позволяет пока существенно снизить себестоимость этого метода лечения и сделать его более доступным для широких слоев населения. В настоящее время совместно с ГНЦ РФ – ФЭИ проведена разработка и испытание опытной партии микроисточников отечественного производства. Более широкое использование брахитерапии в лечении больных раком предстательной железы позволит в короткий период (два-три года) существенно снизить смертность от этого заболевания и увеличить продолжительность жизни мужчин. Вопрос может быть решен, в частности, за счет тиражирования новой технологии в некоторые субъекты РФ с подготовкой специалистов в уже созданном на базе МРНЦ РАМН Учебно-методическом центре.
Таким образом, высокотехнологичные лечебные радиологические методы имеют все основания занять свое достойное место, существенно дополняя, а в ряде случаев и заменяя традиционные методы лечения многочисленной группы заболеваний. Именно эти технологии обеспечивают достижение таких важных для пациента показателей, как сохранение органа и его функции, повышение качества жизни на фоне увеличения ее продолжительности.
1 The GEC ESTRO Handbook of Brachytherapy, 2002.
2 A Breakthrough In Prostate Cancer Treatment. Copyright 2006 Dr.Panos G. Koutrouvelis.
Published by URO-Radiology Prostate Institute URPI Press. ISBN 0-9776964-0-5
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.
Радионуклидная диагностика
Радионуклидная (радиоизотопная) диагностика является составной частью современной лучевой диагностики и предназначена для выявления патологических процессов в организме с помощью радиофармацевтических препаратов (РФП). Это метод функциональной визуализации, позволяющий качественно и количественно оценить наличие функционирующей ткани в исследуемом органе.
Радиофармацевтический препарат — это разрешенное для введения человеку с диагностической целью химическое соединение, в молекуле которого содержится радионуклид.
Сцинтиграфия — основной способ радионуклидной визуализации в современной клинике. Сцинтиграфия позволяет выявлять патологический процесс на ранних стадиях заболевания, т. е. до того момента, как болезнь успела себя проявить.
При проведении сцинтиграфии пациенту внутривенно вводится небольшое количество вещества с радиоактивной меткой (РФП), которое накапливается в исследуемом органе. Накопление регистрируется специальным чувствительным прибором — гамма-камерой. Вводимое вещество практически безопасно для пациента, не вызывает аллергические реакции и быстро выводится из организма.
В зависимости от вида исследования процедура занимает от 30 минут до 4 часов. Это необходимо для того, чтобы введенное вещество распределилось в теле человека.
В Брянском областном онкологическом диспансере отделение функционирует с 1975 года, но в октябре 1996 года приказом департамента здравоохранения Брянской области радиоизотопная служба была переведена в Брянский клинико-диагностический центр. В июне 2013 года было принято решение вновь открыть отделение радионуклидной диагностики в БООД. Отделение располагает многофункциональной комбинированной системой однофотонной эмиссионной компьютерной томографии и рентгеновской компьютерной томографии (ОФЭКТ/КТ) «Discovery NM/CT-670» корпорации General Electric. Коллектив отделения успешно проводит такие исследования как остеосцинтиграфия, ОФЭКТ/КТ костей, сцинтиграфия печени и селезёнки, ОФЭКТ печени с меченными эритроцитами, ангионефросцинтиграфия, сцинтиграфия щитовидной железы (99mTc). Проводятся исследования у пациентов как онкологического, так и эндокринологического, урологического и кардиологического профилей.
Аппаратное оснащение отделения позволяет неинвазивно исследовать органы и ткани человека с применением незначительных доз РФП, быстро покидающих организм после исследования, что обеспечивает минимальное облучение пациента и отсутствие побочных эффектов. С учетом биологического выведения препарата лучевые нагрузки на пациента невелики и в большинстве исследований не превышают облучение при флюорографии.
Основные задачи радионуклидной диагностики при исследовании онкологических больных:
В отделении для пациентов созданы комфортные условия пребывания, благоприятная и доброжелательная атмосфера поддерживается слаженной работой не только врачей, но и среднего медицинского персонала.
Коллектив отделения: зав.отделения, врач-радиолог высшей квалификационной категории Старченкова О. Ю., врач-радиолог Скугорева А. А., старшая м/с высшей квалификационной категории Леквеишвили Г. Ю., м/с Ставер О. В., м/с Царькова Н. М.
При явке на исследование при себе надо иметь: направление; паспорт; СНИЛС; полис ОМС или ДМС; (при наличии) результаты проведенных ранее лучевых исследований (УЗИ, КТ, МРТ, ПЭТ/КТ, ОФЭКТ, анализы крови и т.д.); медицинскую документацию (заключения специалистов, выписки из истории болезни, амбулаторные карты и т.д.).
При отсутствии указанных выше документов интерпретация данных сцинтиграфии может быть неполной.
Запись по телефону: +7 (4832) 78-04-52
ВАЖНО! Отказ от запланированного исследования должен быть сделан не позднее, чем за 24 часа до исследования.
Радионуклидная терапия Lu-PSMA у больных раком предстательной железы
Вторник, 29 Июнь 2021
В клинике ядерной медицины начато применение нового для отечественной клинической практике метода лечения больных раком предстательной железы с помощью Лютеция-177-ПСМА.
Этот метод заключается в ведении радионуклида для внутреннего, сверхнаправленного облучения метастазов, который оседает внутри них за счет сродства к поверхности опухоли (а не за счет простого оседания в костной ткани, как например Ксофиго и ему подобные).
Такое свойство Лютеция-PSMA cущественно меняет как эффективность лечения, так и его переносимость по сравнению с существующими методиками у больных с кастрационной резистентностью (нечувствительностью к гормональной терапии).
Кому показана радионуклидная терапия?
несомненным показанием для терапии Lu-177-PSMA является гормонорезистентный рак предстательной железы (кастрационнная резистентность) при наличии прогрессирования на фоне лекарственного лечения;
уточняющим методом прогнозирования эффективности лечения Лютецием-177 PSMA является сцинтиграфия с GA-67 или F-18-PSMA (тераностика).
Как проводится радионуклидная терапия Lu-PSMA в РНЦРР?
первичная консультация для определения показаний к радионуклидной терапии проводится в кабинете 723 радиологического корпуса по средам с 10 до 12 часов;
при наличии показаний для лечения, а также возможности включения в тот или иной протокол клинического наблюдения пациент госпитализируется в отделение радионуклидной терапии, дата госпитализации сообщается по окончании первичной консультации;
с ограничениями при нахождении на закрытом режиме подробно можно ознакомиться на сайте Центра и в памятке пациента;
в день госпитализации радиофармпрепарат вводится внутиривенно с использованием инфузомата. Далее за пациентом проводится наблюдение, с использованием видеосвязи;
через двое суток выполняется контрольная дозиметрия, при мощности излучения от тела менее предельно допустимой пациент выписывается из закрытого стационара.
Возможные осложнения: типичными осложнениями является тошнота, редко – рвота, сухость во рту в ближайшие часы после введения радиофармпрепарата. Также возможно временное ухудшение показателей кроветворения.
Преимущества радионуклидной терапии Lu-PSMA перед другими методами лечения больных с метастазами кастрационно-резистентного рака предстательной железы:
Лекарственное противоопухолевое лечение: (докситаксел, кабазитаксел), Ингибиторы синтеза андрогенов, блокаторы андрогенных рецепторов (абиратерон, энзалутамид). Увеличение общей выживаемости при проведении радионуклидной терапии лютецием- ПСМА в 1,3 раза, нежелательные явления нетяжелы, и возникают в 6,3 раза реже*. В то же время, поскольку применение Lu-PSMA в России только начинается, показания для его применения временно сужены до случаев прогрессирования заболевания на фоне фармакотерапии.
Дистанционная лучевая терапия: в отличие от наружного облучения, при лечении радиоактивным лютецием нет ограничения по количеству облучаемых метастазов и возможно многократное применение. Здоровые ткани практически не облучаются (около 1 мм вокруг опухоли), что практически не приводит к классическим лучевым реакциям.
*Parker C, Nilsson S, Heinrich D, et al. Alpha emitter radium-223 and survival in metastatic prostate cancer. N Engl J Med 2013;369:213-23;
*Morris M.J. et al. Phase 3 study of lutetium-177-PSMA-617 in patients with metastatic castration-resistant prostate cancer (VISION). J Clin Oncol. 2021,39:(suppl 15; abstr LBA4); DOI:10.1200/JCO.2021.39.15_suppl.LBA4
**Heidenreich A. et al. Safety of cabazitaxel in senior adults with metastatic castration-resistant prostate cancer: results of the European compassionate-use programme // Eur J Cancer. 2014. Vol. 50(6). Р. 1090–1099.
**Morris M.J. et al. Phase 3 study of lutetium-177-PSMA-617 in patients with metastatic castration-resistant prostate cancer (VISION). J Clin Oncol. 2021,39:(suppl 15; abstr LBA4); DOI:10.1200/JCO.2021.39.15_suppl.LB
Fon Eyben FE, Roviello G, Kiljunen T, Uprimny C, Virgolini I, Kairemo K, Joensuu T. Third-line treatment and 177LuPSMA radioligand therapy of metastatic castrationresistant prostate cancer: a systematic review. Eur J Nucl Med Mol Imaging. 2018;45(3):496-508. doi: 10.1007/ s00259-017-3895-x