Рефлекс гофмана что это
Гоффмана рефлекс
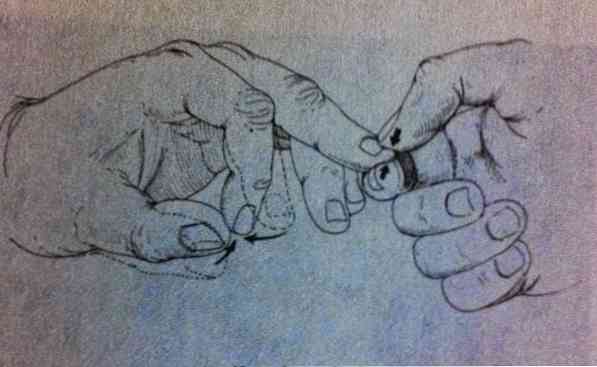
Один из кистевых патологических рефлексов. Методика вызывания: предплечье больного находится в среднем положении между супинацией и пронацией. Исследующий захватывает дистальную фалангу среднего (или – указательного, безымянного) пальца кисти больного своими пальцами между ногтём большого и дистальной фалангой указательного пальцев и производит быстрое соскальзывающее движение. В ответ на это отмечается отрывистое сгибание дистальной или всех фаланг II-V пальцев кисти, а также сгибание и приведение большого пальца кисти.
Методика вызывания рефлекса Гоффмана (источник: http://endeavor.med.nyu.edu/neurosurgery/hoffman.jpg)
Возможен альтернативный вариант вызывания рефлекса Гоффмана: отрывистый щелчок по ногтевой фаланге среднего пальца больного (см. рисунок ниже).
Другой способ вызывания рефлекса Гоффмана (источник: Light R.R. Outline of the screening neurological exam. – http://medicine.tamu.edu/neuro/78.gif)
Эпонимическое название рефлекса связано с именем немецкого невролога Иоганна Гоффмана, который описывал его в своих лекциях и широко применял на практике, однако, нигде не упоминал его в своих публикациях. Рефлекс описан его учеником, немецким неврологом Гансом Куршманном в 1911г. (Curschmann H. Über die diagnostische Bedeutung des Babinskischen Phänomen im präurämischen Zustand // Münchener medizinische Wochenschrift, 1911, 58: 2054).
Амиотрофия Верднига-Гоффмана — это наиболее злокачественная спинальная мышечная атрофия, развивающаяся с рождения или в первые 1-1,5 года жизни ребенка. Характеризуется нарастающими диффузными мышечными атрофиями, сопровождающимися вялыми парезами, прогрессирующими до полной плегии. Как правило, амиотрофия Верднига-Гоффмана сочетается с костными деформациями и врожденными аномалиями развития. Диагностическую основу составляет анамнез, неврологический осмотр, электрофизиологические и томографические исследования, анализ ДНК и изучение морфологического строения мышечной ткани. Лечение слабо эффективно, направлено на оптимизацию трофики нервной и мышечной тканей.
МКБ-10
Общие сведения
Амиотрофия Верднига-Гоффмана является самым тяжелым вариантом из всех спинальных мышечных атрофий (СМА). Ее распространенность находится на уровне 1 случай на 6-10 тыс. новорожденных. Заболевание имеет несколько форм: врожденную, промежуточную (раннюю детскую) и позднюю. Целый ряд специалистов выделяет последнюю форму как самостоятельную нозологию — амиотрофию Кугельберга-Веландера. Отсутствие этиотропного и патогенетического лечения, ранний летальный исход ставят курирование пациентов с болезнью Верднига-Гоффмана в ряд наиболее сложных задач, стоящих перед современной неврологией и педиатрией.
Причины
Амиотрофия Верднига-Гоффмана — наследственная патология, кодируемая поломкой в генетическом аппарате на уровне локуса 5q13 5-й хромосомы. Ген, в котором происходят мутации, получил название survival motor neuron gene (SMN) — ген, ответственный за выживание мотонейронов. У 95% пациентов с болезнью Верднига-Гоффмана отмечается делеция теломерной копии этого гена. Тяжесть СМА прямо коррелирует с протяженностью участка делеции и сопутствующим наличием изменений (рекомбинации) в генах H4F5, NAIP, GTF2H2.
Носителем измененного гена, обуславливающего возникновение заболевания, является каждый 50-й человек. Но благодаря аутосомно-рецессивному типу наследования, патология у ребенка проявляется только тогда, когда соответствующая генетическая аберрация имеется и у матери, и у отца. Вероятность рождения ребенка с патологией в такой ситуации составляет 25%.
Патогенез
Результатом аберрации SMN-гена является недоразвитие мотонейронов спинного мозга, локализующихся в его передних рогах. Следствием становится недостаточная иннервация мышц, приводящая к их выраженной атрофии с потерей мышечной силы и прогрессирующим угасанием способности совершать активные двигательные акты. Основную опасность представляет слабость мышц грудной клетки, без участия которых невозможны движения, обеспечивающие дыхательную функцию. При этом сенсорная сфера на всем протяжении заболевания остается интактной.
Симптомы амиотрофии
Врожденная форма
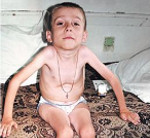
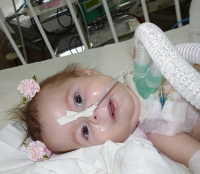
СМА I клинически манифестирует до 6-месячного возраста. Внутриутробно может проявляться вялым шевелением плода. Зачастую мышечная гипотония отмечается с первых дней жизни и сопровождается угасанием глубоких рефлексов. Дети слабо кричат, плохо сосут, не могут держать голову. В отдельных случаях (при более позднем дебюте симптомов) ребенок учится держать голову и даже сидеть, но на фоне развития заболевания эти навыки быстро исчезают. Характерны ранние бульбарные нарушения, понижение глоточного рефлекса, фасцикулярные подергивания языка.
Данная амиотрофия Верднига-Гоффмана сочетается с олигофренией и нарушениями формирования костно-суставного аппарата: деформациями грудной клетки (воронкообразной и килевидной грудной клеткой), искривлением позвоночника (сколиозом), контрактурами суставов. У многих пациентов выявляются другие врожденные аномалии: гемангиомы, гидроцефалия, косолапость, дисплазия тазобедренных суставов, крипторхизм и пр.
Течение СМА I наиболее злокачественное с быстро нарастающей обездвиженностью и парезом дыхательной мускулатуры. Последний обуславливает развитие и прогрессирование дыхательной недостаточности, выступающей основной причиной летального исхода. В связи с нарушением глотания возможен заброс пищи в дыхательные пути с развитием аспирационной пневмонии, которая может явиться смертельно опасным осложнением спинальной амиотрофии.
Ранняя детская форма
СМА II дебютирует после 6-месячного возраста. К этому периоду дети имеют удовлетворительное физическое и нервно-психическое развитие, в соответствии с возрастными нормами приобретают навыки держать голову, переворачиваться, садиться, стоять. Но в подавляющем большинстве клинических случаев дети так и не успевают научиться ходить. Обычно эта амиотрофия Верднига-Гоффмана манифестирует после перенесенной ребенком пищевой токсикоинфекции или другого острого инфекционного заболевания.
В начальном периоде периферические парезы возникают в нижних конечностях. Затем они достаточно быстро распространяются на верхние конечности и мускулатуру туловища. Развивается диффузная мышечная гипотония, происходит угасание глубоких рефлексов. Наблюдаются контрактуры сухожилий, тремор пальцев, непроизвольные мышечные сокращения (фасцикуляции) языка. На поздних стадиях присоединяются бульбарные симптомы, прогрессирующая дыхательная недостаточность. Течение более медленное, чем у врожденной формы болезни Верднига-Гоффмана. Пациенты могут доживать до 15-летнего возраста.
Амиотрофия Кугельберга-Веландера
Диагностика
Больные спинальной мышечной атрофией I типа находятся под наблюдением детских неврологов и неонатологов. Большое значение имеет возраст манифестации заболевания – для амиотрофии Верднига-Гоффмана характерно развитие с момента рождения до 6 месяцев. В анамнезе часто имеются сведения о позднем и вялом шевелении плода во время беременности.
При осмотре ребенка обращается внимание на выраженную мышечную гипотонию, неспособность самостоятельно сидеть или удерживать голову, типичную «позу лягушки» – плечи приподняты, руки вдоль туловища, ноги выпрямлены и повернуты кнаружи. Отмечаются мышечные подергивания, ослабление или отсутствие сухожильных рефлексов, грубые костные деформации (колоколообразная грудная клетка, Х-образные нижние конечности). Для подтверждения диагноза назначаются следующие дополнительные исследования:
Амиотрофию Верднига-Гоффмана следует дифференцировать с другими генетически обусловленными нервно-мышечными заболеваниями, имеющими такое же быстропрогрессирующее течение. К ним относятся врожденные структурные миопатии, ювенильный боковой амиотрофический склероз, синдром Фукуямы.
Лечение амиотрофии Верднига-Гоффмана
Немедикаментозная терапия
Для прохождения лечения все больные подлежат обязательной госпитализации в стационар. В тяжелых ситуациях (например, при выраженной гипоксемии вследствие слабости дыхательных мышц) пациентов переводят в отделение реанимации и интенсивной терапии и подключают к аппарату ИВЛ. На сегодняшний день не существует этиотропной терапии амиотрофии Верднига-Гоффмана. Все мероприятия носят симптоматический и паллиативный характер. Применяются следующие методы лечения:
Медикаментозная терапия
Для достижения максимального эффекта лечение должно быть комплексным, проводиться непрерывно и подбираться индивидуально для конкретного пациента. Лекарственные препараты, применяющие для лечения амиотрофии Верднига-Гоффмана следующие:
Хирургическое лечение
При развитии грубых деформаций грудной клетки и позвоночника или крайне выраженных контрактур суставов показаны ортопедические операции. У лежачих больных, страдающих постоянно рецидивирующими пневмониями, выполняется трахеостомия. При гастроэзофагеальном рефлюксе, резистентном к медикаментозному лечению, прибегают к лапароскопической фундопликации Ниссена.
Новейшие разработки
Ведутся постоянные исследовательские работы по поиску эффективного лекарства для терапии спинальной мышечной атрофии. Наиболее перспективным направлением считается генная терапия. В клинической практике уже используются антисмысловые олигонуклеотиды, исправляющие дефекты матричной РНК в гене SMN2 (Спинраза).
В конце 2019 года был зарегистрирован и одобрен к клиническому применению препарат Золгенсма, который содержит функционально полноценный ген SMN1. Доставка этого гена в нервные клетки производится с помощью аденоассоциированного вируса, проникающего через гематоэнцефалический барьер. Использование Золгенсмы приводит к значительному увеличению продукции белка SMN1 и улучшению состояния пациентов.
Прогноз
Врожденная амиотрофия Верднига-Гоффмана имеет крайне неблагоприятный прогноз. При ее манифестации в первые дни жизни ребенка, его гибель, как правило, происходит до 6-месячного возраста. При начале клиники после 3-х месяцев жизни, летальный исход наступает в среднем к возрасту 2 года, иногда — к 7-8 годам. Ранняя детская форма характеризуется более замедленным прогрессированием, дети погибают в возрасте 14-15 лет.
Профилактика
Первичная профилактика амиотрофии Верднига-Гоффмана заключается в пренатальной диагностике. При обнаружении в биоптатах ворсин хориона или амниотической жидкости мутации SMN1 показано прерывание беременности. Вторичная профилактика сводится к предупреждению осложнений – аспирационной пневмонии, контрактур суставов, инфекций нижних дыхательных путей.
Знак Хоффмана Как вы получаете и что это значит
знак Гофмана это ненормальный рефлекторный ответ, который заключается в сгибании пальцев кисти при нажатии на ноготь среднего пальца.
Хотя это обычно связано с патологиями, такими как пирамидный синдром, оно может встречаться у здоровых людей с возвышенными рефлексами (так называемая гиперрефлексия). Видимо этот знак обычно указывает на некоторые повреждения спинного мозга или головного мозга.
Неврологическое клиническое обследование имело большое значение в прошлом, когда технологических разработок современной медицины не существовало. В нем проверялись рефлексы для наблюдения за состоянием здоровья человека.
Однако в настоящее время при использовании методов нейровизуализации эти тесты имеют меньший вес при принятии клинических решений..
Описание рефлекса Бабинского или подошвенного рефлекса в 1896 году побудило неврологов искать другие типы рефлексов. Анатомической областью, в которой рефлексы были наиболее исследованы, были нижние конечности.
Аномальные рефлексы в верхних конечностях были менее постоянными, более трудными для получения и с меньшей диагностической значимостью. Хотя признак Гофмана использовался более ста лет для выявления патологий.
Его название происходит от немецкого невролога Иоганна Хоффмана (1857-1919), который открыл его в конце 19-го века. Тем не менее, кто впервые написал об этом знаке, был его помощник Curschmann в 1911 году.
Признаки Хоффмана и Тромнера являются наиболее часто используемыми клинически по отношению к верхним конечностям, чтобы указать на проблемы в кортикально-спинальном тракте..
Рефлекс Хоффмана иногда ошибочно называют «рефлексом Бабинского верхней конечности». Однако они имеют разные рефлексы и их не следует путать.
Знак Хоффмана также известен как цифровой рефлекс и использовался в качестве теста на заболевание кортикально-спинального тракта пирамидного пути..
Наличие этого рефлекса может указывать на вовлечение верхних двигательных нейронов, которые составляют пирамидный путь. Эти нейроны ответственны за произвольные движения верхних конечностей..
При поражении, в дополнение к признаку Хоффмана, они вызывают другие симптомы, такие как гипертония (повышение мышечного тонуса), слабость, гиперрефлексия, ритмичные и непроизвольные сокращения мышц или затруднения в совершении точных движений руками..
Как вы получаете знак Хоффмана?
Чтобы получить знак Хоффмана, расслабленную руку пациента берут с согнутым запястьем и частично согнутым средним пальцем. Экзаменатор будет держать средний палец пациента, поместив его между указательным и средним пальцами.
Он сделает сильное движение, когда большой палец ударит или ущипнет ноготь среднего пальца пациента. Однако это также можно наблюдать, ударяя ноготь указательного или безымянного пальца..
Сказано, что признак Хоффмана присутствует, если есть отведение большого пальца и сгибание указательного пальца. Иногда также происходит сгибание оставшихся пальцев.
Кроме того, было отмечено, что сгибание или расширение шеи может ухудшить этот признак в некоторых случаях.
На что указывает знак Хоффмана??
Признак Хоффмана указывает на повреждение кортикально-спинного тракта пирамидного тракта. Это набор нервных волокон, которые перемещаются от коры головного мозга к спинному мозгу. Его функция заключается в передаче нервных импульсов для выполнения произвольных движений.
Эти повреждения могут быть двусторонними или односторонними. Когда происходит одностороннее повреждение, поражается сторона тела, противоположная той, где находится травма. Таким образом, этот знак может быть представлен в одной руке или в обеих, в зависимости от того, является ли он односторонним или двусторонним.
Признак Хоффмана указывает на наличие гиперрефлексии. Он сопровождает различные состояния, такие как гипертиреоз, некоторые виды тревоги и другие состояния, связанные с глубокими сухожильными рефлексами..
Гиперрефлексия из-за гипертиреоза обычно дает двусторонние результаты. В то время как структурное повреждение мозга, такого как опухоль, приведет к одностороннему рефлексу.
Этот признак также используется для оценки заболеваний шейного отдела позвоночника. По сравнению со знаком Бабинского знак Хоффмана более распространен у пациентов, которых лечили миелопатиями хирургическим путем..
По-видимому, признак Хоффмана также может быть показателем рассеянного склероза. Наблюдается, когда были поражения нервных двигательных путей или спинного мозга в части нервов, которые контролируют движения рук (например, C5).
У пациентов с заболеванием поясничного отдела позвоночника, но без симптомов, связанных с шейным отделом позвоночника, этот признак является показателем скрытой компрессии в шейном отделе позвоночника..
Однако в исследовании Glaser, Cura, Bailey and Morrow (2001), в котором были проанализированы 165 пациентов с компрессией шейного отдела спинного мозга, сделан вывод о том, что тест Хоффмана не является надежным инструментом для прогнозирования этого состояния..
Так как они наблюдали значительную частоту существования знака Хоффмана у здоровых людей, в то время как они обнаружили пациентов с сдавлением костного мозга, которые не имели этого признака.
С другой стороны, в исследовании Sung and Wang (2001) были изучены бессимптомные пациенты с признаком Хоффмана. Рентген шейки матки и магнитные резонансы были сделаны для 16 пациентов.
Магнитный резонанс отражал патологии у всех пациентов. У 14 из них был спондилез шейки матки. 15 имели сдавление пуповины грыжей пульпозного ядра. В то время как у одного из них был грыжа межпозвоночного диска в T5-T6, с последующим сжатием.
Важно отметить, что признак Гофмана не всегда указывает на наличие патологии пирамидального пути. Иногда это наблюдается у людей с «живыми» рефлексами, например у тех, кто страдает от тревоги или находится под воздействием стимулирующих веществ..
Однако, когда этот признак сопровождается другими патологическими рефлексами или ненормальными симптомами, это означает некоторое заболевание нервной системы..
Основы патофизиологии кашля. Глава 1
Кашель возникает при раздражении афферентных сенсорных интраэпителиальных рецепторов блуждающего нерва.
Кашель – это защитный рефлекс, который способствует выведению избыточного секрета и инородных частиц из верхних и нижних отделов дыхательных путей.
Кашель возникает при раздражении афферентных сенсорных интраэпителиальных рецепторов блуждающего нерва. Афферентные веточки блуждающего нерва находятся в глотке, гортани, трахее, бронхах, легких и обусловливают респираторные причины кашля. Кашель может быть связан с раздражением рецепторов блуждающего нерва, которые располагаются в пищеводе и желудке, плевре, перикарде или в других органах, например, ушном проходе («ушной кашель»), в матке («маточный кашель»).
Выделяют следующие основные группы кашлевых рецепторов: быстро адаптирующиеся, или ирритантные (Aδ рецепторы), и рецепторы немиелинизированных бронхиальных С-волокон (С-рецепторы).
Медленноадаптирующиеся рецепторы локализованы в эпителии воздухоносных путей и являются окончаниями нервов гладких мышц бронхов. Они cтимулируются при бронхоспазме, застое в легких, легочной эмболии. Афферентные импульсы с чувствительных окончаний при участии сенсорных нейропептидов передаются в кашлевой центр, локализованный в ядре солитарного тракта (nucleus tractus solitarius) продолговатого мозга, который сообщается с центральным генератором дыхания. Интеграция этой информации инициирует моторные команды по эфферентным путям к респираторной мускулатуре.
Рис. 1. Проводящие пути, участвующие в формировании кашлевой реакции.
Рис. 2. Физиология кашля.
Кашлю предшествует тягостное, неприятное ощущения позыва к кашлю (urge-to-cough), сопровождаемое чувством першения в горле, что согласуется с понятием сенсорной нейрональной дисфункции афферентных веточек блуждающего нерва. Большинство пациентов описывают ассоциированные с кашлевым позывом ощущения как першение в горле, щекотание, зуд, жжение, боль.
Таблица. Триггеры кашля
| Простуда Холодный воздух Разговор Курение/запах дыма Запах плесени Усталость/стресс Специи, такие как карри или чили Постназальный затек (носовые выделения стекают по горлу) Физические нагрузки Зуд в горле | Питание Алкоголь Изжога Влажность Сухой воздух Изменения положения тела, особенно лежа Контакт с домашними животными Пыльца |
Механизм кашля включает 3 фазы: инспираторную, компрессионную и экспираторную.
Инспираторная фаза. Ей предшествует кашлевое раздражение, характеризующееся субъективным чувством «трахеобронхиального зуда», за которым следует ощущение в необходимости кашля. Во время рефлекторного открытия голосовой щели происходит глубокий форсированный вдох с участием всех инспираторных мышц. Объем вдыхаемого воздуха может варьировать от 50% дыхательного объема до 50% жизненной емкости легких (ЖЕЛ). Длительность этой фазы около 2 с.
Компрессионная фаза. Рефлекторно закрываются верхние дыхательные пути – голосовые связки и голосовая щель. Затем происходит резкое сокращение экспираторных мышц – внутренних межреберных и брюшных. Фаза характеризуется быстрым повышением внутригрудного и внутрибрюшного давления приблизительно на 0,5 с. Для эффективного откашливания необходимо повышение внутригрудного давления минимум до 40 мм рт. ст.
Экспираторная фаза. Приблизительно через 0,2 с после завершения периода компрессии голосовая щель рефлекторно открывается, создается перепад давления, и турбулентный поток воздуха резко выбрасывается из дыхательных путей, увлекая за собой содержимое бронхов. Отмечается серия форсированных экспираторных маневров. Движение воздуха приводит к вибрации (флаттеру) вокальных хорд, стенок гортани, трахеи, что создает характерные кашлевые звуки («лающий», резонирующий, битональный, глухой и др.). Объемная скорость воздушного потока достигает 12 л/с, а внутригрудное давление может достигать 300 мм рт. ст., генерируется до 25 Дж энергии. Резкое повышение внутригрудного давления в эту фазу кашля может привести к различным осложнениям.
Рис. 3. Изменение давления в дыхательных путях на разных фазах кашля.
Причины и диагностика спинальной мышечной атрофии (СМА)
Отмирание моторных нейронов приводит к прогрессивному развитию слабости мышц, их атрофии, и в итоге, обездвиживанию пациента. Спинальная мышечная атрофия делится на несколько типов, в зависимости от того, насколько серьезны симптомы и в каком возрасте они начались:
Частота и тип наследования СМА
Спинальная мышечная атрофия встречается у 1 из 6000 — 10 000, с частотой носительства 1 из 38 человек. Больной ребенок рождается, при наличии двух мутаций, со стороны матери и со стороны отца. Родители, являющиеся носителями мутации в гене SMN1, не имеют клинических симптомов. Спинальная мышечная атрофия наследуется по аутосомно-рецессивному типу:
Есть и другие гены (например ATP7A и др.), поломки в которых приводят к развитию СМА. Поэтому возможны и другие типы наследования (доминантный/X-сцепленный) и, соответственно, другие риски.
Причина заболевания и патогенез СМА
Тяжесть течения болезни модифицируется вторым геном SMN2. Он очень похож на ген SMN1, но отличается последовательностью нуклеотидов в 7 и 8 экзонах. Ген SMN2 не способен продуцировать функциональный белок SMN в достаточном количестве, однако количество копий SMN2, а также последовательность этих копий влияют на фенотип. Поэтому важно получить информацию о количестве копий генов SMN1и SMN2, не только у пациента с признаками СМА, но и у пар, планирующих беременность.
Скрининг новорожденных на СМА
Хотя скрининг новорожденных еще не является стандартной практикой, время имеет решающее значение. Более ранняя диагностика СМА может помочь улучшить исходы для детей с атрофией дыхательных и скелетных мышц.



.png)
.png)
.png)
.png)

