Риск втэо что это
ВЕНОЗНЫЕ ТРОМБОЭМБОЛИЧЕСКИЕ ОСЛОЖНЕНИЯ: КТО ВИНОВАТ И ЧТО ДЕЛАТЬ?
Венозные тромбоэмболические осложнения, к которым относятся: тромбоз глубоких вен, тромбоз подкожных вен, тромбофлебит и тромбоэмболия легочных артерий, на протяжении длительного времени являются важнейшей клинической проблемой.
По статистике, около 100 тысяч пациентов в РФ ежегодно погибают от внезапной тромбоэмболии легочной артерии. Тромбоэмболия представлена тромбами, образующимися в просвете сосудов и разносящимися с потоком крови по организму. Чаще всего тромбы образуются в просвете вен нижних конечностей, а затем попадают в правую половину сердца и далее в артерии лёгких.
Механизм прижизненного образования тромбов внутри сосудов описывается триадой, открытой в 1856 году немецким морфологом Рудольфом Вирховым, которая включает в себя повреждение сосудистой стенки, замедление кровотока и повышение вязкости (свертывающей способности) крови.
Наиболее значимыми факторами для возникновения венозного тромбоза является гемодинамические нарушения (замедление кровотока) и гиперкоагуляция (повышенная свертываемость крови).
Вероятность венозного тромбоза увеличивается, в случае если у человека имеется врожденная или приобретенная тромбофилия, т.е. состояние, характеризующееся склонностью к тромбообразованию. С наличием тромбофилии могут быть связаны многие случаи “неожиданного” венозного тромбоза и легочной тромбоэмболии (в частности, возникающие у лиц молодого возраста, не имеющих серьезных клинических факторов риска). Инициировать тромбоз у пациентов с тромбофилией могут оперативные вмешательства, травмы, беременность и роды, т.е. те состояния, которые сопровождаются повреждением тканей, изменением тонуса сосудов, гормонального фона.
Поставить правильный диагноз, установить причину тромбоэмболических осложнений, определить тактику ведения после случившегося тромбоза или назначить тромбопрофилактику при имеющихся факторах риска, оценить риск тромботических событий перед началом приёма гормональной терапии, планируемых оперативных вмешательствах, сможет только специалист.
В ГАУ РО ОКДЦ работают врачи-гематологи, терапевты-гемостазиологи, прошедшие специальную подготовку по патологии свертывающей системы крови, в распоряжении которых имеется современная высококачественная лабораторная диагностика. Врачи центра патологии гемостаза могут определить тактику ведения пациента; подобрать соответствующую терапию; снизить риск возможных осложнений; определить необходимость лабораторного контроля эффективности терапии.
Специалисты Центра патологии гемостаза в ГАУ РО ОКДЦ помогут Вам, своевременно распознать нарушения в системе гемостаза и при необходимости подберут эффективное лечение, подходящее в каждом конкретном случае.
Татьяна Николаевна Абрамова,
врач-терапевт- гемостазиолог высшей категории.
Венозные тромбоэмболические осложнения: смена парадигмы в профилактике и лечении
Обзор симпозиума «ВТЭО: где мы сегодня и куда движемся?», прошедшего в рамках XIII Съезда хирургов России 8-10 сентября 2021.
Самая насущная тема последнего года – Covid – не прошла стороной и XIII Съезд хирургов России. Известно, что коронавирусная инфекция является причиной тяжелой гипоксемии и респираторного дистресс-синдрома, что приводит к развитию коагулопатии и формированию тромбоза в артериях и венах мелкого калибра. Кроме того, Covid-19 увеличивает риск развития тяжелых осложнений со стороны сердечно-сосудистой системы. Среди таких пациентов также регистрируется высокая частота венозных тромбоэмболических осложнений (ВТЭО) с преобладанием случаев легочной эмболии. Эта тема была подробно представлена в рамках сателлитного симпозиума «ВТЭО: где мы сегодня и куда движемся?» на первом докладе Кириенко А.И., д.м.н., профессора кафедры факультетской хирургии РНИМУ им. Пирогова и Почетного президента Ассоциации флебологов России (АФР).
Профессор Кириенко сформулировал шесть вопросов, ответы на которые необходимо знать для правильного ведения пациентов с ВТЭО и Covid-19: целесообразность профилактики, необходимость применения антикоагулянтов, а также принципы выбора препарата, дозы, способа контроля и длительности терапии. Рекомендации Минздрава способны дать ответ лишь на некоторые из этих вопросов: всем госпитализированным пациентам с Covid, не имеющим противопоказаний, а также амбулаторным пациентам с высоким риском тромбоза, должны назначаться низкомолекулярные гепарины (НМГ); особые показания перечислены к применению фондапаринукса – это низкий уровень тромбоцитов и иммунная тромбоцитопения. Место пероральных антикоагулянтов (ПОАК) прежде всего представлено продленной профилактикой ВТЭО после выписки пациента, однако при неприемлемых лекарственных взаимодействиях, а также при тяжелой форме Covid, рекомендуется переход на лечебные дозы НМГ. К ограничениям такой терапии стоит отнести необходимость парентерального введения и подбора дозы, сложность в самостоятельном использовании, риск развития гепарин-индуцированной тромбоцитопении и стоимость лечения, которая на порядок превышает таковую у ПОАК и на несколько порядков в сравнении с варфарином, который, однако, не избавлен от ряда других сложностей, характерных для НМГ.
Следующей частью симпозиума стал доклад Сокуренко Г.Ю., д.м.н., главного врача клиники №2 Всероссийского центра экстренной и радиационной медицины им. Никифорова. Свое выступление Герман Юрьевич начал с напоминания о роли антикоагулянтной терапии в общих масштабах здравоохранения – со времен появления гепарина в начале XX века антикоагулянты спасли миллионы жизней, но в то же время они принадлежат к одной из наиболее опасных групп препаратов, по степени потенциального вреда уступая лишь химиотерапевтическим средствам, используемым в онкологии. Один из наиболее известных ангиологов, итальянский профессор Андреосси, рассуждая о соотношении пользы и риска при длительной антикоагулянтной терапии, постулировал, что эта польза частично нивелируется повышением риска значимых кровотечений, а также указывал, что риск ретромбоза возрастает после отмены антикоагулянтов, при этом пролонгация терапии свыше рекомендованных сроков лишь оттягивает наступление этого явления без снижения его риска после прекращения терапии. Это обуславливает важное значение лабораторного мониторинга, который требуется в том числе на фоне длительного приема ПОАК в виде измерения уровня D-димера, что отражено в одной из классических работ по этой теме Palareti et al., опубликованной в New England Journal of Medicine в 2006 году. Эти данные легли в основу как национальных, так и международных рекомендаций, в частности рекомендаций ACCP (American College of Chest Physicians) 2016 года.
Все представители группы ПОАК, ознаменовавшие новую эру антикоагулянтной терапии, показали свою эффективность и безопасность в целом ряде исследований, посвященных изучению как острой фазы, так и пролонгированному применению. В частности, результаты исследования AMPLIFY продемонстрировали схожий профиль эффективности апиксабана в сравнении с традиционной схемой лечения эноксапарин/варфарин при существенной разнице в безопасности: в группе апиксабана риск больших и клинически значимых кровотечений был на 58% ниже. В рамках исследования AMPLIFY-EXT также было изучено продлённое лечение препаратом, причем сразу в двух различных дозировках апиксабана (2,5 и 5 мг). Обе дозы антикоагулянта обладали сравнимой эффективностью, однако различались по показателям безопасности – апиксабан в дозе 2,5 мг был ассоциирован с меньшей частотой нежелательных событий и практически соответствовал таковой в группе плацебо.
В современных реалиях большое внимание уделяется не только рандомизированным клиническим испытаниям (РКИ), но и так называемым пост-маркетинговым наблюдательным исследованиям – данным реальной клинической практики. Главное различие в этих двух типах работ состоит в том, что в РКИ над пациентами осуществляется более строгий контроль и более тщательное наблюдение. Одно из таких крупных популяционных исследований, результаты которого опубликованы в Journal of Thrombosis and Haemostasis, сравнивало 2 группы пациентов, принимающих апиксабан или НМГ/варфарин. По данным этой работы были практически подтверждены результаты исследования AMPLIFY-EXT, что подчеркивает важную преемственность между РКИ и данными реальной клинической практики. Самый крупный регистр данных Optum Clininformatics Mart, накопленный за период 2003-2019, включает 34201 пациента, принимающих апиксабан, и 46007 пациентов, принимающих ривароксабан. Результаты анализа этого регистра указывают на то, что частота общего количества кровотечений и, в частности, не внутричерепных кровотечений, находится на более низком уровне у апиксабана в сравнении с ривароксабаном, при этом летальные исходы между группами не имели статистически значимой разницы.
О том, как меняются взгляды на лечение ВТЭО в эру ПОАК, а также о новых данных в клинических рекомендациях, рассказал Сучков И.А., д.м.н., профессор, главный внештатный сердечно-сосудистый хирург Рязанской области, Президент АФР.
Рекомендации ACCP разделяют длительность антикоагулянтной терапии на начальный этап (до 7 дней), длительную терапию (до 3 мес) и продленный вариант (который может иметь в том числе неопределенный срок с периодической оценкой пользы/риска). Оценка риска рецидива тромбозов и риска геморрагических осложнений является основной мерой, определяющей как длительность антикоагулянтной терапии, так и дозировку препаратов. При этом среди ПОАК только апиксабан и дабигатран показали снижение риска клинически значимых и больших кровотечений. Один из основных антикоагулянтов, с которым сравниваются ПОАК, варфарин, также обладает высоким терапевтическим потенциалом, однако требует значительной комплаентности ввиду необходимости постоянного контроля МНО, что не всегда соответствует реалиям клинической практики.
До недавнего времени имплантация кава-фильтров считалась золотым стандартом, но в клинических рекомендациях АФР четко отслеживается тенденция по сужению показаний к применению этих устройств. К настоящему времени они представлены лишь одним показанием – при проксимальных тромбозах глубоких вен (ТГВ) при наличии абсолютных противопоказаний к антикоагулянтной терапии. Такая тенденция была связана с осложнениями, ассоциированными с кава-фильтрами: миграция фильтра или его эмболизация, перелом страт и перфорация, синдром нижней полой вены, посттромбофлебитический синдром, ТГВ. Кроме того, непосредственное удаление кава-фильтра также несет за собой существенные риски вторичного тромбоза.
Наиболее актуальный европейский опыт лечения ВТЭО представлен в клинических рекомендациях ESVS 2021 года. В отношении диагностических мероприятий в них указывается, что при неспровоцированных ТГВ показано клиническое и специфичное полу обследование на наличие онкологических новообразований без рутинной подробной диагностики. Это связано с тем, что у таких пациентов удается выявить скрытое онкологическое заболевание только в 10%, в то время как избыточные диагностические мероприятия часто могут приводить к специфическим осложнениям. С определенными сомнениями в рекомендациях ESVS указывается вопрос о целесообразности назначения антикоагулянтной терапии при ТГВ голени. В своем докладе Игорь Александрович отметил, что своевременная терапия может оказаться эффективной как в отношении прогрессирования ТГВ, так и для реканализации вен, при этом длительность такой терапии должна составлять 3 месяца. В лечении тромбофлебита поверхностных вен (ТПВ) акцент сделан на применении профилактических доз фондапаринукса или НМГ в течение 45 дней, что также отражено и в отечественных рекомендациях, утвержденных Минздравом.
Профессор Сучков отметил исследования новых антикоагулянтов, направленных на разработку антагонистов фактора коагуляции XI и XIа, а также фактора XII, находящегося на стадии доклинических исследований. Также в докладе были озвучены основные нерешенные вопросы профилактики и лечения ТГВ, к которым можно отнести неопределенность в потенциальной пользе проведения скрининга на ТЭЛА, а также роль тромболизиса у пациентов с ТГВ, пользе и целесообразности катетерного тромболизиса при илиофеморальном тромбозе из-за неоднозначности выводов исследований CaVenT и ATTRACT, а также лечение дистальных форм ТГВ и ТПВ в контексте использования ПОАК, и, наконец, особенности антикоагулянтной терапии в лечении и профилактике ассоциированных с Covid ВТЭО.
В качестве завершающего доклада Андрияшкин В.В., д.м.н., профессор кафедры факультетской хирургии № 1 РНИМУ им. Пирогова, выступил с представлением новой информации о лечении онкотромбозов. Пациенты этой группы сочетают в себе целый ряд факторов риска, связанных как со злокачественной опухолью, так и с общим состоянием пациента и применяемыми агрессивными методами лечения. Риск развития ВТЭО у этих пациентов по меньшей мере в 6 раз выше по сравнению с другими категориями больных по данным всех имеющихся регистров, а ВТЭО является второй по частоте причиной смерти. Последние тенденции в лечении и профилактике рецидивов ТГВ и ТЭЛА все больше уходят от хирургических методов в пользу консервативных – и даже имеющиеся показания к хирургическому лечению так или иначе связаны с назначением антикоагулянтной терапии.
Принципы ведения онкологических пациентов были заложены в рекомендациях ACCP 2016 года – использование НМГ считалось более предпочтительным в сравнении с антагонистами витамина К и ПОАК. Эти данные основывались на результатах исследования CLOT, в котором две группы пациентов лечили схемой далтепарин/варфарин или только далтепарином, где в последней было продемонстрировано почти двукратное снижение риска ТГВ и ТЭЛА. В то же время терапия НМГ обладает существенными ограничениями: парентеральный путь введения, сложность подбора дозы и высокая стоимость. Альтернатива в виде применения ПОАК еще в 2015 году не рекомендовалась Американским обществом клинической онкологии ввиду недостаточного количества данных и отсутствия антидота. Эта точка зрения была пересмотрена уже через 3 года в рекомендациях NCCN (National Comprehensive Cancer Network), где было указано, что ПОАК являются приемлемой альтернативой терапии НМГ. Впоследствии 15-летний «золотой стандарт» лечения далтепарином был окончательно пересмотрен благодаря целому ряду исследований, посвященных изучению ПОАК – CARAVAGGIO и ADAM (апиксабан), HOKUSAI-VTE (эдоксабан) и SELECT-D (ривароксабан). Среди них по риску больших кровотечений особенно выделяется апиксабан, ставший наиболее предпочтительным ПОАК в контексте профиля безопасности.
Появление ПОАК произвело революцию в области лечения и профилактики рецидивов ВТЭО у самых разных групп пациентов. Последние международные и российские клинические рекомендации все чаще позволяют проводить более персонифицированный выбор метода лечения и профилактики ВТЭО с учетом наиболее актуальных данных об эффективности и безопасности ПОАК.
Служба Медицинской Информации: Medinfo.Russia@Pfizer.com. Доступ к информации о рецептурных препаратах Pfizer в России: www.pfizermedinfo.ru
Copyright 2021 Пфайзер Россия. Все права защищены. Информация предназначена только для специалистов здравоохранения Российской Федерации.
OOO «Пфайзер Инновации»
123112, Москва, Пресненская наб., д.10, БЦ «Башня на Набережной» (блок С), 22 этаж
Тел.: +7 495 287 50 00. Факс: +7 495 287 53 00
Профилактика венозных тромбоэмболических осложнений у госпитальных больных
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
РГМУ имени Н.И. Пирогова
Не будет преувеличением сказать, что в госпитальных отделениях любого профиля без труда можно обнаружить пациентов с ВТЭО. При этом клинически диагностируемые тромбозы и эмболии зачастую представляют лишь видимую «вершину айсберга», поскольку в ряде случаев венозный тромбоз протекает бессимптомно, либо диагностируется уже после выписки больного из стационара, а статистические данные учитывают, в основном, массивную легочную эмболию, приведшую к летальному исходу.
Экономические затраты на диагностику и лечение ВТЭО значительны и имеют стойкую тенденцию к увеличению во всем мире. Кроме того, к ним необходимо приплюсовать материальные и моральные потери от длительного и не всегда успешного лечения хронической венозной недостаточности и постэмболической легочной гипертензии, инвалидизации больных, значительного снижения их социальной активности и уровня качества жизни. Классическое утверждение о том, что любую болезнь легче предупредить, чем лечить, в полной мере относится к венозным тромбозам, учитывая их широкое распространение, возможные тяжелые осложнения, серьезные последствия, экономическую и социальную значимость. Между тем эта аксиома пока не стала руководством к действию для всех врачей по отношению к ВТЭО.
Прежде чем говорить о программе профилактики ВТЭО, целесообразно остановиться на группах риска, т.е. тех пациентах, у которых реальна угроза возникновения тромбоза глубоких вен нижних конечностей. Это же определяет возможность развития эмболии легочных артерий, так как тромбоз в системе нижней полой вены служит основным ее источником.
Многочисленные клинические исследования показали, что опасность ВТЭО особенно велика у пациентов:
• в послеоперационном периоде
• с травматическими повреждениями костей и суставов
• соблюдающих постельный режим
• с генетически обусловленными тромбофилиями
• принимающих гормональные препараты, содержащие эстрогены
• беременных (особенно в III триместре) и рожениц.
В свою очередь, на вероятность развития венозного тромбоза в каждой из групп влияют многие факторы: ожирение, возраст, сопутствующие заболевания, принимаемые лекарственные препараты, приобретенные тромбофилические состояния различного генеза и пр. У оперированных больных огромное значение имеют длительность хирургического вмешательства, его объем и травматичность, локальное сдавление сосудов, вид анестезии, степень ограничения подвижности пациента в послеоперационном периоде.
Планируя профилактические мероприятия, которые подразделяют на физические (механические) и фармакологические, следует предусмотреть использование всех возможностей коррекции факторов, определяющих развитие венозного тромбоза.
В первую очередь это относится к послеоперационным тромбозам. Данные анкетирования, проведенного на IX Всероссийском съезде хирургов (Волгоград, 2000 г.), показали, что тромбоэмболии легочной артерии больше, чем кровотечения, опасаются 73% опрошенных. Вместе с тем оценку риска ВТЭО перед операцией всегда проводят лишь 47% клиницистов. Только 19% хирургов в обязательном порядке используют эластическую компрессию нижних конечностей (доступную меру предупреждения тромбоза). Обычно (73%) применение компрессии ограничивают случаями выраженного варикозного расширения вен. К профилактическому назначению антикоагулянтов при высоком риске тромбоза прибегают 63% хирургов. Весьма отрадный факт, тем более что еще несколько лет назад этот показатель не превышал 15%. Тем не менее, еще многие хирурги относятся к массивной тромбоэмболии легочных артерий, развившейся в послеоперационном периоде, как к фатальной неизбежности, не считая ее «своим» осложнением.
В Российской Федерации ежегодно производят свыше 8 миллионов операций, что дает возможность представить, сколь велика совокупность больных, подвергающихся опасности ВТЭО в связи с хирургическим вмешательством. Очевидно, что не у всех оперируемых больных опасность тромбообразования одинаково высока. Соответственно, и объем профилактических мер требуется различный. Для практических целей оправдано подразделение больных на группы низкого, умеренного и высокого риска ВТЭО, в зависимости от состояния больного и факторов, связанных с хирургической агрессией.
Необходимость профилактических мер существует у всех без исключения больных. Однако их объем должен быть адекватен клинической ситуации и экономически оправдан. Целесообразно соблюдать следующие правила:
• Не следует прибегать к антикоагулянтам при отсутствии показаний (реального риска ВТЭО), учитывая возможные осложнения
• При выборе способа профилактики ВТЭО целесообразно учитывать его стоимость и экономическую оправданность.
Меры профилактики должны быть задействованы уже в предоперационном периоде, продолжаться во время и после операции.
Перед плановой операцией эффективной и доступной мерой является активное поведение больного. На это следует обязательно обращать внимание, т.к. небольшое пространство отделения больницы резко ограничивает подвижность пациента. Целесообразно проведение лечебной физкультуры, использование простых тренажеров, частые прогулки хотя бы по коридору отделения. Больного следует заранее предупредить о крайней важности ранней активации в ближайшем послеоперационном периоде, необходимой в первую очередь для ритмичного сокращения икроножных мышц.
Активное поведение больного способствует ускорению кровотока и предупреждает венозный стаз. Этой же цели служит эластическая компрессия ног: эластические бинты или чулки, оказывающие постепенно снижающее от периферии в проксимальном направлении давление.
В группе низкого риска (не осложненные операции продолжительностью до 45 мин. у сравнительно здоровых пациентов) этих неспецифических профилактических мер у подавляющего числа больных оказывается достаточно. Превентивная антикоагулянтная терапия в таких условиях представляется неоправданной по соотношению риск/польза и экономически затратной.
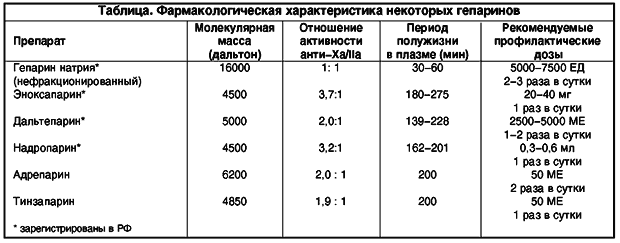
Применение с профилактической целью НФГ возможно, но менее желательно, поскольку он обладает существенно меньшей биодоступностью и мало предсказуемым антикоагулянтным эффектом, чаще вызывает гепарининдуцированную тромбоцитопению и остеопороз. НФГ используют в дозе 5 000 ЕД 2-3 раза в день под кожу живота.
Грубой ошибкой следует признать начало антикоагулянтной профилактики тромбоза через 2-3 дня после операции, как это иногда рекомендуется, т.к. флеботромбоз начинает развиваться раньше, зачастую уже на операционном столе. Лишь в ограниченном числе случаев, при высоком риске интраоперационного кровотечения, можно отложить введение гепарина на несколько часов. В экстренной хирургии, когда не известен коагуляционный потенциал больного, допустимо назначение антикоагулянтов после операции, но не позднее 12 часов после ее окончания.
Воздержаться от введения антикоагулянтов в этой группе пациентов целесообразно лишь при нейрохирургических и офтальмологических вмешательствах, когда даже минимальное кровотечение несет высочайшую опасность. У этих больных следует активно использовать перемежающуюся пневмокомпрессию, тренажеры икроножных мышц.
Существуют еще и так называемые особые случаи, когда хирургическое вмешательство производится на фоне уже имеющегося венозного тромбоза или легочной эмболии. В такой ситуации при флотирующих, эмболоопасных тромбах выполняют имплантацию кава-фильтра или пликацию нижней полы вены, а НМГ или обычный гепарин следует использовать в лечебных дозах.
Считаем необходимым обратить внимание и на чрезвычайную важность максимально ранней активизации больного в послеоперационном периоде, продолжения использования эластической компрессии. В плановой хирургии найдется немного вмешательств, после которых (разумеется, при адекватном обезболивании) нельзя было бы поднять больного на следующие сутки и сделать с ним хотя бы десяток шагов по палате.
Серьезное значение имеет метод анестезиологического пособия. Так, использование регионарной анестезии значительно облегчает течение послеоперационного периода и в несколько раз снижает вероятность развития ВТЭО.
Все вышесказанное служит еще одним аргументом в пользу расширения практики лечения в условиях стационара одного дня, увеличения числа и круга малоинвазивных эндоскопических вмешательств.
Применяющиеся в настоящее время профилактические меры не позволяют в 100% случаев исключить формирование тромбоза в глубоких венах нижних конечностей, однако при их использовании реально минимизировать частоту тромботических осложнений, что позволяет предотвратить, по крайней мере, 2 из 3 летальных легочных эмболий. В Российской Федерации, к сожалению, систематическое профилактическое применение современных антикоагулянтов (НМГ) пока скорее исключение, чем правило. Ссылки на возможность кровотечений на фоне профилактических доз НМГ не имеют аргументированных доказательств, хотя, действительно, в 1-3% случаев возможно возникновение таких осложнений, главным образом в виде раневых гематом. Более тщательный гемостаз решает эту проблему. Вероятность кровотечений не идет ни в какое сравнение с частотой ВТЭО и тяжестью их последствий.
Принципы профилактики ВТЭО в травматологии сходны с таковыми у оперированных больных, поскольку в патогенезе тромбообразования очень много общего. Хочется лишь напомнить, что и без оперативных вмешательств до 10% больных старше 50 лет с переломом шейки бедра умирают от массивной ТЭЛА. Высокий риск развития венозного тромбоза после серьезных травм является основанием для антикоагулянтной профилактики. Ее начинают в течение 36 часов после травмы. Применение НМГ также является предпочтительным по сравнению с обычным гепарином, поскольку они в значительно меньшей степени вызывают остеопороз. Продолжительность использования НМГ не должна быть менее 10 дней. Наряду с этим активно используют массаж стоп и голеней, ранние движения конечностей, максимальное сокращение постельного режима. Применение перемежающейся пневматической компрессии при травмах нижних конечностей иногда невозможно или затруднено.
Обязательно ношение (с I триместра) эластичных бинтов или хорошо подобранного по размеру медицинского компрессионного трикотажа I-II компрессионных классов, значительно улучшающих отток по глубоким венам и препятствующих варикозной трансформации вен подкожных с возможным развитием тромбофлебита. С той же целью рекомендуют подъем ножного конца кровати на 10-15 см. Эластическая компрессия нижних конечностей обязательна и во время родов, а также в послеродовом периоде (4-6 недель).
Немаловажным является предупреждение эмоциональных стрессов у беременных. Стрессовая реакция может вызвать активацию тромбогенного потенциала системы гемостаза и торможение фибринолиза.
После родов гепарин постепенно заменяют на антивитамины К и терапию продолжают, по крайней мере, 4-6 недель, хотя оптимальная длительность этого лечения еще не установлена. В послеродовом периоде следует рекомендовать возможно более раннюю активизацию и лечебную физкультуру.
Наиболее сложной представляется задача предотвращения ВТЭО у больных с генетически обусловленными тромбофилическими состояниями. Задачей, стоящей на повестке дня, следует считать биохимический скрининг таких нарушений. При перенесенном венозном тромбозе у пациентов с некоторыми тромбофилиями (например, дефицит AT-III), возможно, оправдано пожизненное применение наименее токсичных кумаринов (варфарина).
В заключение коснемся экономической стороны проблемы ВТЭО. Антикоагулянтную профилактику многие считают неоправданно дорогой. Действительно, стоимость Клексана на стандартный профилактический курс составляет около 52 долларов США. Однако стоимость лишь консервативного лечения флеботромбоза (не менее 300 долларов), а тем более тромбоэмболии легочных артерий (более 900 долларов), превышает таковую во много раз, даже если не рассматривать затраты на лечение хронической венозной недостаточности в отдаленном посттромботическом периоде. Целенаправленная профилактика ВТЭО позволяет не только сохранить жизнь и здоровье многих тысяч пациентов, но и значительные бюджетные средства российского здравоохранения.