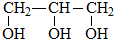с чем не реагирует этиленгликоль
Этиленгликоль: химические свойства и получение
Этиленгликоль C2H4(OH)2 или CH2(OH)CH2OH, этандиол-1,2 – это органическое вещество, предельный двухатомный спирт .
Общая формула предельных нециклических двухатомных спиртов: CnH2n+2O2 или CnH2n(OН)2
Строение этиленгликоля
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому этиленгликоль – жидкость с относительно высокой температурой кипения.
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Химические свойства этиленгликоля
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
1. Кислотные свойства
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
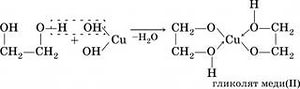
При взаимодействии этиленгликоля с растворами щелочей реакция практически не идет, т. к. образующийся алкоголят почти полностью гидролизуется водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому этиленгликоль не взаимодействует с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Этиленгликоль взаимодействует с активными металлами (щелочными и щелочноземельными).
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии этиленгликоля с галогеноводородами группы ОН замещаются на галоген и образуются дигалогеналкан.
| Например, этиленгликоль реагирует с бромоводородом. |
2.2. Этерификация (образование сложных эфиров)
Многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, этиленгликоль реагирует с уксусной кислотой с образованием эфира: |
2.4. Взаимодействие с кислотами-гидроксидами
Этиленгликоль взаимодействует и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии этиленгликоля с азотной кислотой образуется нитроэтиленгликоль : |
3. Дегидратация
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. При высокой температуре (180 о С) протекает внутримолекулярная дегидратация этиленгликоля и образуется соответствующий ацетальдегид.
4. Окисление этиленгликоля
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Этиленгликоль можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества.
4.2. Окисление кислородом в присутствии катализатора
Этиленгликоль можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.).
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) этиленгликоль окисляется до щавелевой кислоты.
| Например, при взаимодействии этиленгликоля с перманганатом калия в серной кислоте образуется щавелевая кислота |
4.4. Горение этиленгликоля
При сгорании этиленгликоля образуется углекислый газ и вода и выделяется большое количество теплоты.
5. Дегидрирование этаниленгликоля
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования.
| Например, при дегидрировании этиленгликоля образуется этандиаль |
Получение этиленгликоля
1. Щелочной гидролиз дигалогеналканов
При взаимодействии дигалогеналканов с водным раствором щелочей образуются двухатомные спирты. Атомы галогенов в дигалогеналканах замещаются на гидроксогруппы.
| Например, при нагревании 1,2-дихлорэтана с водным раствором гидроксида натрия образуется этиленгликоль |
2. Гидрирование карбонильных соединений
| Например, при гидрировании этандиаля образуется этиленгликоль |
О=CН-CH=O + 2H2 → CH2(OH)-CH2OH
3. Гидролиз сложных эфиров
При гидролизе сложных эфиров этиленгликоля и карбоновых кислот образуются этиленгликоль и карбоновая кислота.
4. Мягкое окисление алкенов
Мягкое окисление протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкена разрывается только π-связь и окисляется каждый атом углерода при двойной связи.
При этом образуются двухатомные спирты (диолы).
Понятие и свойства
Этиленгликоль (МЭГ, моноэтиленгликоль) – химический реактив, который 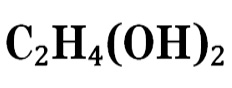
К списку свойств этиленгликоля можно отнести и свойства гликолей. Так, с такими химреактивами, как органические кислоты, образует сложные эфиры, щелочи и щелочные металлы – гликоляты. При окислении этиленгликоля возможно образование смесей гликолевого альдегида и щавелевой кислоты купить которую по доступной цене предлагает наш интернет магазин, а при окислении молекулярным кислородом – смесь муравьиной кислоты.
Данное химическое соединение выпускается двух марок: антифризный и волоконный, к последнему предъявляют очень серьезные требования к количественному содержанию примесей альдегидов.
Открытие этиленгликоля
Данный химический реактив впервые был получен химиком Вюрцом во Франции в середине XIX века. До начала Первой мировой войны он не имел широкого применения, позже в Германии во время военных действий его стали использовать как заменитель глицерина в процессе производства взрывчатых веществ. К 1930 году этиленгликоль стал активно использоваться многими известными производителями динамита.
Токсические и ядовитые действия этиленгликоля зависят от ряда факторов, среди которых следует выделить:
— количество;
— индивидуальную чувствительность организма;
— состояние нервной системы;
— степень наполнения желудка и другие.
Дозы, которые могут привести в организме к необратимым изменениям и вызвать смертельное отравление этиленгликолем, могут варьироваться от 100 до 700 мл. По данным ряда исследований для человека летальной дозой является 50-200 мл. При поражении этиленгликолем смертность очень высока и составляет примерно 60 % всех случаев отравления.
Применение
Области применения данного химического реактива весьма разнообразны. 
— в машиностроительной (в производстве тосола, тормозных жидкостях, антифриза);
— в текстильной (как растворитель красящих веществ);
— энергетической (как теплоноситель в отопительных системах);
— в химической (при производстве полимеров: целлофана, полиуретана, при синтезе высокотемпературных растворителей, для предотвращения процесса образования гидрата метана);
— электротехнической (в качестве вещества, защищающее объекты от замораживания, при производстве конденсаторов, как составляющий компонент в системе жидкостного охлаждения компьютеров);
— в военной (как исходное сырьё при производстве нитрогликоля – взрывоопасного вещества).
Меры безопасности, хранение
Хранить этиленгликоль необходимо в лабораторной посуде из стали, стойкой к коррозии, в закрытых неотапливаемых помещениях.
В связи с тем, что этиленгликоль ядовит, важно не допускать его попадания внутрь организма, так как это токсичное вещество влечет за собой необратимые изменения в работе внутренних органов и может привести к летальному исходу.
Этиленгликоль в соответствии с классификацией химвеществ причислен к третьему классу опасности: он взрывоопасен и горюч, поэтому при работе с ним следует придерживаться особых мер безопасности, используя защитные средства для органов дыхания – противогазы, респираторы, маски; для органов зрения – защитные очки; для кожных покровов – перчатки нитроловые, фартук, бахилы и другие резинотехнические изделия. Лабораторное оборудование и приборы должны быть использованы согласно требованиям инструкции по безопасности при работе с ядовитыми веществами.
Необходимо знать, что в случае отравления МЭГ первая доврачебная помощь должна быть проведена в срочном порядке. Это, прежде всего, промывание желудка плюс слабительные, вызывание рвоты, врачебная – назначение антидота.
Качественные химические реактивы по доступной цене
К выбору приобретения химических реактивов, а также любого другого лабораторного оборудования в Москве следует отнестись с особой ответственностью, так как от качества данной продукции зависят и результаты исследовательских процессов. Как кальций хлористый купить или молочную кислоту купить, так и этиленгликоль стоит в специализированных магазинах, где соблюдаются требования по хранению и отпуску товаров. Одним из таких является магазин химических реактивов Москва розница и оптовая торговля Prime Chemicals Group. Мы специализируемся только по продаже только сертифицированного лабораторного оборудования и химвеществ.
«ПраймКемикалсГрупп» – надежный помощник в оснащении Вашей лаборатории!
ХИМИЧЕСКИЕ СВОЙСТВА ЭТИЛЕНГЛИКОЛЯ
Екатеринбург 2016
Содержание
— Понятие об Спиртах
— Применение спиртов в промышленности
Введение
СПИРТЫ (алкоголи) – класс органических соединений, содержащих одну или несколько группировок С–ОН, при этом гидроксильная группа ОН связана с алифатическим атомом углерода (соединения, у которых атом углерода в группировке С–ОН входит в состав ароматического ядра, называются фенолами)
Классификация спиртов разнообразна и зависит от того, какой признак строения взят за основу.
1. В зависимости от количества гидроксильных групп в молекуле спирты делят на:
а) одноатомные (содержат одну гидроксильную ОН-группу), например, метанол СН3ОН, этанол С2Н5ОН, пропанол С3Н7ОН
б) многоатомные (две и более гидроксильных групп), например, этиленгликоль
HO–СH2–CH2–OH, глицерин HO–СH2–СН(ОН)–CH2–OH, пентаэритрит С(СН2ОН)4.
Многоатомные спирты
Многоатомными являются спирты, содержащие две и более гидроксильные группы в составе молекулы органического вещества. Все двухатомные спирты называются гликолями.
Этиленгликоль
Этиленгликоль (тривиальное название) или этандиол (систематическое название). Химическая формула HO−CH2CH2−OHHO−CH2CH2−OH.
Двухатомный спирт, простейший представитель многоатомных спиртов. В очищенном виде представляет собой прозрачную бесцветную жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Этиленгликоль токсичен. По степени воздействия на организм относится к веществам 3-го класса опасности. Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу. Этиленгликоль — горючее вещество. Температура вспышки паров 120 градусов C.
Этиленгликоль находит широкое применение в технике в качестве охлаждающего реагента систем охлаждения двигателей и компьютеров, антифризов и тормозных жидкостей. Используется в органическом синтезе.
ПОЛУЧЕНИЕ ЭТИЛЕНГЛИКОЛЯ
В промышленности этиленгликоль получают путём:
· (I) гидратацией 1,2-дихлорэтана;
· (II) гидратацией хлоргидринов;
· (III) гидратации окиси этилена при повышенном давлении и температуре в присутствии 0,1—0,5 % серной или ортофосфорной кислоты, достигая 90 % выхода;
· (IV) окислением этилена перманганатом калия:
ХИМИЧЕСКИЕ СВОЙСТВА ЭТИЛЕНГЛИКОЛЯ
Этиленгликоль обладает всеми свойствами гликолей.
1. Взаимодействие с щелочными металлами: образует соли гликоляты

3. Взаимодействие с галогеноводородами HHal: образует этиленгалогенгидрины
HOCH2CH2OH+HHal⟶HOCH2CH2Hаl+H2O
4. Дегидратация при нагревании в присутствии концентрированной серной кислоты: образуется ацетальдегид 5. Окисление в зависимости от условий и окислителя: могут образовываться
· глиоксалевая и щавелевая кислоты;
Окисление молекулярным кислородом приводит к образованию формальдегида HCOH и муравьиной кислоты HCOOH.
Глицерин
Глицерин(тривиальное название) или пропантриол-1,2,3 (название по систематической номенклатуре).
Бесцветная вязкая жидкость, за счет наличия водородных связей смешивается с водой в любых отношениях. Безводный глицерин очень гигроскопичен, при попадании на кожу вызывает ожоги, но в разбавленном состоянии используется при изготовлении косметических средств (кремов, гелей), и даже в пищевой промышленности для приготовления ликеров.
Получение глицерина
Глицерин получают гидролизом жиров, а также из пропилена (через получение 2,3-гидроксипропановой кислоты с последующим ее восстановлением):
Этиленгликоль. Применение, свойства, характеристики
Что такое этиленгликоль ?
Этиленгликоль – это бесцветная вязкая жидкая субстанция, лишённая всяких ароматических признаков. Имеет некоторый сладкий вкус, выраженный не слишком отчётливо. Вещество токсично, относится к группе гликолей (двухатомные спирты). Получен данный реактив лабораторными методами в середине девятнадцатого столетия. Длительное время оставался лабораторным веществом, не имеющим никакого применения в хозяйственных целях. Однако в к началу двадцатого века выяснилось, что данный химикат может с успехом заменить глицерин необходимый при производстве взрывчатых веществ и боеприпасов.
Этиленгликоль (формула вещества C2H6O2) – первый в ряду гликолей, органических веществ, имеющих в составе по 2 гидроксильных группы (О – Н) и сходных по внешнему виду, химическому составу и свойствам.
Свойства этиленгликоля
Смешивается с водой, спиртами. Вещество сильно гигроскопично, взрыво- и пожароопасно, что, как уже было сказано, повлияло на его практическое использование в производственных целях.
Вместе с тем, данный химикат имеет низкую температуру замерзания (-12,9°С) и высокую температуру кипения (+197°С). Вязкость этиленгликоля обусловлена плотностью вещества 1,113 г/см³, которая более чем на десять процентов выше, чем плотность воды.
Химические свойства этиленгликоля сходны со свойствами одноатомных спиртов. Вещество способно вступать в реакции с представителями группы щелочных металлов, образовывая при этом гликоляты (полные и неполные). Этиленгликоль взаимодействует с гидроксидами металлов, с органическими и неорганическими кислотами и другими веществами.
Применение этиленгликоля
Несмотря на то, что первоначальной отраслью, в которой нашёл своё применение этот химикат, было производство взрывчатых веществ, в наши дни для этих целей используются более дешёвые и более мощные аналоги. Но этиленгликоль по-прежнему широко эксплуатируется в промышленном производстве, только теперь уже в других отраслях.
Чаще это оказываются сферы, производящие различные жидкости технического назначения. Низкая температура кристаллизации и невысокая стоимость данного продукта послужили тому, что примерно 60% производимого современной химической индустрией этиленгликоля поступает в изготовление антифризов и прочих веществ.
Кроме того, этот химикат используется в качестве сырья для синтеза широкой номенклатуры полимерных материалов. Таких, как полиуретаны, полиэтилентерефталат и прочее. Из них производят пластиковую тару (бутылки и прочие изделия), волоконную, плёночную продукцию и многое другое.
Всё более широкую распространённость получает этот материал в качестве теплоносителя. Этиленгликоль мало пригоден для этих целей в чистом виде, однако популярны в этой отрасли его водные растворы с различной концентрацией. У этих разновидностей теплоносителей температура замерзания ниже нуля и температура закипания заметно выше ста градусов по Цельсию. Однако есть ещё кое-что, что выгодно отличает эти смеси от воды. Водные растворы этиленгликоля, даже при их охлаждении до температуры застывания, не превращаются в ледяные глыбы, способные порвать стенки трубопроводов и прочие элементы отопительных систем. Они при замерзании превращаются в желеподобную субстанцию, которая не наносит никакого вреда ни трубам, ни котлам. А при повышении температуры, снова возвращается в жидкое агрегатное состояние и может далее эксплуатироваться по назначению.
А также с применением этиленгликоля производятся жидкости для гидравлической техники. В чистом виде этот продукт в данной отрасли почти не применяется, но часто используется в качестве компонента этих технических жидкостей.
Помимо всего названного в химическом промышленном производстве пригодились растворяющие свойства этого вещества. Его применяют, как растворитель, как пластифицирующий агент при получении различных полимерных материалов, резинотехнических изделий и прочих видов продукции.
Токсичность этиленгликоля
Химикат не является легкоподвижным и подверженным обильному испарению, поэтому накапливать опасное количество паровоздушных смесей быстро не способен. Однако класс опасности этиленгликоля предписывает обязательное соблюдение всего свода правил техники безопасности при работе с данной группой веществ. Также к числу обязательных условий его безопасной эксплуатации стоит отнести обязательное оснащение всех рабочих помещений приточно-вытяжными вентиляционными системами достаточной эффективности. И использование рабочим персоналом индивидуальных средств защиты органов дыхания.
Получение этиленгликоля
На данный момент существует несколько методов синтеза этого соединения. Наиболее распространённый в химическом производстве метод заключается в каталитической гидратации оксида этилена. Условия данного химического взаимодействия предусматривают давление на уровне десяти атмосфер, и повышение температуры до 200 °C. Полученный в процессе описанной реакции продукт содержит порядка 90% этиленгликоля и некоторое количество примесей, состоящих их других гликолей более высокого порядка и определённого количества высших полимеров.
Существует ещё один более старый метод, который сейчас, большей частью, снят с вооружения в химической индустрии. Он заключается в гидролизе группы веществ сложных эфиров. В этом случае также получался конечный продукт не в чистом виде, а с некоторым количеством примесей. В качестве примесей в этом случае оказывалась группа кислот, удаляющихся при дальнейшей обработке.