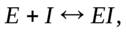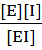с чем связывается конкурентный ингибитор
Конкурентное и неконкурентное ингибирование
Конкурентное и неконкурентное ингибирование [ править | править код ]
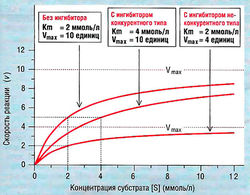
На рис. показано, как выглядит график Михаэлиса— Минтен (зависимость V от [S]) без ингибиторов и в присутствии ингибиторов конкурентного или неконкурентного типа. Рисунок иллюстрирует те же процессы в координатах Лайнуивера—Берка (т.е. в обратных координатах). Приведенный на рис. фермент в отсутствие ингибитора имеет Vmax = 10 единиц и Km = 2 ммоль/л.
Ингибиторы конкурентного типа используются в качестве лекарств. По своей структуре они сходны с природным субстратом и поэтому конкурируют с ним за доступ к сайту связывания на ферменте. Так, противоопухолевый препарат метотрексат имеет структурное сходство с фолатом — субстратом дигидрофолатредуктазы. Метотрексат используется для ингибирования дигидрофолатредуктазы при химиотерапии рака.
Из рис. следует, что ферменту в присутствии ингибитора конкурентного типа требуется большее количество субстрата, чтобы «выиграть» соревнование с ингибитором. При достаточном количестве субстрата ингибитор-конкурент уступает первенство ферменту, и последний может работать с максимальной скоростью Vmax. Примечание: конкурентный ингибитор закрывает сайт связывания субстрата на ферменте, тем самым уменьшая сродство фермента к субстрату; другими словами, он повышает Кт (в приведенном примере до 4 ммоль/л), но Vmax при этом остается неизменной.
Ингибиторы неконкурентного типа. Ингибитор неконкурентного типа связывается не с субстратсвязывающим сайтом, а с другим сайтом фермента, поэтому ингибирующий эффект нельзя преодолеть посредством повышения концентрации субстрата. Чтобы понять принцип неконкурентного ингибирования, достаточно запомнить, что для каждого субстрата существует свой сайт связывания. Таким образом, повышение концентрации одного субстрата никак не повлияет на связь ингибитора с ферментом, который блокирует другой (несубстратсвязывающий) сайт фермента. Поэтому ингибиторы неконкурентного типа блокируют определенную долю молекул фермента, не изменяя Km, но понижая Vmax на некоторый постоянный процент.
Конкурентное ингибирование



СОДЕРЖАНИЕ
| 1 Конкурентное ингибирование ….………………………………………………… |
| 2Неконкурентное ингибирование………………………………………………….. |
| 3Графическое изображение в двойных обратных координатах……….………… |
| Список использованной литературы…..…………………………………………… |
Конкурентное ингибирование
Существуют обратимые ингибиторы двух типов – конкурентные и неконкурентные. Изучение обратимых ингибиторов ферментов позволило получить весьма важные сведения о структуре активных центров различных ферментов.
Конкурентный ингибитор конкурирует с субстратом за связывание с активным центром, но в отличие от субстрата связанный с ферментом конкурентный ингибитор не подвергается ферментативному превращению (Рисунок 1). Отличительная особенность конкурентного ингибирования состоит в том, что его можно устранить или ослабить, просто повысив концентрацию субстрата.
Рисунок 1- Схема конкурентного ингибирования активности фермента
Например, если при заданных концентрациях субстрата и конкурентного ингибитора активность фермента подавлена на 50%, то мы можем уменьшить степень ингибирования, повысив концентрацию субстрата.
По своей трехмерной структуре конкурентные ингибиторы обычно напоминают субстрат данного фермента. Благодаря такому сходству конкурентному ингибитору удается «обмануть» фермент и связаться с ним. Конкурентное ингибирование можно количественно изучать на основе теории МихаэлисаМентен. Конкурентньпй ингибитор I просто обратимо присоединяется к ферменту Е, образуя с ним комплекс EI.Однако в отличие от субстрата ингибитор не подвергается действию фермента и новые продукты реакции не образуются (Рисунок 1).
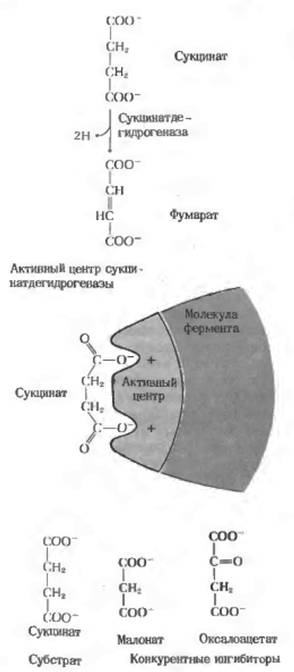
Конкурентные ингибиторы напоминают в структурном отношении сукципат: они содержат две определенным образом расположенные в пространстве отрицательно заряженные группы, которые соответствуют конформацин активного центра.
Изучение структурных особенностей всех этих ингибиторов позволило сделать вывод, что в каталитическом центре сукцинатдегидрогеназы находятся две определенным образом расположенные в пространстве положительно заряженные группы, способные притягивать две отрицательно заряженные карбоксильные группы сукцинат-аниона. Таким образом, каталитический центр сукцинатдегидрогеназы оказывается комплементарным структуре своего субстрата (Рисунок 2).
Конкурентное ингибирование проще всего можно распознать экспериментальным путем, определив влияние концентрации ингибитора на зависимость начальной скорости реакции от концентрации субстрата. Для выяснения вопроса о том, по какому типу конкурентному или неконкурентному происходит обратимое ингибирование фермента, весьма удобно преобразовать уравнение Михаэлиса-Ментен в линейную форму. Чаще всего для этой цели используют метод двойных обратных величин. Из графиков, построенных в двойных обратных координатах, можно определить также значение константы диссоциации комплекса фермент ингибитор. Для реакции диссоциации
константа диссоциации равна
К =
Лекарства обычно ингибируют ферменты
В медицине активно разрабатываются и используются соединения, изменяющие активность ферментов с целью регуляции скорости метаболических реакций и уменьшения синтеза определенных веществ в организме.
Подавление активности ферментов обычно называют ингибированием, однако это не всегда корректно. Ингибитором называется вещество, вызывающее специфичное снижение активности фермента. Таким образом, неорганические кислоты и тяжелые металлы ингибиторами не являются, а являются инактиваторами, так как снижают активность многих ферментов, т.е. действуют неспецифично.
Ингибирование ферментов
Можно выделить два основных направления ингибирования
Необратимое ингибирование
При необратимом ингибировании происходит связывание или разрушение функциональных групп фермента, необходимых для проявления его активности.
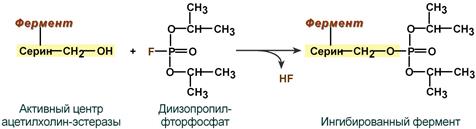
Например, вещество диизопропилфторфосфат прочно и необратимо связывается с гидроксигруппой серина в активном центре фермента ацетилхолинэстеразы, гидролизующей ацетилхолин в нервных синапсах. Ингибирование этого фермента предотвращает распад ацетилхолина в синаптической щели, в результате чего медиатор продолжает оказывать воздействие на свои рецепторы, что бесконтрольно усиливает холинергическую регуляцию.
Аналогично диизопропилфторфосфат ингибирует химотрипсин и другие протеазы, имеющие в активном центре серин (сериновые протеазы).
Диизопропилфторфосфат относится к нервно-паралитическим ядам, аналогичным образом действуют боевые фосфоорганические вещества (зарин, зоман). Сюда же относится вещество «малатион», включенный в инсектициды (карбофос, дихлофос) и превращающийся в организме насекомых в ингибитор ацетилхолинэстеразы, а в организме животных и человека разрушающийся до безвредных продуктов.
Механизм необратимого ингибирования ацетилхолинэстеразы
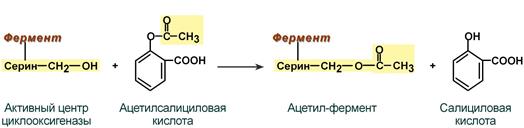
Еще один пример связан с ингибированием ацетилсалициловой кислотой (аспирином) ключевого фермента синтеза простагландинов – циклооксигеназы. Эта кислота входит в состав противовоспалительных средств и используется при воспалительных заболеваниях и лихорадочных состояниях. Присоединение ацетильной группы к гидроксильной группе серина в активном центре фермента вызывает инактивацию последнего и прекращение синтеза простагландинов.
Механизм необратимого ингибирования циклооксигеназы
Третьим показательным примером необратимого ингибирования является влияние антибиотика пенициллина на фермент транспептидазу, сшивающую цепи пептидогликана как последний шаг в синтезе клеточной стенки бактерий.
Обратимое ингибирование
При обратимом ингибировании происходит непрочное связывание ингибитора с функциональными группами фермента, вследствие чего активность фермента постепенно восстанавливается.
Примером обратимого ингибитора может служить прозерин, связывающийся с ферментом ацетилхолинэстеразой в ее активном центре. Группа ингибиторов холинэстеразы (прозерин, дистигмин, галантамин) используется при миастении, после энцефалита, менингита, травм ЦНС.
Конкурентное ингибирование
При таком виде ингибирования ингибитор по своей структуре похож на субстрат фермента. Поэтому он соперничает с субстратом за активный центр (за контактный участок), что приводит к уменьшению связывания субстрата с ферментом и нарушению катализа. В этом состоит особенность конкурентного ингибирования – возможность усилить или ослабить ингибирование через изменение концентрации субстрата. При данном ингибировании максимальная скорость реакции остается вполне достижимой при создании высоких концентраций субстрата.
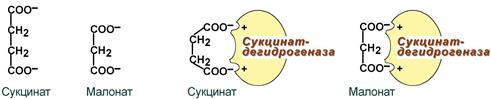
1. Ингибирование фермента цикла трикарбоновых кислот сукцинат-дегидрогеназы малоновой кислотой, структура которой схожа со структурой субстрата этого фермента – янтарной кислоты (сукцината).
Конкурентное ингибирование сукцинатдегидрогеназы
3. В качестве других примеров лекарственных конкурентных ингибиторов можно привести
Данный вид ингибирования связан с присоединением ингибитора не в активном центре, а в другом месте молекулы. Но при этом меняется структура активного центра и связь с субстратом становится невозможной. Это может быть аллостерическое ингибирование, когда активность фермента снижается естественными модуляторами, или связывание с ферментом каких-либо веществ вне активного и аллостерического центра. Например:
Особенностью неконкурентного ингибитора является его способность связываться с ферментом независимо от субстрата, т.е. изменение концентрации субстрата никак не влияет на образование комплекса фермент-ингибитор.
В этом случае ингибитор связывается в активном центре с фермент-субстратным комплексом. Повышение концентрации субстрата, увеличивая количество фермент-субстратного комплекса, усиливает и связывание ингибитора с ним. Таким образом, бесконкурентное ингибирование более сложно, чем другие типы ингибирования.
Смешанное ингибирование
При таком ингибировании ингибитор способен присоединяться везде – не только в активном центре, но и в других частях молекулы. Но после этого фермент еще способен частично сохранять свою активность. Примером является влияние мертиолата (ртутьорганическое вещество) на сахаразу грибов микромицетов для подавления их роста.
РАЗДЕЛ 2. ЭНЗИМОЛОГИЯ
VI. Ингибирование ферментативной активности
Под термином «ингибирование ферментативной активности» понимают снижение каталитической активности в присутствии определённых веществ — ингибиторов. К ингибиторам следует относить вещества, вызывающие снижение активности фермента. Следует отметить, что все денатурирующие агенты также вызывают уменьшение скорости любой ферментативной реакции, вследствие неспецифической денатурации белковой молекулы, поэтому денатурирующие агенты к ингибиторам не относят.
Ингибиторы вызывают большой интерес для выяснения механизмов ферментативного катализа, помогают установить роль отдельных ферментов в метаболических путях организма. В основе действия многих лекарственных препаратов и ядов лежит ингибирование активности ферментов, поэтому знание механизмов этого процесса крайне важно для молекулярной фармакологии и токсикологии.
Ингибиторы способны взаимодействовать с ферментами с разной степенью прочности. На основании этого различают обратимое и необратимое ингибирование. По механизму действия ингибиторы подразделяют на конкурентные и неконкурентные.
А. Обратимое ингибирование
Обратимые ингибиторы связываются с ферментом слабыми нековалентными связями и при определённых условиях легко отделяются от фермента. Обратимые ингибиторы бывают конкурентными и неконкурентными.
1. Конкурентное ингибирование
К конкурентному ингибированию относят обратимое снижение скорости ферментативной реакции, вызванное ингибитором, связывающимся с активным центром фермента и препятствующим образованию фермент-субстратного комплекса. Такой тип ингибирования наблюдают, когда ингибитор — структурный аналог субстрата, в результате возникает конкуренция молекул субстрата и ингибитора за место в активном центре фермента. В этом случае с ферментом взаимодействует либо субстрат, либо ингибитор, образуя комплексы фермент-субстрат (ЕS) или фермент-ингибитор (ЕI). При формировании комплекса фермента и ингибитора (ЕI) продукт реакции не образуется (рис. 2-21).
Рис. 2-21. Схема конкурентного ингибирования активности фермента.
Для конкурентного типа ингибирования справедливы следующие уравнения:
Классический пример конкурентного ингибирования — ингибирование сукцинатдегидрогеназной реакции малоновой кислотой (рис. 2-22). Малоновая кислота — структурный аналог сукцината (наличие двух карбоксильных групп) и может так же взаимодействовать с активным центром сукцинат дегидрогеназы. Однако отщепление двух атомов водорода от малоновой кислоты невозможно; следовательно, скорость реакции снижается.
Конкурентные ингибиторы уменьшают скорость химической реакции. Конкурентный ингибитор повышает Кm для данного субстрата (уменьшает сродство субстрата к ферменту). Это означает, что в присутствии конкурентного ингибитора необходима большая концентрация субстрата для достижения 1/2 Vmax.
Увеличение соотношения концентрации субстрата и ингибитора снижает степень ингибирования. При значительно более высоких концентрациях субстрата ингибирование полностью исчезает, потому что активные центры всех молекул фермента будут находиться преимущественно в комплексе с субстратом.
Лекарственные препараты как конкурентные ингибиторы
Многие лекарственные препараты оказывают своё терапевтическое действие по механизму конкурентного ингибирования. Например, четвертичные аммониевые основания ингибируют ацетилхолинэстеразу, катализирующую реакцию гидролиза ацетилхолина на холин и уксусную кислоту (см. схему ниже).
При добавлении ингибиторов активность ацетилхолинэстеразы уменьшается, концентрация ацетилхолина (субстрата) увеличивается, что сопровождается усилением проведения нервного импульса. Ингибиторы холинэстеразы используют при лечении мышечных дистрофий. Эффективные антихолинэстеразные препараты — прозерин, эндрофоний и др. (рис. 2-23).
Антиметаболиты как лекарственные препараты
В качестве ингибиторов ферментов по конкурентному механизму в медицинской практике используют вещества, называемые антиметаболитами. Эти соединения, будучи структурными аналогами природных субстратов, вызывают конкурентное ингибирование ферментов, с одной стороны, и, с другой — могут использоваться этими же ферментами в качестве псевдосубстратов, что приводит к синтезу аномальных продуктов. Аномальные продукты не обладают функциональной активностью; в результате наблюдают снижение скорости определённых метаболических путей.
В качестве лекарственных препаратов используют следующие антиметаболиты: сульфаниламидные препараты (аналоги парааминобензойной кислоты), применяемые для лечения инфекционных заболеваний (см. раздел 9), аналоги нуклеотидов для лечения онкологических заболеваний (см. раздел 10).
2. Неконкурентное ингибирование
Неконкурентным называют такое ингибирование ферментативной реакции, при котором ингибитор взаимодействует с ферментом в участке, отличном от активного центра (рис. 2-24). Неконкурентные ингибиторы не являются структурными аналогами субстрата.
Неконкурентный ингибитор может связываться либо с ферментом, либо с фермент-субстратным комплексом, образуя неактивный комплекс. Присоединение неконкурентного ингибитора вызывает изменение конформации молекулы фермента таким образом, что нарушается взаимодействие субстрата с активным центром фермента, что приводит к снижению скорости ферментативной реакции.
Рис. 2-24. Схема неконкурентного ингибирования активности фермента.
Кинетическая зависимость неконкурентного ингибирования представлена на рис. 2-25. Этот тип ингибирования характеризуется снижением Vmах ферментативной реакции и уменьшением сродства субстрата к ферменту, т. е. увеличением Кm.
Рис. 2-25. Влияние неконкурентного ингибитора на скорость ферментативной реакции в зависимости от концентрации субстрата. Vmах — максимальная скорость реакции в отсутствие ингибитора; ‘\/mах — максимальная скорость реакции в присутствии ингибитора; Кm — константа Михаэлиса в отсутствие ингибитора; ‘Кm — константа Михаэлиса в присутствии ингибитора.
Б. Необратимое ингибирование
Необратимое ингибирование наблюдают в случае образования ковалентных стабильных связей между молекулой ингибитора и фермента. Чаще всего модификации подвергается активный центр фермента. В результате фермент не может выполнять каталитическую функцию.
К необратимым ингибиторам относят ионы тяжёлых металлов, например, ртути (Нg 2+ ), серебра (Аg + ) и мышьяка (Аs 3+ ), которые в малых концентрациях блокируют сульфгидрильные группы активного центра. Субстрат при этом не может подвергаться химическому превращению (рис. 2-26). При наличии реактиваторов ферментативная функция восстанавливается. В больших концентрациях ионы тяжёлых металлов вызывают денатурацию белковой молекулы фермента, т. е. приводят к полной инактивации фермента.
Рис. 2-26. Механизм действия ионов ртути как необратимого ингибитора. Ионы ртути в малых концентрациях блокируют сульфгидрильные группы активного центра, что приводит к снижению скорости ферментативной реакции.
1. Специфические и неспецифические ингибиторы
Использование необратимых ингибиторов представляет большой интерес для выяснения механизма действия ферментов. С этой целью применяют вещества, блокирующие определённые группы активного центра ферментов. Такие ингибиторы называют специфическими. Ряд соединений легко вступает в реакции с определенными химическими группами. Если эти группы участвуют в катализе, то происходит полная инактивация фермента.
Роль гидроксильных групп серина в механизме катализа исследуют с помощью фторфосфатов, например, диизопропилфторфосфата. Диизопропилфторфосфат (ДФФ) специфически реагирует лишь с одним из многих остатков серина в активном центре фермента. Остаток Сер, способный реагировать с ДФФ, имеет идентичное или очень сходное аминокислотное окружение (табл. 2-2). Высокая реакционная способность этого остатка по сравнению с другими остатками Сер обусловлена аминокислотными остатками, также входящими в активный центр ферментов.
Таблица 2-2. Исследование последовательности аминокислотных остатков вокруг реакционноспособного остатка серина, взаимодействующего с ДФФ
Функция ферментов (подкласс ферментов)
Аминокислотные остатки, находящиеся в окружении реакционно-способного серина в активном центре
С чем связывается конкурентный ингибитор
В этом случае вещество, близкое по своей структуре к обычному субстрату фермента, соединяется с активным центром фермента, но не может прореагировать с ним. Находясь здесь, оно преграждает доступ к активному центру любой молекуле настоящего субстрата.
Поскольку в этом случае ингибитор и субстрат конкурируют за место на активном центре фермента, эту форму ингибирования называют конкурентным ингиЖированием. Для конкурентного ингибирования характерно, что, если концентрация субстрата увеличивается, то скорость реакции возрастает, т. е. это ингибирование обратимо.
Рисунок иллюстрирует один из примеров конкурентного ингибирования.
Явление конкурентного ингибирования помогает понять механизм действия некоторых лекарственных препаратов, в частности сульфаниламидов. Цель химиотерапии — уничтожить при помощи тех или иных химических препаратов возбудителя болезни, не повреждая при этом ткани организма-хозяина. Первыми такими препаратами были сульфаниламиды, антибактериальное действие которых было обнаружено в 30-е годы XX в. Во время второй мировой войны их широко применяли для борьбы с раневыми инфекциями. Сульфаниламиды по своей химической природе близки к парааминобензойной кислоте (ПАБК) — необходимому фактору роста многих патогенных бактерий. ПАБК требуется бактериям для синтеза фолиевой кислоты, которая служит у них одним из кофакторов ферментов. Сульфаниламиды ингибируют один из ферментов, участвующих в синтезе фолиевой кислоты из ПАБК.
Животные клетки нечувствительны к сульфаниламидам, хотя им для некоторых реакций и требуется фолиевая кислота. Объясняется это тем, что они используют уже образованную фолиевую кислоту; метаболический путь, который бы обеспечивал ее синтез, у них отсутствует.
Неконкурентное обратимое ингибирование
Ингибиторы этого типа не родственны по своей структуре субстрату данного фермента; в образовании комплекса с ингибитором участвует в этом случае не активный центр фермента, а какая-нибудь другая часть его молекулы. Это не препятствует соединению субстрата с ферментом, но делает невозможным катализ.
С повышением концентрации ингибитора скорость реакции все более снижается. К моменту насыщения ингибитором она оказывается практически равной нулю. В отличие от конкурентного инги-бирования в этом случае повышение концентрации субстрата на скорость реакции не влияет.