сера более сильный окислитель чем
Тест с ответами: “Сера”
1. Распределение электронов по энергетическим уровням в атоме серы:
а) 2, 8, 6 +
б) 2, 8, 8, 6
в) 2, 8,
2. Сера – более сильный окислитель, чем:
а) фтор
б) фосфор +
в) хлор
5. Раствор серной кислоты может взаимодействовать со всеми веществами группы:
а) NaOH, ZnO, Cu, Na2CO3
б) MgO, CO2, NaCl, Fe(OH)3
в) Mg(OH)2, BaCl2, FeO, Zn +
6. И сернистый газ, и оксид серы (VI) будут реагировать со следующей парой веществ:
а) H2O и Cl2
б) NaOH и CaO +
в) Н2О и СО2
7. Для осуществления превращения H2S→SO2→SO3→K2SO4 нужно последовательно использовать:
а) воду, кислород, карбонат калия
б) кислород, воду, калий
в) кислород, кислород, гидроксид калия +
8. Газ, обладающий запахом тухлых яиц, образующий при растворении в воде слабую кислоту, называется:
а) сероводород +
б) сернистый
в) угарный
9. Концентрированную серную кислоту прилили к медным стружкам и нагрели. Продуктами реакции будут:
а) CuSO4 и H2O
б) CuS и H2S
в) CuSO4, SO2 и H2O +
10. На полное «растворение» алюминия массой 2,7 г затратится серной кислоты (в г):
а) 24,7 г
б) 14,7 г +
в) 4,7 г
11. Половина получаемой серы в природе используется для получения:
а) серной кислоты +
б) спичек
в) сернистой кислоты
12. Способствует очистки нефти, жидкий:
а) триоксид серы
б) диоксид серы +
в) анридрид
13. Для лечения ревматизма используют ванны с:
а) сероводородом +
б) триоксидом серы
в) диоксидом серы
14. Бесцветный газ с резким запахом:
а) триоксид серы
б) анридрид
в) диоксид серы +
15. При образовании серной кислоты с водой вступает в реакцию:
а) триоксид серы +
б) диоксид серы
в) анридрид
16. Соли сероводородной кислоты называются:
а) сульфаты
б) сульфиды +
в) сульфиты
17. Сера проявляет окислительные свойства при взаимодействии с:
а) фтором
б) хлором
в) водородом +
18. При температуре 119 градусов, какая сера плавится, превращаясь в желтокоричневую жидкость:
а) моноклинная
б) ромбическая +
в) пластическая
19. Какое аллотропное видоизменение серы плохо проводит ток и тепло:
а) кубическая
б) моноклинная
в) ромбическая +
20. В соединении H2SO4 сера проявляет степень окисления равную:
а) 5
б) 6 +
в) 4
21. Сера расположена в этой подгруппе:
а) главной +
б) основной
в) побочной
22. Сера является составной частью органических соединений:
а) жиров
б) белков +
в) углеводов
23. Сера проявляет высшую валентность равную:
а) 4
б) 2
в) 6 +
24. Количество энергетических уровней у серы равно:
а) 4
б) 3 +
в) 5
25. Сколько аллотропных видоизменений серы существует:
а) 5
б) 4
в) 3 +
26. Для отбеливания шерсти, шелка используют:
а) триоксид серы
б) диоксид серы +
в) сульфат калия
27. Серная мазь используется для производства мази при заболеваниях:
а) кожи +
б) глаз
в) натоптышей
28. Красный цвет краски придает:
а) сульфит кадмия
б) сульфид натрия
в) сульфид ртути +
29. При температуре 160 градусов сера превращается в молекулы с такой цепью:
а) открытой +
б) замкнутой
в) разорванной
Контролирующий материал Тесты, для текущего контроля знаний по теме: «Сера и её соединения»
государственного образовательного профессионального образовательного учреждения Саратовской области
« Саратовский областной базовый медицинский колледж »
Тесты , для текущего контроля знаний по теме :
«Сера и её соединения »
Дисциплина «Общая неорганическая химия»
Тема : «Сера и её соединения»
Контролирующий материал тесты, для текущего контроля знаний по дисциплине «Общая неорганическая химия»
Автор: Белова Наталья Леонидовна Балашов 2021 г.
Общепрофессиональных дисциплин Протокол№. от». «20. г. Председатель ЦМК__ Тимофеева О.С
1. Распределение электронов по энергетическим уровням в атоме серы:
3. Степени окисления серы изменяются с +6 до 0 в группе веществ:
4.Раствор серной кислоты может взаимодействовать со всеми веществами из группы:
В )CuO, Fe, HNO3, NaOH
5. Схеме превращения S +6 → S +4 соответствует уравнению реакции:
6. И сернистый газ, и оксид серы( VI ) будут реагировать со следующей парой веществ:
А) воду, кислород, оксид калия
Б) кислород, воду, калий
В) кислород, кислород.гидроксид калия
Г) воду, кислород, карбонат калия
А) является восстановителем
Б) является окислителем
В) понижает степень окисления
Г) не изменяет степень окисления
9. Разбавленная серная кислота не будет взаимодействовать с каждым веществом изследующей пары веществ:
А) водород, воду, оксид кальция
Б) водород, кислород, гидроксид кальция
В) водород, кислород, кальций
Г) водород, воду, кальций
1.Распределение электронов по энергетическим уровням в атоме серы:
А) 2, 6
3. Степени окисления серы изменяются с +6 до 0 в группе веществ:
А) S,SO2, SO3
4. Раствор серной кислоты может взаимодействовать со всеми веществами из группы:
А) MgO, CO2, NaCl, Fe(OH)3
Б ) NaOH, ZnO, Cu, Na2CO3
В ) CuO, Fe, HNO3, NaOH
Г ) Mg(OH)2, BaCl2, FeO, Zn
5. Схеме превращения S+6→ S+4 соответствует уравнения реакций:
А) SO3+ H2O = H2SO4
Б ) H2SO4+ Zn = ZnSO4+ H2
В ) 2SO2+ O2= 2SO3
Г ) Cu +2H2SO4= CuSO4+ SO2+ 2H2O
7. Для осуществления превращения H2S → SO2→ SO3→ K2SO4 нужно последовательно
использовать:
А) воду, кислород, оксид калия
Б) кислород, воду, калий
В) кислород, кислород, гидроксид калия
Г) воду, кислород, карбонат калия
Б) является окислителем
В) понижает степень окисления
Г) не изменяет степень окисления
9. Разбавленная серная кислота не будет взаимодействовать с каждым веществом из следующей пары веществ:
А) CuO, HCl
10. Для осуществления превращения S → H2S → SO2→ CaSO3 нужно последовательно
использовать:
А) водород, воду, оксид кальция
Б) водород, кислород, гидроксид кальция
В) водород, кислород, кальций
Г) воду, воду, кальций
1. При комнатной температуре сера, серная кислота и сероводород имеют следующие агрегатные состояния:
А) Жидкое, жидкое и твердое
Б) Твердое, газообразное и газообразное
В) Твердое, жидкое и жидкое
Г) Твердое, жидкое и газообразное
2. Сера проявляет степени окисления
3. Химический элемент, имеющий схему строения атома: +16 ) 2е,8е,6е – это:
4.Степень окисления серы в гидросульфите натрия:
5. В реакции взаимодействия серы с кислородом сера является:
В) Не меняет степень окисления
6. Назовите вещество по его физическим свойствам: бесцветный газ, с запахом тухлых яиц, тяжелее воздуха, ядовит – это:
7.Схеме превращения S +6 → S +4 соответствует уравнения реакций:
А) SO 3 + H 2 O = H 2 SO 4
Б ) H2SO4+ Zn = ZnSO4+ H2
В ) 2SO2+ O2= 2SO3
Г ) Cu +2H2SO4= CuSO4+ SO2+ 2H2O
А) водород, хлор, серную кислоту
В) водород, концентрированную серную кислоту, гидроксид кальция
10. К окислительно-восстановительным относится реакция между водой и
«Сера и её соеденения»
Саенко О.Е. Аналитическая химия: учебник для средних специальных учебных заведений. О.Е Саенко- Издательство 4-е,стер,-Ростов. Д: Феник 2016
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Методическая работа в онлайн-образовании
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Ищем педагогов в команду «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Похожие материалы
Терминологический диктант по теме: «Химическая связь. Строение вещества»
Тест по теме: «Периодический закон и периодическая система Д. И. Менделеева»
Конспект урока на тему «Карбоновые кислоты»
Ктп по химии 9 класс 2 часа в неделю «ХимиЯ»
Ктп по химии 2 часа в неделю «ХимиЯ»
Презентация по химии на тему «Жиры: процессы, происходящие при жарке и варке»
Рабочая программа по химии 10-11 классы. 2020г.
Рабочая программа по химии 8-9 классы. 2020г.
Не нашли то что искали?
Воспользуйтесь поиском по нашей базе из
5361740 материалов.
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
В России планируют создавать пространства для подростков
Время чтения: 2 минуты
Петербургский Политех создал отдельное меню для вегетарианцев в своих столовых
Время чтения: 1 минута
Каждый третий российский школьник хотел бы стать разработчиком игр
Время чтения: 2 минуты
В России будут создавать школьные театры
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Проверочная работа «Сера и её соединения»
Проверочная работа по теме «Сера и её соединения» 9 класс
Часть А. Задания с выбором одного правильного ответа (10 баллов)
Для серы характерна степень окисления:
Сера – более сильный окислитель, чем
1. Фтор 2. Хлор 3. Фосфор 4. Кислород
1. S, SO2, SO3 2. H2SO4, SO2, H2S 3. Na2SO4, K2S, S 4. SO3, K2SO3, S
Схема превращения S+6 → S+4 соответствует уравнению реакции
1. SO3 + H2O → H2SO4 3. H2SO4 + Zn → ZnSO4 + H2
2. 2SO2 + O2 → 2SO3 4. Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Раствор серной кислоты может взаимодействовать со всеми веществами группы
1. MgO, CO2, NaCl, Fe(OH)3 3. NaOH, ZnO, Cu, Na2CO3
2. CuO, Fe, HNO3, NaOH Mg(OH)2, 4. BaCl2, FeO, Zn, KOH
И сернистый газ, и оксид серы (VI) будут реагировать со следующей парой веществ
1. Н2О и СО2 2. NaOH и CaO 3. H2O и Cl2 4. H2S и О2
1. Воду, кислород, оксид калия 3. Кислород, воду, калий
2. Кислород, кислород, гидроксид калия 4. Воду, кислород, карбонат калия
Качественную реакцию на сульфат-анион можно представить сокращённым ионным уравнением
1. 2H+ + SO42- → H2SO4 2. Cu2+ + SO42- → CuSO4 3. Ba2+ + SO42- → BaSO4 4. S2- + 2H+ → H2S
Газ с запахом тухлых яиц, образующий при растворении в воде слабую кислоту, называется
1. Сернистый 2. Угарный 3. Сероводород 4. Хлор
Верны ли следующие утверждения о свойствах серы и её соединений?
А. Самой устойчивой аллотропной модификацией серы является ромбическая.
Б. Чтобы приготовить раствор серной кислоты, нужно в концентрированную кислоту вливать воду.
1. Верно А 2. Верно Б 3. Оба суждения верны 4. Оба суждения неверны
Часть В. Задания на соотнесение и с выбором нескольких вариантов ответа (4 балла)
Выберите два верных суждения. Ответ запишите в виде последовательности цифр без пробелов и запятых (2 балла)
11. В ряду S – Se – Te
1. Уменьшается радиус атома.
2. Усиливаются восстановительные свойства.
3. Уменьшаются кислотные свойства высших оксидов.
4. Увеличивается число электронов на внешнем энергетическом уровне.
5. Уменьшается число энергетических уровней в атоме.
12. Установите соответствие между левой и правой частями уравнения. Ответ представьте в виде последовательности четырёх цифр без пробелов и запятых (2 балла) (цифры могут повторяться!)
H 2 S + O 2 (избыток ) →
Ag + H 2 SO 4 ( разб) →
SO 2 + NaOН ( избыток) →
Часть С Задания со свободным ответом (10 баллов)
(4 балла) Через 240 г 10% раствора гидроксида натрия пропускают сернистый газ объёмом 5,6 л. Определить массу полученной соли. (Ответ: 31,5 г.)
( 5 баллов) Составьте уравнения реакций, соответствующих схеме превращений:
S → H2S → Na2S → PbS Для последней реакции составьте уравнение в сокращённой ионной форме, укажите цвет образовавшегося осадка.
(3 балла) Для реакции H2SO4(конц.) + Zn → …. + H2S + H2O определить коэффициенты методом
электронного баланса, указать окислитель и восстановитель.
Проверочная работа по теме «Сера и её соединения» 9 класс
Часть А. Задания с выбором одного правильного ответа (10 баллов)
Для серы нехарактерна степень окисления:
Сера является восстановителем в реакции с:
1. Фтором 2. Железом 3. Натрием 4. Водородом
1. S, SO2, SO3 2. H2SO4, SO2, H2S 3. Na2SO4, K2S, S 4. SO3, K2SO3, S
Схема превращения S+6 → S-2 соответствует уравнению реакции
1. SO3 + H2O → H2SO4 3. H2SO4 + Zn → ZnSO4 + H2S + H2O
2. 2SO2 + O2 → 2SO3 4. Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Раствор серной кислоты может взаимодействовать со всеми веществами группы
1. MgO, SO2, NaCl, Fe(OH)3 3. Fe(OH)3, CaO, Zn, K2SO3
2. CuO, Ag, HNO2, NaOH 4. Ba(OH)2, NaCl, FeO, Zn
И сернистый газ, и серная кислота будут реагировать со следующей парой веществ
1. Н2О и СО2 2. КOH и MgO 3. H2O и SO3 4. Na2S и О2
Для осуществления превращения S → SO 2 → SO 3 → BaSO 4 нужно последовательно использовать
1. Воду, кислород, оксид бария 3. Кислород, кислород, гидроксид бария
2. Кислород, кислород, нитрат бария 4. Воду, кислород, нитрат бария
Качественную реакцию на сульфит-анион можно представить сокращённым ионным уравнением
1. Pb2+ + S2- → PbS 2. Cu2+ + SO42- → CuSO4 3. Ba2+ + SO42- → BaSO4 4. 2H+ + SO32- → SO2 + H2O
Газ с запахом горящих спичек, образующий при растворении в воде слабую кислоту, называется
1. Сернистый 2. Угарный 3. Сероводород 4. Фтор
Верны ли следующие утверждения о свойствах серы и её соединений?
А. Пластическую серу можно получить при нагревании и последующем охлаждении ромбической серы.
Б. Раствор сернистого газа в концентрированной серной кислоте называется «олеум».
1. Верно А 2. Верно Б 3. Оба суждения верны 4. Оба суждения неверны
Часть В. Задания на соотнесение и с выбором нескольких вариантов ответа (4 балла)
Выберите два верных суждения. Ответ запишите в виде последовательности цифр без пробелов и запятых (2 балла)
11. В ряду Р – S – Cl
1. Уменьшается радиус атома.
2. Усиливаются восстановительные свойства.
3. Уменьшаются кислотные свойства высших оксидов.
4. Увеличивается число электронов на внешнем энергетическом уровне.
5. Уменьшается число энергетических уровней в атоме.
12. Установите соответствие между левой и правой частями уравнения. Ответ представьте в виде последовательности четырёх цифр без пробелов и запятых (2 балла) (цифры могут повторяться!)
H 2 S + O 2 (недостаток ) →
Au + H 2 SO 4 ( разб) →
SO 3 + NaOН ( избыток) →
Fe + H 2 SO 4 ( разб) →
Часть С Задания со свободным ответом (10 баллов)
13. (4 балла) Через 1120 г 5% раствора гидроксида калия пропускают серный ангидрид объёмом 4,48 л. Определить массу полученной соли. (Ответ: 34,8 г.)
14. (5 баллов) Составьте уравнения реакций, соответствующих схеме превращений:
SО2 → SО3 → H2SО4 → ВаSО4 Для последней реакции составьте уравнение в сокращённой ионной форме, укажите цвет образовавшегося осадка.
15. (3 балла) Для реакции Mg + H2SO4 → …. + S + H2O определить коэффициенты методом электронного баланса, указать окислитель и восстановитель.
Ответы к проверочной работе по теме «Сера и её соединения» 9 класс
Критерий: 0-9 = 2, 10-16 =3, 17-23 = 4, 24-26 = 5
Проверочная работа по теме «Сера и её соединения» 9 класс
Часть А. Задания с выбором одного правильного ответа (10 баллов)
1. Распределение электронов по энергетическим уровням в атоме серы:
1) 2, 6 2) 2, 8, 8 3) 2, 8, 6 4) 2, 8, 8, 6
1) фтор 2)хлор 3) фосфор 4) кислород
3. Степени окисления серы изменяются с +6 до 0 в группе веществ:
4. Раствор серной кислоты может взаимодействовать со всеми веществами из группы:
5. Схеме превращения S +6 → S +4 соответствует уравнению реакции:
1) SO 3 + H 2 O = H 2 SO 4 3) H 2 SO 4 + Zn = ZnSO 4 + H 2
2) 2SO 2 + O 2 = 2SO 3 4) Cu +2H 2 SO 4 = CuSO 4 + SO 2 + 2H 2 O
6. И сернистый газ, и оксид серы( VI ) будут реагировать со следующей парой веществ:
1) воду, кислород, оксид калия 3) кислород, воду, калий
2) кислород, кислород. гидроксид калия 4) воду, кислород, карбонат калия
1) является восстановителем 3) является окислителем
2) понижает степень окисления 4) не изменяет степень окисления
9. Разбавленная серная кислота не будет взаимодействовать с каждым веществом из следующей пары веществ:
10. Верны ли следующие утверждения о свойствах серы и её соединений?
А. Чтобы приготовить раствор серной кислоты, нужно в концентрированную кислоту вливать воду.
Б. Раствор серного ангидрида в концентрированной серной кислоте называется «олеум».
Часть В. Задания на соотнесение и с выбором нескольких вариантов ответа (4 балла)
Выберите два верных суждения. Ответ запишите в виде последовательности цифр без пробелов и запятых (2 балла)
11. В ряду S – Se – Te
1. Уменьшается радиус атома.
2. Усиливаются восстановительные свойства.
3. Уменьшаются кислотные свойства высших оксидов.
4. Увеличивается число электронов на внешнем энергетическом уровне.
5. Уменьшается число энергетических уровней в атоме.
12. Установите соответствие между левой и правой частями уравнения. Ответ представьте в виде последовательности четырёх цифр без пробелов и запятых (2 балла) (цифры могут повторяться!)
Тест по теме «Сера и ее соединения»
Тест по теме «Сера и ее соединения» составлен на 1 вариант с ответами
Просмотр содержимого документа
«Тест по теме «Сера и ее соединения»»
Тест «Сера и её соединения»
Распределение электронов по энергетическим уровням в атоме серы
2, 6 2) 2, 8, 8 3) 2, 8, 6 4) 2, 8, 8, 6
Сера – более сильный окислитель, чем
Фтор 2) Хлор 3) Фосфор 4) Кислород
Схема превращения S +6 S +4 соответствует уравнению реакции
Раствор серной кислоты может взаимодействовать со всеми веществами группы
И сернистый газ, и оксид серы (VI) будут реагировать со следующей парой веществ
Для осуществления превращения H2SSO2SO3 K2SO4 нужно последовательно использовать
Воду, кислород, оксид калия
Кислород, кислород, гидроксид калия
Кислород, воду, калий
Воду, кислород, карбонат калия
Качественную реакцию на сульфат-анион можно представить сокращённым ионным уравнением
Zn 0 + 2H + H2 0 + Zn 2+
Газ, обладающий запахом тухлых яиц, образующий при растворении в воде слабую кислоту, называется
Сернистый 2) Угарный 3) Сероводород 4) Йодоводород
Концентрированную серную кислоту прилили к медным стружкам и нагрели. Продуктами реакции будут
На полное «растворение» алюминия массой 2,7 г затратится серной кислоты (в г)
9,8 г 2) 14,7 г 3) 4,9 г 4) 19,6 г
Через 160 г 10% раствора гидроксида натрия пропускают сернистый газ. Сколько г средней соли получится?
28,4 г 2) 25,2 г 3) 56,8 г 4) 50,4 г
Ответы: 1) 3; 2) 3; 3) 3; 4) 4; 5) 4; 6) 2; 7) 2; 8) 3; 9) 3; 10) 4; 11) 2; 12) 2.
Сера более сильный окислитель чем
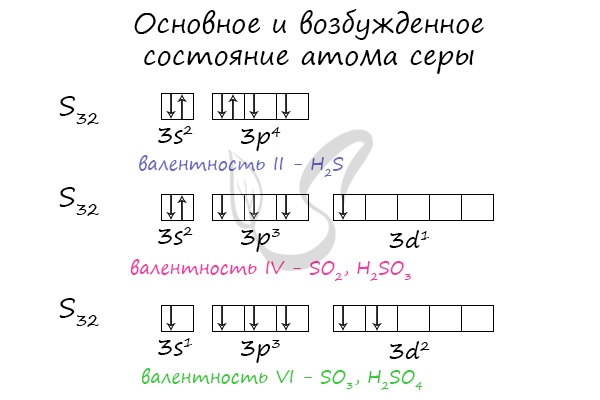
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
В местах вулканической активности встречаются залежи самородной серы.
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S, SO2.
Серу можно получить разложением пирита
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
Сера вступает в реакции диспропорционирования с щелочами.
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные ванны).
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит от соотношения основания и кислоты).
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
В промышленных условиях сернистый газ получают обжигом пирита.
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота, распадающаяся на сернистый газ и воду.
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Диссоциирует в водном растворе ступенчато.
С сильными восстановителями сернистая кислота принимает роль окислителя.
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.