серозометра что это такое у женщин как лечить
Лечение гиперплазии эндометрия матки
Утолщение внутреннего маточного слоя под воздействием гормонов с изменением структуры ткани. Чаще встречается у женщин после 35-40 лет. Лечение гиперплазии эндометрия матки – компетенция врача-гинеколога. Основной фактор риска гиперплазии – чрезмерное влияние прогестерона на рост клеток эндометрия. Толщина слоя продолжает увеличиваться в нехарактерную фазу менструального цикла, что приводит к формированию гиперплазии. При наличии диагноза необходимо постоянное медицинское наблюдение и своевременное лечение.
Бызова Татьяна Евгеньевна
Михальчук Диана Васильевна
Покшубина Светлана Дмитриевна
Заведующая отделением, акушер-гинеколог высшей квалификации, хирург-гинеколог
Ступина Светлана Вадимовна
Зарайская Зоя Петровна
Врач-гинеколог высшей квалификации
Основные факторы роста эндометрия
Основная причина развития гиперплазии – дисбаланс гуморальной регуляции в женском организме. Также существуют факторы, способствующие развитию болезни:
Гиперплазия эндометрия полости матки чаще всего возникает на фоне половых изменений. Патологическое утолщение эндометрия, связанное с психосоматикой, встречается реже и связано с активацией гормонов стресса.
Репродуктивная функция очень важна для каждой женщины. Для того, чтобы сохранить здоровье как можно дольше, необходимо регулярно посещать врача-гинеколога. Рекомендуется проходить гинекологическое обследование не реже 2 раз в год. При появлении настораживающих симптомов – немедленно проконсультироваться у специалиста.
Гиперплазия в подростковом возрасте и менопаузе
У девочек в подростковом возрасте встречаются нарушения со стороны гипоталамо-гипофизарной системы. Это влечет за собой нарушение созревания фолликулов и ведет к их преждевременной атрезии. Атрезия фолликула – это процесс обратного развития путем рассасывания и замещения соединительной тканью. В норме в яичниках вырабатываются фолликулы, имеющие разную жизнеспособность.
Как правило, это 1-2 доминантных фолликула, остальные – нежизнеспособные клетки. На фоне гормонального сбоя все клетки, вырабатываемые яичниками, претерпевают преждевременную атрезию. В результате нарушается последовательность созревания и отторжения эндометрия, что приводит к его гиперплазии. В подростковом возрасте обычно встречается гиперплазия эндометрия матки без атипии.
В период менопаузы происходит угасание детородной функции. Концентрация половых гормонов существенно снижается. В этот период вероятность утолщения эндометрия достаточно велика. Характерны нерегулярные менструации или их отсутствие, на фоне которого вдруг появляются кровянистые выделения в середине цикла, схваткообразные боли внизу живота и другие настораживающие симптомы. Если замечены подобные признаки гиперплазии эндометрия, лучше решение – обратиться к гинекологу для консультации и возможного лечения.
Виды гиперплазии эндометрия
В зависимости от механизма развития патологии выделяют несколько типов гиперплазии:
Железистый тип – активное деление железистых клеток с сохранением выделительной способности. Происходит расширение просвета трубчатых желез, которые расположены группами. Данная форма носит доброкачественный характер. Атипичная железистая гиперплазия эндометрия матки формируется редко. Как правило, заболевание протекает легко, и также легко лечится.
Кистозный тип – очень похож на железистую гиперплазию. Железы значительно увеличиваются в размерах, их клетки стремительно делятся. Существенным отличием является то, что железа изнутри покрыта эпителием нормального строения. Кистозный эндометрий способен перерождаться в раковую ткань. Именно поэтому рекомендуется своевременное лечение гиперплазии такого вида.
Очаговая гиперплазия – характерно наличие гормоночувствительных очагов эндометрия, которые начинают активно разрастаться. Диаметр очагов составляет от нескольких миллиметров до десятков сантиметров. Локальная гиперплазия эндометрия матки может перерождаться в раковый процесс в местах формирования очагов.
Смешанная гиперплазия эндометрия – присутствуют признаки и железистой и кистозной формы роста эндометрия. Структура клеток напоминает пузырь. Это связано с затрудненным оттоком слизистого отделяемого эндометрия. Формируется под влиянием эстрогенов.
Аденоматоз, или гиперплазия эндометрия матки с атипией наиболее опасное перерождение эндометрия. В половине случаев при несвоевременном лечении гиперплазии процесс переходит в злокачественный. В структурах тканей происходит активное деление, мутация, перестройка ядра. В этом случае показан радикальный метод лечения – удаление матки.
Симптомы гиперплазии эндометрия
Первая группа симптомов напрямую связана с маткой и ее функциями. В 98% случаев в клинической картине присутствует симптоматика, связанная с кровотечениями:
Вторая группа симптомов гиперплазии носит общий характер и почти всегда сопровождает гиперплазию эндометрия наряду с кровотечениями:
При появлении описанных симптомов гиперплазии необходимо обратиться к врачу гинекологу для квалифицированного лечения.
Женская матка – это мышечный орган, имеющий небольшие размеры (в среднем не более 5-7 см). Во время беременности она увеличивается в несколько раз, а через несколько недель после родов сокращается до прежних размеров. Медицине известны множество случаев, когда при обследовании женщины выявляются две матки. Это происходит из-за сбоя в эмбриональном развитии плода. Во внутриутробном периоде орган формируется из двух трубок, которые, соединяясь, образуют один полый. Иногда по каким-то причинам этого не происходит и обе трубки формируются в две отдельных матки.
Диагностика гиперплазии эндометрия
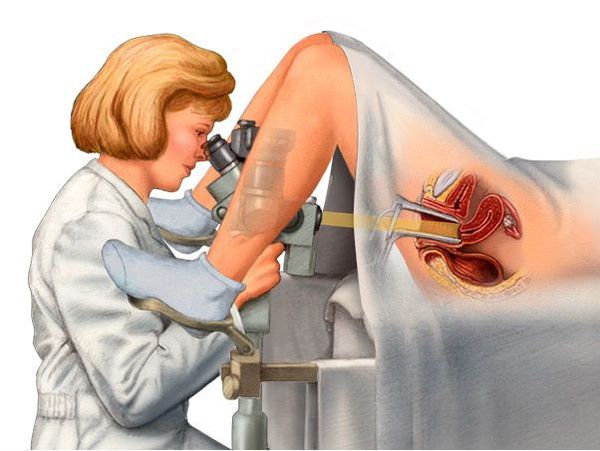
Для подтверждения диагноза и определения наиболее оптимального пути лечения применяется несколько методов. Среди них – ультразвуковое исследование, эхосальпингография, гистероскопия, выскабливание полости матки при гиперплазии эндометрия и другие. Ниже об основных видах исследований.
УЗИ. Проводится с помощью датчика, который вводится во влагалище. Точный метод исследования, позволяет выявить патологию в 90% случаев. Во время осмотра оценивается толщина слоя, полипозные образования, наличие характерных очагов. Не требует специальной подготовки. Возможно провести в день обращения пациентки к врачу.
Эхосальпингография – исследование маточной полости и труб. С введением специального раствора с контрастным веществом, или без него. Через полость влагалища сканируют состояние органов. Хорошо видны кистозные узлы, очаговые изменения, утолщение слоя, полипы эндометрия.
Биопсия. Забор образцов тканей эндометрия на исследование структуры клеток. Применяется эндоскопическое оборудование. По результатам возможно выявить видоизмененные, потенциально злокачественные клеточные элементы и своевременно начать лечение атипичной гиперплазии эндометрия матки. Забор материала сложный, требует высокой квалификации гинеколога.
Выскабливание. Представляет собой механическое воздействие на эндометрий. Проводится с целью диагностики, а также лечебной целью в случае длительного кровотечения. После выскабливания, удаленные ткани исследуются под микроскопом на предмет онкопатологии. Выскабливание применяется часто, поскольку не требует наличия высокотехнологичной аппаратуры.
Радиоизотопный метод. Внутривенно вводится контрастное вещество, которое накапливается в гиперплазированных очагах эндометрия, что свидетельствует о наличии патологии. Обычно в качестве контрастного вещества используются радиоизотопы фосфора.
Гормональное лечение гиперплазии эндометрия
Лечение гиперплазии эндометрия матки возможно в любом возрастном периоде. Основной принцип – принять своевременные меры и не допустить малигнизации процесса. Терапия включает в себя два основных направления – гормонотерапия и хирургическое вмешательство. В лечении гормональными препаратами существует несколько подходов:
Гормональное лечение гиперплазии эндометрия матки в постменопаузе не всегда оправдано, поскольку детородная функция частично или полностью утрачена.
| Описание | Цена, руб. |
|---|---|
| Биопсия шейки матки сургитроном | 4000 рублей |
| Прием гинеколога с расширенной консультацией | 1800 рублей |
Запишитесь на прием по телефону
+7 (495) 021-12-26 или заполнив форму online
Администратор свяжется с Вами для подтверждения записи.
Конфиденциальность Вашего обращения гарантирована.
Хирургическое лечение гиперплазии эндометрия
Операция в полости матки – инвазивная процедура, применяемая в осложненных ситуациях, когда консервативная терапия неэффективна или не оправдана. Среди щадящих методик лечения выделяют применение лазера для прижигания патологических участков. После лазеротерапии слизистая матки восстанавливается и нормально функционирует. Лечение эффективно при очаговой форме болезни.
Лечение жидким азотом или криодеструкция используется реже, но по эффективности сравнима с лазером. Самой травматичной для женщины считается “чистка” или выскабливание полости. Внутренний слой полностью извлекается из матки с помощью хирургического инструмента – кюретки. Операция проводится под наркозом в стационарных условиях. Лечение гиперплазии эндометрия матки в менопаузе и постменопаузе нередко заканчивается полным удалением матки – гистерэктомией. перед радикальным вмешательством оценивается состояние яичников. Если изменений после лечения нет, удаляют только матку.
Получить квалифицированную консультацию врача-гинеколога можно в нашем медцентре. Гинекологи имеют большой опыт в лечении заболеваний женской репродуктивной системы. Гиперплазия эндометрия матки – это серьезный повод обратиться за медицинской помощью и пройти тщательное обследование. Наша клиника оснащена самым современным оборудованием. Записаться на прием можно по телефону, указанному на сайте, или через форму обратной связи. После администратор подберет наиболее удобное для вас время визита.
Приводим сравнительную таблицу цен на данную процедуру клиник г. Москвы*.
Урогенитальные расстройства в постменопаузе и заместительная гормонотерапия
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если
Изменение демографической структуры общества во второй половине XX в. привело к увеличению в популяции доли женщин старшей возрастной группы. С каждым годом возрастает число женщин, вступающих в период менопаузы. Если 75 лет принять за 100%, то продолжительность препубертатного периода составляет 16%, репродуктивного — 44%, пременопаузального — 7%, а постменопаузального — 33% (H. Нaney, 1986). То есть более трети своей жизни женщина проводит в состоянии дефицита женских половых гормонов. Менопауза, не являясь собственно заболеванием, приводит к нарушению эндокринного равновесия в организме женщины, вызывая приливы, раздражительность, бессонницу, урогенитальные расстройства, а также повышая риск развития остеопороза и сердечно-сосудистых заболеваний. Все эти данные свидетельствуют о необходимости разработки целого ряда медицинских и социальных мер по защите здоровья, сохранению работоспособности и достойного качества жизни женщин пери- и постменопаузального периода.
В последние годы в симптоматологии климактерических нарушений стала лидировать проблема урогенитальных расстройств, что связано с их выраженным отрицательным влиянием на качество жизни женщины в постменопаузе. Частота развития возрастных урогенитальных расстройств достигает 30%. В перименопаузальном периоде урогенитальные нарушения встречаются у 10% женщин, тогда как в возрастной группе 55—60 лет — у 50%. К 75 годам уже 2/3 женщин испытывают урогенитальный дискомфорт, а после 75 лет трудно встретить женщину, у которой не наблюдалось отдельных симптомов урогенитальных расстройств.
Урогенитальные расстройства в климактерии — это симптомокомплекс вторичных изменений, связанных с развитием атрофических и дистрофических процессов в эстроген-зависимых тканях и структурах нижней трети мочеполового тракта, мочевом пузыре, уретре, влагалище, связочном аппарате малого таза и мышцах тазового дна.
Прогрессирующее увеличение с возрастом частоты развития урогенитальной атрофии связывают с развивающимися на фоне эстрогенного дефицита необратимыми возрастными метаболическими изменениями. Влагалище, уретра, мочевой пузырь и нижняя треть мочеточников имеют единое эмбриональное происхождение и развиваются из урогенитального синуса. Это объясняет наличие рецепторов к эстрогенам, прогестерону и андрогенам в мышцах, слизистой оболочке, сосудистых сплетениях влагалища, мочевого пузыря и уретры, а также в мышцах и связочном аппарате малого таза.
Процессы старения урогенитального тракта развиваются в двух направлениях:
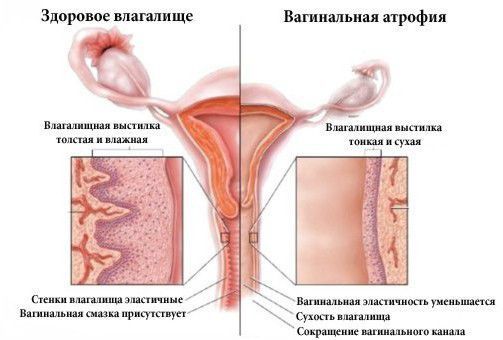
Атрофический вагинит возникает в результате эстрогенного дефицита и характеризуется резким истончением слизистой оболочки влагалища, прекращением пролиферативных процессов во влагалищном эпителии, уменьшением продукции гликогена эпителиальными клетками, снижением или полным исчезновением лактобацилл, повышением влагалищного рН (см. таблицу 1).
Основные клинические проявлениями атрофического вагинита — это сухость и зуд во влагалище, рецидивирующие выделения, диспареуния, контактные кровянистые выделения.
Диагностика атрофического вагинита включает:
К проявлениям атрофического цистоуретрита относятся «сенсорные» или раздражающие симптомы:
Обследование женщин с расстройствами мочеиспускания:
Вычленение симптомов атрофического вагинита и цистоуретрита условно, так как в большинстве случаев они сочетаются. Различные сочетания симптомов атрофического вагинита и цистоуретрита позволили выделить три степени тяжести урогенитальных расстройств (В. Е. Балан, 1997).
К легким урогенитальным расстройствам (16% женщин) относится сочетание симптомов атрофического вагинита и «сенсорных симптомов» атрофического цистоуретрита без нарушения акта мочеиспускания.
К среднетяжелым урогенитальным расстройствам (80% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита и истинного недержания мочи при напряжении.
К тяжелым урогенитальным расстройствам (4% женщин) относится сочетание симптомов атрофического вагинита, цистоуретрита, истинного недержания мочи при напряжении и неудержание мочи.
Итак, установлено, что эстрогенный дефицит является причиной развития урогенитальных нарушений у женщин в климактерии. Проблема лечения урогенитальных расстройств неоднозначна. Акцент ставится на том, какой вид заместительной гормонотерапии (ЗГТ) считать оптимальным. ЗГТ урогенитальных нарушений может осуществляться препаратами, обладающими как системным, так и местным действием. К системной ЗГТ относятся все препараты, содержащие эстрадиол, эстрадиол валерат и конъюгированные эстрогены.
К местной ЗГТ — препараты, содержащие эстриол. Выбор типа ЗГТ для лечения урогенитальных расстройств является индивидуальным и зависит от возраста пациентки, длительности постменопаузы, ведущих жалоб, необходимости лечения климактерического синдрома либо профилактики поздних метаболических нарушений.
Назначение системной ЗГТ должно соответствовать общепринятым правилам с учетом абсолютных и относительных противопоказаний. При назначении ЗГТ пациенткам с урогенитальными нарушениями преследуется цель восстановления нормального состояния местных гормонозависимых структур нижних отделов мочеполовой системы и стимуляции механизмов биологической тканевой защиты.
При решении вопроса о выборе типа препарата для ЗГТ крайне важно определить:
При интактной матке применяется комбинированная терапия препаратами, содержащими эстрогены и гестагены:
У женщин после гистерэктомии системное воздействие обеспечивает монотерапия натуральными эстрогенами в циклическом или непрерывном режиме (эстрофем, прогинова, климара, дивигель, эстрадерм).
Приоритетная роль в выборе ЗГТ расстройств урогенитального тракта, обусловленных снижением функции гонад, принадлежит эстриол-содержащим препаратам, обладающим избирательной активностью в отношении мочеполовой системы. Специфичность действия эстриола определяется особенностями его метаболизма и сродством с соответствующими рецепторными системами. Местный эффект стероидных гормонов реализуется путем пассивной диффузии их в клетки организма. Задерживаясь лишь в клетках чувствительных тканей, они образуют комплексы с цитозольными рецепторами с последующей транслокацией в ядро клетки. Таким путем реализуется действие на уровне генетических структур клетки. Это и определяет специфичность эффекта, свойственного данной ткани.
Ответ тканей на воздействие эстрогенов определяется концентрацией рецепторов, их структурой и свойствами эстрогенов. Эстриол является конечным метаболитом в обмене эстрогенов. Он выводится из организма в конъюгированной форме с мочой и лишь в незначительном количестве экскретируется с калом, в основном в неконъюгированной форме.
При пероральном введении эстриола его максимальная концентрация в плазме крови достигается через 1-2 ч. Попавший в плазму крови эстриол не связывается с глобулином, связывающим половые стероиды, и довольно быстро элиминируется. Эстриол является наименее активным эстрогеном с кратковременным действием.
Установлено, что ткани, чувствительные к эстриолу, широко представлены в нижних отделах урогенитального тракта. Терапия эстриолом способствует развитию и восстановлению влагалищного эпителия, а также приводит к восстановлению основных элементов соединительной ткани — коллагена и эластина. При этом главным в назначении эстриол-содержащих препаратов является минимальное системное действие. Известно, что для стимуляции развития эндометрия связь его рецепторов с эстрогеном должна быть длительной, не менее 8—10 ч. Эстриол же связывается с чувствительными к нему структурами не более чем на 2—4 ч. Такого непродолжительного действия недостаточно для пролиферативной реакции эндометрия, но достаточно для эффективного воздействия на структуры нижних отделов урогенитального тракта. Таким образом, при однократном введении эстриол связывается с ядерным рецептором на непродолжительное время и не вызывает пролиферацию эндометрия, поэтому при его назначении не требуется добавления прогестагенов.
При урогенитальных расстройствах традиционно отдается предпочтение местному введению эстрогенов и именно эстриола (овестин) в мазях и свечах (см. таблицу 2).
В любой форме эстриол-содержащие препараты принимаются один раз в сутки. Не рекомендуется сочетание системных и местных форм препарата.
Выбор терапии зависит также от степени тяжести урогенитальных расстройств.
При легкой степени тяжести урогенитальных расстройств применяются препараты эстриола (свечи, крем) ежедневно или три раза в неделю, в зависимости от степени выраженности клинических симптомов. При сочетании явлений атрофического вагинита или атрофического цистоуретрита с климактерическим синдромом назначаются препараты для системной ЗГТ.
При средней степени тяжести урогенитальных расстройств проводится сочетанная терапия (системная и местная) не менее шести месяцев для нормализации уродинамических показателей.
При тяжелой степени урогенитальных расстройств в случае имеющихся показаний к системной ЗГТ проводится комбинированная терапия препаратами для системной ЗГТ в сочетании с местным введением препаратов эстриола и одного из препаратов аддитивного воздействия, обладающих избирательным действием на холинергические (парасимпатические) и адренергические (симпатические) или мускариновые рецепторы, расположенные в мышечной стенке мочевого пузыря и различных структурах урогенитального тракта: гладкомышечной мускулатуре уретры и мышцах тазового дна, участвующих в создании уретральной поддержки. Комбинированную терапию необходимо проводить в течение шести месяцев и более, после чего вопрос о типе терапии решается индивидуально в отношении каждой пациентки (см. таблицу 3).
 |
| Таблица 3. Схема лечения урогенитальных расстройств. |
Такая система дифференцированной ЗГТ позволяет повысить качество жизни больных с урогенитальными расстройствами на 60—70%.
Таким образом, представленные данные позволяют говорить о ЗГТ как об основной терапии урогенитальных нарушений в постменопаузе.
В связи с прогрессирующим характером урогенитальных расстройств преимущество отдается профилактическому назначению ЗГТ и ее долговременному применению. ЗГТ урогенитальных расстройств должна назначаться длительно, практически пожизненно, и в этой ситуации на помощь приходит именно местная терапия эстриолом.
На сегодняшний день современная медицина располагает достаточно широким выбором хороших препаратов для ЗГТ и опытом их применения, свидетельствующим о том, что преимущества назначения ЗГТ заметно преобладают над риском развития побочных эффектов. Все это дает основание рекомендовать широкое применение ЗГТ для профилактики и лечения урогенитальных нарушений в пери- и постменопаузе с целью улучшения качества жизни и сохранения работоспособности женщин, вступающих в этот «осенний» период.
А. Л. Тихомиров, доктор медицинских наук, профессор
Ч. Г. Олейник, кандидат медицинских наук
МГМСУ, Москва
Что такое постменопауза? Причины возникновения, диагностику и методы лечения разберем в статье доктора Симаниной Светланы Викторовны, гинеколога со стажем в 21 год.
Определение болезни. Причины заболевания
Постменопауза — это один из периодов угасания репродуктивной функции, который начинается после менопаузы и длится до 65-70 лет или до конца жизни. Этот этап требует от женщины особого внимания к состоянию своего здоровья, так как в это время её организм подвержен развитию различных заболеваний.
Пременопауза — это период, когда месячные становятся нерегулярными. Он может длиться несколько лет до наступления последней менструации.
Пременопауза может наступить в любом возрасте за 1-3 года до менопаузы. Возраст начала данного периода зависит от генетических и индивидуальных особенностей женского организма. На этапе пременопаузы у женщины начинают проявляться вазомоторные и эмоционально-психические расстройства: появляются приливы, отмечается неустойчивость настроения, изменяется гормональный профиль, который определяется по анализам крови. Как правило, в это время начинает повышаться уровень ФСГ — гормона гипофиза, стимулирующего работу яичников. Уровень эстрогенов может оставаться в норме за счёт усиленной выработки ФСГ.
Так как яичники начинают неравномерно вырабатывать женские половые гормоны, цикл становится нерегулярным, а со временем полностью прекращается. Это говорит о том, что процесс созревания и выхода яйцеклетки уже не происходит.
Хаотичный выброс гормонов в период пременопаузы может приводить к различным женским заболеваниям:
Менопауза — это период, при котором менструации отсутствуют на протяжении одного года. Как правило, менопауза развивается в возрасте 50-55 лет. Наличие менструальноподобных кровянистых выделений в более позднем возрасте может свидетельствовать о гинекологической патологии, порой очень серьёзной, такой как рак гениталий. Это повод немедленно обратиться к врачу.
Симптомы постменопаузы
Все симптомы постменопаузы, сопровождаемой климаксом, можно разделить на три большие группы:
Вазомоторные симптомы особенно выражены в первые несколько лет постменопаузы. К ним относятся:
Гипертония может носить «кризовый» характер с ярко выраженной психоэмоциональной окраской. Она сопровождается ознобами, сердцебиением, перебоями (аритмией), затруднением дыхания.
Другим атипичным признаком постменопаузы является климактерическая миокардиодистрофия, которая сопровождается появлением боли в груди. Взаимосвязь между выраженностью такой боли и данными ЭКГ практически отсутствует: даже при выраженном болевом синдроме ЭКГ картина изменения либо незначительные, либо вовсе не выявляются.
Пациентки с таким нарушением обычно обращаются к терапевту с подозрением на ишемическую болезнь сердца. Но в отличие от ИБС, боли в сердце при климаксе постоянные и поддаются лечению гормональными препаратами.
Урогенитальные расстройства встречаются более чем у 50 % женщин старше 55 лет. К таким расстройствам относятся:
Женщины чаще всего стесняются говорить об этих симптомах. Однако умалчивать о них во время приёма не стоит, так как они могут повлиять на постановку диагноза и тактику лечения.
К кожным признакам наступления постменопаузы относится резкое старение кожи — она становится сухой и морщинистой. Также сохнут слизистые оболочки, наблюдается ломкость ногтей, сухость и выпадение волос. Все эти изменения связаны с нехваткой эстрогенов, которая снижает образование коллагена в соединительной ткани.
У некоторых женщин усиливается рост волос на лице и снижается тембр голоса. Такие изменения вызываются усиленной выработкой андрогенов в яичниках при условии дефицита эстрогенов.
К поздним обменным нарушениям относятся:
Патогенез постменопаузы
Со временем функцию выработки эстрогенов для поддержания обменных процессов в организме берут на себя надпочечники. Также в метаболизм эстрогенов включается жировая ткань. Поэтому у женщин в постменопаузе преобладают такие фракции эстрогенов, как эстрон и эстриол. Однако компенсаторные возможности организма у всех женщин разные. Этим и объясняется разнообразие и выраженность клинических проявлений в постменопаузе.
Классификация и стадии развития постменопаузы
В зависимости от преобладания тех или иных возрастных проявлений постменопаузу принято делить на два периода:
Эмоционально-психические проявления обычно появляются ещё до наступления постменопаузы и беспокоят женщину в течение года после её окончания. Вазомоторные симптомы в виде приливов и других соматических проявлений присоединяются в самом начале постменопаузы и могут сохраняться в течение 3-5 лет.
Спустя 2-5 лет от начала постменопаузы проявляются урогенитальные симптомы в виде сухости влагалища, неприятных ощущений при половом акте, частом мочеиспускании и недержании мочи. Также в этот период начинаются изменения со стороны кожи, волос и ногтей.
В позднюю менопаузу на первый план выходят обменные нарушения в виде остеопороза, атеросклеротических поражений сосудов, нарушения мозгового кровообращения, болезни Альцгеймера и пр. Эти нарушения являются самостоятельными заболеваниями, требующими специфического лечения. Остеопороз, как правило, развивается постепенно и никак себя не проявляет. Его симптомы становятся заметными только спустя 10-15 лет после завершения менопаузы.
Тяжесть течения климактерического синдрома, который сопровождает постменопаузу, зависит от количества приливов в день. Согласно классификации учёного-гинеколога Е. М. Вихляевой, выделяют три степени тяжести климакса:
Осложнения постменопаузы
У женщин с тяжёлыми приливами повышается риск развития гипертензии и сердечно-сосудистых заболеваний. Так как сосудистый тонус становится неустойчивым, снижается стрессоустойчивость, в крови повышается уровень холестерина, что в итоге может привести к развитию ишемической болезни сердца, нарушению мозгового кровообращения и деменции.
Одним из осложнений поздней постменопаузы является остеопороз. Он развивается из-за недостатка эстрогенов, который нарушает кальциевый обмен в организме. Кости становятся хрупкими, переломы возникают легко, буквально «на ровном месте».
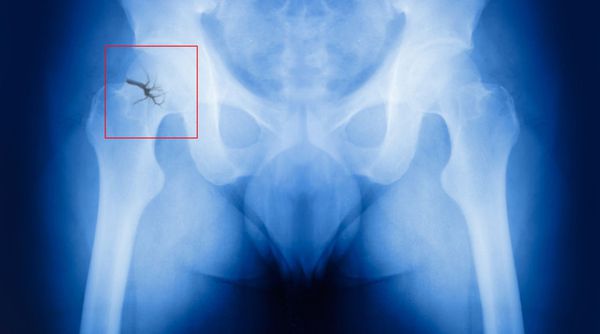
Самый опас ный перелом в постменопаузе — перелом шейки бедра. Он никогда не срастается самостоятельно, т. е. без реконструктивных операций, и часто приводит к инвалидизации больных.
Замечено, что развитию остеопороза особенно подвержены худощавые пациентки. Это связано с дефицитом жировой ткани, которая принимает участие в синтезе эстрогенов. Поэтому у женщин с умеренно развитой подкожно-жировой клетчаткой уровень эстрогенов выше.
Диагностика постменопаузы
Обязательным является обследование на раковые клетки — цитология и кольпоскопия. Данные исследования проводятся раз в год в связи с высокой частотой развития рака шейки матки и вульвы в период постменопаузы.
Цитология — это исследование мазка, взятого с поверхности шейки матки и цервикального канала на раковые клетки. Предпочтение следует отдавать жидкостной цитологии, при которой биоматериал помещается не на стекло, как при традиционной цитологии, а в специальный контейнер с консервирующей жидкостью. Её информативность приравнивается к биопсии шейки матки.
Кольпоскопия — это исследование шейки матки под микроскопом с обработкой шейки матки кислотным реактивом и красителями. Оно позволяет выявить морфологически изменённые клетки и участки на слизистой шейки матки и вульвы.
Лечение постменопаузы
Лечение расстройств в постменопаузе должно начинаться с общих рекомендаций по изменению образа жизни : правильное питание, физическая активность, полноценный сон и отдых, устранение негативных факторов окружающей среды.
В последние десятил етия для лечения климактерических расстройств активно используются гормональные препараты. Они обладают рядом положительных эффектов:
Гормональное лечение проводи тся не менее одного года (в среднем длится 3-5 лет). Если приливы не возвращаются, то приём гормональных препаратов следует прекратить.
Среди средств для гормонального лечения постменопаузальных расстройств выделяют двуфазные препараты: цикло-прогинова, дивина, климен, климонорм и фемостон. Они рекомендуются женщинам, начиная с пременопаузы, т. е. когда менструации ещё не закончились, но возникают нерегулярно. При наступлении постменопаузы показаны препараты для непрерывного режима: фемостон конти, фемостон мини, анжелик, индивина, климодиен и клиогест.
В последнее время для лечения климактерических расстройств в постменопаузе и профилактики остеопороза применяется препарат ливиал (тиболон, ледибон). Он оказывает эстрогеноподобное действие на те органы и ткани, которые испытывают дефицит эстрогенов. Особенно данный препарат подходит для пациенток с депрессией. Его можно принимать длительно.
Альтернатива гормонотерапии
В комплексном лечении постменопаузальных нарушений также используется психотерапия. Она помогает справиться пациентке с психологическими трудностями, возникающими во время постменопаузы, и предупредить развитие некоторых психосоматических осложнений.
Прогноз. Профилактика
Профилактика негативных последствий постменопаузы в первую очередь должна включать в себя изменение общего образа жизни:
Правильное питание предполагает низкоуглеводную диету, богатую растительной клетчаткой, фрукты, хлеб из муки грубого помола, злаковые и молочные продукты, богатые кальцием. Необходимо ограничить употребление животных жиров и соли. Желательно два раза в неделю устраивать «рыбные» дни.