синдром гудпасчера что это такое простыми словами
Синдром гудпасчера
Что провоцирует / Причины синдрома гудпасчера:
Этиология заболевания неизвестна. Возникновение его иногда связывают с вдыханием летучих углеводородов и других органических растворителей. Ряд авторов рассматривают синдром Гудпасчера как вариант течения идиопатического гемо- сидероза легких, что косвенно подтверждается существованием клинически и патоморфологически переходных состояний. В отличие от коллагенозов, при синдроме Гудапасчера отсутствуют явления васкулита. Предположение о вирусной природе не имеет достаточных фактических подтверждений [Spencer Н„ 1977].
Патогенез (что происходит?) во время синдрома гудпасчера:
Вопрос о первичной локализации заболевания окончательно не решен, хотя поражение легких, как правило, предшествует поражению почек.
Патологическая анатомия. При гистологическом исследовании выявляются геморрагический некротизирующий альвео- лит (изменения в легких, аналогичные идиопатическому гемо- сидерозу легких) и нефрозоиефрит с очаговыми внутрнкапил- лярными тромботическими изменениями и развитием гломеру- лярного фиброза.
Симптомы синдрома гудпасчера:
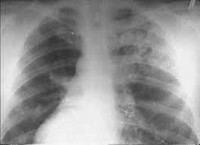
Наиболее характерными признаками синдрома Гудпасчера являются кровохарканье (повторные легочные кровотечения) и анемия. К ним часто присоединяются прогрессирующая одышка, кашель, боли в грудной клетке, похудание. На рентгенограммах выявляются мелкосетчатая деформация легочного рисунка, мелкоочаговые изменения. Может повышаться температура тела. К этим, как правило, первым признакам синдрома Гудпасчера вскоре добавляются симптомы поражения почек: протеинурия, гематурия, цилиндрурия, повышение уровня остаточного азота в крови, периферические отеки. Прогрессирует гипохромная железодефицитная анемия. При присоединении вторичной инфекции отмечаются соответствующие изменения в формуле крови.
Течение болезни неуклонно прогрессирующее и заканчивается смертью вследствие повторных легочных кровотечений или азотемической уремии.
Лечение синдрома гудпасчера:
Некоторое замедление прогрессирования процесса может дать раннее назначение кортикостерои- дов и иммуиосупрессантов (азатиоприн, циклофосфамид, 6-меркаптопурин и др.). Повторный гемодиализ несколько продлевает жизнь больным. При некупирующейся уремии (после предварительного гемодиализа) иногда производят нефрэктомию (с последующей пересадкой почек), что позволяет устранить источник антигенного раздражения. С целью удаления циркулирующих антител в последние годы применяется плазмаферез. Отмечено, что антитела против базаль- ных мембран почечных клубочков перестают определяться в сыворотке крови через 6-8 мес от начала заболевания. Поэтому интенсивная терапия в течение этого периода (кортико- стероиды, иммуносупрессанты, гемодиализ, плазмаферез, нефрэктомия), возможно, позволяет продлить жизнь больного до прекращения аутоантителогенеза.
Симптоматическая терапия включает повторные переливания крови, назначение препаратов железа.
К каким докторам следует обращаться если у Вас Синдром гудпасчера:
Синдром Гудпасчера
Синдром Гудпасчера представляет собой иммуно-воспалительное заболевание мелких сосудов легких и почек.
Симптомы Синдрома Гудпасчера:
Классической триадой, выражающей клинико-патогенетическую сущность этой болезни, являются легочные кровотечения, гломерулонефрит и антитела к антигенам основной мембраны капилляров легких и почек. Заболевание встречается редко и может поражать любой возраст, но чаще болеют молодые мужчины. Конкретные причины неизвестны; не раз описывалось развитие синдрома Гудпасчера после недавно перенесенного гриппа или вдыхания углеводородов. В связи с этим не исключено, что подобные воздействия таким образом изменяют химическую структуру упомянутых выше антигенов основных мембран, что они приобретают аутоантигенные свойства и вызывают продукцию соответствующих антител с патогенными свойствами.
Течение болезни в целом неблагоприятное, хотя и неоднотипное. На первых этапах основной угрозой являются легочные геморрагии, причем нередко больной умирает в результате первого и единственного профузного кровотечения. У ряда переживших это кровотечение может развиться относительная ремиссия легочного процесса, но во многих случаях кровохарканье и легочные геморрагии рецидивируют. Поражение почек у отдельных больных остается относительно нетяжелым, но в большинстве случаев быстро прогрессирует с развитием олигурической почечной недостаточности, приводящей к смерти в течение нескольких месяцев и даже недель. Средняя продолжительность жизни у неадекватно леченных больных составляет менее полугода.
Диагностика Синдрома Гудпасчера:
При дифференциальном диагнозе синдрома Гудпасчера следует иметь в виду, что сочетание легочного кровотечения с выраженной почечной патологией (в том числе с недостаточностью почек) может встретиться при гранулематозе Вегенера, узелковом полиартериите, СКВ, геморрагическом васкулите, криоглобулинемии, эмболии ветвей легочной артерии вследствие тромбоза почечной вены, болезни легионеров и даже при тяжелой недостаточности кровообращения с выраженным застоем в легких и почках. Однако все эти заболевания отличаются от синдрома Гудпасчера по клиническим признакам и отсутствию антител к антигенам базальных мембран.
Лечение Синдрома Гудпасчера:
К каким докторам следует обращаться если у Вас Синдром Гудпасчера:
Синдром Гудпасчера
Синдром Гудпасчера – аутоиммунная патология, характеризующаяся образованием аутоантител к базальным мембранам почечных клубочков и легочных альвеол. Клинически синдром Гудпасчера проявляется рецидивирующими легочными кровотечениями, прогрессирующим гломерулонефритом и почечной недостаточностью. Диагноз синдрома Гудпасчера подтверждается выявлением антител к базальной мембране клубочков (Anti GBM), данными биопсии почек и легких, рентгенологического исследования легких. Лечение синдрома Гудпасчера включает иммуносупрессивную терапию (глюкокортикостероиды, цитостатики), плазмаферез, по показаниям – гемодиализ, трансплантацию почек.
Общие сведения
Причины синдрома Гудпасчера
Этиологические механизмы заболевания достоверно не определены. Клинические наблюдения указывают на связь развития синдрома Гудпасчера с перенесенной вирусной инфекцией (гриппом, вирусным гепатитом А и др.), приемом лекарственных препаратов (карбимазола, пеницилламина), производственными вредностями (вдыханием паров органических растворителей, лаков, бензина), переохлаждением, курением. Отмечена генетическая предрасположенность к данному синдрому у лиц–носителей HLA-DRwl5, HLA-DR4 и HLA-DRB1 аллелей. Описаны семейные случаи синдрома Гудпасчера.
Под воздействием того или иного этиологического фактора, в результате изменения толерантности иммунной системы, в организме начинается выработка аутоантител к базальным мембранам легочных альвеол и почечных клубочков. Предполагается, что в роли аутоантигена выступает структурный компонент а-3 цепи коллагена IV типа, присутствующий в базальных мембранах легочных и почечных капилляров. Сформировавшиеся антитела (GВМ-антитела) в присутствии С3-комплемента связываются с антигенами; образовавшиеся иммунные комплексы откладываются вдоль базальных мембран, индуцируя иммуно-воспалительное поражение почечных клубочков (гломерулонефрит) и альвеол (альвеолит). В развитии аутоиммунного воспаления большая роль принадлежит активации клеточных элементов (Т-лимфоцитов, эндотелиоцитов, моноцитов, альвеолярных макрофагов, полиморфноядерных лейкоцитов), цитокинов (инсулиноподобного, тромбоцитарного факторов роста, факторов некроза опухоли, интерлейкина-1), свободных радикалов, протеолитических ферментов и других факторов, повреждающих почечную и легочную ткань.
Патоморфологическими субстратами синдрома Гудпасчера служат геморрагический некротизирующий альвеолит и нефрозонефрит. При гистологическом исследовании почечной ткани обнаруживается пролиферативно-мембранозный, пролиферативный или некротизирующий гломерулонефрит, склероз клубочков и фиброз почечной паренхимы. Морфологическое исследование легочной ткани выявляет капиллярит межальвеолярных перегородок, легочные инфильтраты, гемосидероз, пневмосклероз.
Симптомы синдрома Гудпасчера
Выделяют три варианта клинического течения синдрома Гудпасчера: злокачественный, умеренный и медленный. Для злокачественного течения характерны рецидивирующая геморрагическая пневмония и стремительно прогрессирующий гломерулонефрит. При втором типе легочно-почечный синдром развивается медленнее и выражен умеренно. При третьем варианте синдрома Гудпасчера преобладают явления гломерулонефрита и ХПН; легочные проявления развиваются поздно.
Вскоре к легочным проявлениям добавляется почечная симптоматика: гематурия, олигурия, периферические отеки, артериальная гипертензия. У 10-15% пациентов синдром Гудпасчера манифестирует с клинических признаков гломерулонефрита. Во многих случаях течение заболевания сопровождается миалгиями, артралгиями, геморрагиями кожи и слизистых оболочек, интраретинальными кровоизлияниями, перикардитами.
Диагностика синдрома Гудпасчера
При осмотре пациентов с синдромом Гудпасчера обращает на себя внимание бледность кожных покровов, пастозность или отеки лица. В легких выслушиваются сухие и влажные хрипы, количество которых увеличивается в момент кровохарканья и после него. В общем анализе крови обнаруживается гипохромная анемия, анизоцитоз, пойкилоцитоз, лейкоцитоз, резкое увеличение СОЭ. Для общего анализа мочи характерна протеинурия, цилиндрурия, эритроцитурия; проба по Зимницкому выявляет изогипостенурию. В биохимическом анализе крови определяется нарастание уровня креатинина, мочевины, серомукоида; снижение концентрации железа. Для синдрома Гудпасчера типично обнаружение большого количества эритроцитов, сидерофагов и гемосидерина в общем анализе мокроты.
Наиболее чувствительным и специфичным методом диагностики синдрома Гудпасчера служит определение антител к базальной мембране клубочков (Anti-GBM) с помощью ИФА или РИА. На рентгенограммах легких выявляются множественные очаговые тени. Морфологическое подтверждение синдрома Гудпасчера основывается на данных биопсии легких и почек. Вспомогательное значение имеют результаты инструментальной диагностики: спирометрии, УЗИ почек, ЭКГ, ЭхоКГ.
Лечение и прогноз синдрома Гудпасчера
В остром периоде синдрома Гудпасчера показано назначение пульс-терапии метилпреднизолоном или комбинированной пульс-терапии (метилпреднизолон+циклофосфан) с последующим переводом на поддерживающую терапию после достижения клинико-лабораторной и рентгенологической ремиссии. С целью элиминации циркулирующих иммунных комплексов проводится плазмаферез. Симптоматическая терапия синдрома Гудпасчера включает переливания эритроцитарной массы и плазмы крови, назначение препаратов железа. При развитии терминальной почечной недостаточности применяются сеансы гемодиализа. Возможно выполнение нефрэктомии с последующей трансплантацией почки, однако это не исключает рецидива некротизирующего гломерулонефрита в трансплантате.
Течение синдрома Гудпасчера неуклонно прогрессирующее; прогноз – мало обнадеживающий. Гибель пациентов происходит, как правило, вследствие профузных легочных кровотечений, тяжелой почечной или дыхательной недостаточности. При злокачественном варианте летальный исход наступает в считанные недели; в остальных случаях средняя продолжительность жизни колеблется от нескольких месяцев до 1-3 лет. В литературе описаны единичные спонтанные ремиссии синдрома Гудпасчера.
Синдром Гудпасчера
Синдром Гудпасчера (СГ) — редкое заболевание, в основе которого лежит аутоиммунная реакция с выработкой организмом аутоантител главным образом к базальным мембранам клубочковых капилляров почек и альвеол легких. Клинически проявляется симптомами быстропрогрессирующего гломерулонефрита и геморрагического пульмонита в сочетании с легочным кровотечением (кровохарканьем).

В 1958 г. М. Stanton и J. Tange сообщили о девяти случаях сочетанного поражения легких и почек, характеризовавшегося рецидивирующими легочными кровотечениями, гемосидерозом легких и гломерулонефритом, с летальным исходом через несколько месяцев от начала заболевания. Они ввели термин «синдром Гудпасчера».
Распространенность заболевания составляет 0,5 на 1 млн населения (F. Mercel et al., 1998). К 1984 г. в мировой литературе описано 280, в отечественной — 21 случай этого недуга (у 8 женщин и 13 мужчин) (Ю.М. Мостовой и соавт., 1984).
Этиология СГ до настоящего времени не известна. Сам Гудпасчер связывал развитие заболевания с небактериальным воспалением. Большинство авторов считают, что возникновение его связано с вирусными и бактериальными инфекциями. СГ может развиваться на фоне различных заболеваний, под воздействием физических и химических факторов внешней среды (действие органических растворителей, паров бензина, лаков, введение D-пеницилламина).
В настоящее время основной теорией патогенеза СГ, как и диффузных болезней соединительной ткани, является аутоиммунная. Суть ее заключается в следующем. Под воздействием этиологических факторов базальные мембраны легочных альвеол и почечных клубочков либо подвергаются антигенной трансформации, либо в результате срыва толерантности иммунной системы стимулируют выработку антител к неизмененным структурным элементам (антигены) базальных мембран легочных альвеол и почек (Е.J. Lewis и соавт., 1971).
При вирусной, бактериальной инфекции возможно наличие общих антигенов как в базальных мембранах клубочковых и легочных капилляров, так и в клеточных структурах бактерий, что приводит к выработке в организме перекрестно реагирующих антител (Н.Е. Ярыгин и соавт., 1980). Продуцируемые иммунной системой аутоантитела к базальным мембранам преимущественно легочных альвеол и почечных клубочков прямо связываются с антигеном мембран в присутствии С3-комплемента с последующим развитием воспалительного процесса, что и обусловливает морфологическую и клиническую картину заболевания.
Теория аутоиммунного генеза СГ подкрепляется данными иммунофлюоресцентного и электронно-микроскопического исследования, с помощью которого выявляют патогномоничный для данного заболевания линейный характер отложений иммунных депозитов на базальных мембранах капилляров в легких и в почечных клубочках. Для СГ характерно также повышение в крови больных титра антител к гломерулярной базальной мембране.
При патологоанатомическом исследовании обнаруживают преимущественно поражение клубочков, соответствующее сегментарному очаговому, пролиферативно-мембранозному, пролиферативному (чаще экстракапиллярному) или некротизирующему гломерулонефриту с развитием склероза почечных клубочков и реактивным разрастанием на месте погибших нефронов соединительной ткани.
При электронно-микроскопическом и иммунофлюоресцентном исследовании в качестве характерных признаков СГ описывают утолщение и гомогенизацию базальных мембран, пролиферацию и отек эндотелиальных клеток, линейные отложения (депозиты), состоящие из иммуноглобулинов G и M, C3-, С4-фракций комплемента, которые при СГ располагаются внутри базальных мембран, а не субэпителиально или субэндотелиально, как при системной красной волчанке и постстрептококковом гломерулонефрите.
Наиболее типичной гистологической картиной для легочной патологии при СГ является капиллярит межальвеолярных перегородок, а затем некротизирующий альвеолит. В паренхиме легких, как правило, развивается гемосидероз, степень выраженности которого прямо зависит от сроков заболевания и распространенности геморрагии, возникающий при очередном рецидиве болезни. В патологический процесс вовлекаются бронхи и бронхиолы.
При быстром развитии СГ, когда патологический процесс в легких характеризуется массивностью поражения, обнаруживаются преимущественно свежие изменения в виде мелких и обширных кровоизлияний, изолированных или сливающихся пневмонических фокусов и полостей распада. Проявления гемосидероза и склероза легких у таких больных выражены слабо. Если же легочная патология прогрессирует медленно, на первое место выступает очаговый или диффузный гемосидероз и фиброз ткани органа.
Степень тяжести поражения легких и почек у больных на разных этапах заболевания различна. В одних случаях преобладает патология почек, в других — поражение легких, в третьих легочные и почечные изменения одинаково тяжелы. Превалирующая в начале болезни легочная патология может затем смениться более серьезными нарушениями со стороны почек, и наоборот.
Клиническая картина
СГ отмечается в основном у мужчин в возрасте 20-30 лет, хотя болезнь описана также у лиц пожилого возраста, у детей и подростков. В большинстве случаев заболевание развивается внезапно после острой респираторной вирусной инфекции и проявляется симптомами поражения легких: кровохарканием или легочным кровотечением, одышкой, кашлем, болью в грудной клетке. Эти признаки возникают на фоне общей слабости, повышенной температуры, похудения.
Несколько позже отмечаются симптомы поражения почек, которые могут проявляться микрогематурией (но может отмечаться и макрогематурия), протеинурией, цилиндрурией. Быстро нарастают признаки почечной недостаточности на фоне олигурии и даже анурии. В более поздних стадиях может развиваться нефротический синдром, когда суточная протеинурия достигает 4-5 г.
Один из основных признаков СГ — возникновение уже в ранние сроки заболевания признаков железодефицитной анемии, которая развивается вследствие частого кровохаркания (легочного кровотечения) и геморрагии в легочные альвеолы.
При осмотре больного отмечают резкую бледность кожных покровов без признаков цианоза. При аускультации в легких выслушиваются сухие и влажные (особенно в период легочного кровотечения) хрипы на фоне жесткого дыхания, преимущественно в прикорневой зоне. При перкуссии легочный звук не изменен. Пульс частый, обычно малого наполнения, мягкий. Артериальное давление у большинства больных в пределах нормы. Печень и селезенка не пальпируются. В редких случаях могут отмечаться геморрагические изменения кожи и слизистых оболочек, гепатомегалия, признаки сердечной декомпенсации, перикардиты, как исключение — спленомегалия (Г. Маждраков, 1983).
Указанный порядок возникновения симптомов при СГ является классическим. Однако ряд авторов приводят менее типичные варианты болезни, когда выраженные признаки могут долгое время отсутствовать (у части пациентов не наблюдается кровохаркания, гематурии, а на первое место в начале заболевания выходят нехарактерные симптомы — артралгия, диспептические явления и др.). Естественно, что установить точный диагноз в таких случаях очень сложно.
Уже на ранних стадиях заболевания, кроме гипохромной анемии с ретикулоцитозом, может отмечаться умеренный лейкоцитоз. Скорость оседания эритроцитов обычно значительно повышена и достигает 50-70 мм/ч. При нормальной резистентности эритроцитов срок их жизни существенно сокращается (в тяжелых случаях до 5-12 дней). Реакция Кумбса как правило отрицательная. При биохимическом исследовании крови нередко отмечается снижение содержания сывороточного железа до 10 ммоль/л, даже на фоне лечения препаратами железа. Проба на С-реактивный белок положительная. Гемокоагуляционные пробы обычно в пределах нормы. LE-клеток не обнаруживают.
В моче уже в ранний период болезни выявляют белок — от следов до 10 г/л. В осадке, как правило, обнаруживают эритроциты, реже — лейкоциты, зернистые и эритроцитарные цилиндры. С наступлением почечной недостаточности наблюдаются характерные для этого состояния биохимические изменения крови (гиперазотемия и др.). В мокроте выявляют сидерофаги.
При рентгенографии легких чаще всего отмечаются диффузные двусторонние облаковидные затемнения, преимущественно в нижних долях или прикорневой и срединной локализации, которые имеют преходящий характер и могут исчезать спонтанно. В редких случаях они могут сливаться или развиваются с одной стороны. Диффузное «пылеобразное» затемнение в легких отмечается во время легочного кровотечения и связано с интраальвеолярной геморрагией.
Диагностика
Предположить наличие СГ можно при детальной оценке клинической картины заболевания: сочетание легочной геморрагии с быстропрогрессирующим гломерулонефритом при отсутствии признаков системного васкулита.
Диагноз более достоверный, если наряду с характерными клиническими признаками при иммунофлюоресцентном исследовании биоптата почечной ткани на базальных мембранах клубочков выявляют линейные депозиты, включающие иммуноглобулины G или М и С3-фракцию комплемента. Обязательным для подтверждения диагноза является обнаружение в крови антител к клубочковым базальным мембранам.
Дифференциальный диагноз
Во всех случаях легочных кровотечений, причину которых (бронхоэктазы, рак бронха и др.) установить не удается, следует предполагать наличие СГ, даже если еще нет симптомов поражения почек.
СГ необходимо дифференцировать с гломерулонефритом, особенно в тех случаях, когда последний в результате уремии может осложняться легочными кровотечениями, с идиопатическим гемосидерозом легких, системной красной волчанкой, болезнью Шенлейна-Геноха, узелковым периартериитом, гранулематозом Вегенера, синдромом Чарга-Стросса, криоглобулинемией, микроскопическим полиангиитом. Иногда СГ приходится дифференцировать с милиарным туберкулезом легких, вирусной пневмонией, лептоспирозом, первичными или метастатическими опухолями с поражением почек и легких и т.д.
Лечение
Протокол лечения СГ предложен еще в 1976 г. и является основой терапии, применяемой при этом заболевании во всем мире (Н.А. Мухин и соавт., 2002).
• Преднизолон — 1 мг/кг массы тела.
• Циклофосфамид — 3 мг/кг.
• Плазмаферез — ежедневно в течение 14 дней (обмен 4 л плазмы крови на 5% раствор альбумина или свежезамороженной одногруппной плазмы крови).
• При легочном кровотечении — трансфузия 300-400 мл свежезамороженной плазмы крови.
Современные схемы лечения предусматривают внутривенную капельную пульс-терапию метилпреднизолоном в высоких дозах (3 пульс-дозы по 500 мг) с последующим переходом на прием глюкокортикоида внутрь (1-1,5 мг/кг в сутки) с параллельным применением циклофосфамида (1-2 мг/кг в сутки) и 4-6 курсов плазмафереза. Поддерживающая терапия заключается в постепенном снижении дозы преднизолона до 10-20 мг в сутки, приеме циклофосфамида по 1 мг/кг в сутки в течение 3 мес или циклоспорина А в дозе 3-5 мг/кг в сутки в течение 6-12 мес (F. Merkel et al., 1998; A. Gause, 2003; A.G. Josse et al., 2003).
Обсуждается возможность применения в перспективе иммуноадсорбции и циклоспорина А в качестве монотерапии (A. Gause, 2003). Имеются экспериментальные данные об эффективном применении при СГ анти-CD4+ антител, что позволяет снизить концентрацию антител к клубочковой мембране и протеинурию (V. Parsons, 2002; A. Gause, 2003).
Течение и прогноз
Типичный вариант течения СГ характеризуется быстрым прогрессированием заболевания с преобладанием в клинической картине легочной или почечной симптоматики. В короткий срок патология завершается летальным исходом в результате развития почечной недостаточности или легочного кровотечения. Средняя продолжительность жизни составляет 11-12 мес. (В.Л. Бялик и соавт., 1967; В.З. Прохур, А.Ф. Глоба, 1972; Е.А. Смирнов, Г.Н. Колин, 1975).
Реже заболевание отличается относительно медленным прогрессированием легочных изменений и признаков поражения почек. Иногда отмечаются спонтанные ремиссии. Продолжительность жизни колеблется от 2 (В.А. Алмазов и соавт., 1972) до 3-5 и даже 12 лет (И.П. Корзун и соавт., 1976).
При своевременно начатом лечении происходит стабилизация функции почек, снижается титр антител к базальной мембране клубочков, что позволяет перейти на длительную поддерживающую терапию циклофосфамидом в сочетании с преднизолоном в невысоких дозах до проведения программного гемодиализа (Н.А. Мухин и соавт., 2002). По данным D. Jayne (2001), у больных с СГ удавалось сохранять функцию почек в течение 12 лет без заместительной терапии программным гемодиализом.
Имеются единичные сообщения о выздоровлении больных после лечения кортикостероидами, антибиотиками, применения экстракорпорального гемодиализа (Lockwood et al., 1975; Fischman, 1976; Misiani et al., 1978).
Приводим случай собственного наблюдения пациента с СГ, описанного и опубликованного в 1984 г. (Ю.М. Мостовой и соавт., 1984).