синдром хауса что такое
Синдром доктора Хауса: стоит ли резать правду-матку?
В любом обществе обязательно найдётся такой человек, которого хлебом не корми, дай только высказаться об окружающих предельно громко и откровенно. Одна из моих знакомых обожает говорить правду в глаза: «Вам этот цвет не идёт, он вас полнит!», «Боже мой, что за платье! Сколько же вы заплатили за этот кошмар?», «Вам не кажется, что ваша жена флиртует с тем молодым человеком?»
Надо ли говорить, что в обществе её, мягко говоря, не любят. Лично я знаю, что у неё есть масса замечательных качеств. Она, например, всегда поможет в трудной ситуации. Но большинство людей избегают близкого знакомства с ней и, как следствие, не могут наблюдать её с хорошей стороны именно из-за того, что испытывают шок уже в момент первого контакта. Это и понятно, кому понравится, когда ваш собеседник концентрирует своё внимание на ваших недостатках!
Несколько раз я пыталась ей объяснить, что таким образом друзей не завоюешь. «А зачем мне друзья, которые не хотят слышать правду о себе? Что может быть плохого в том, что я честна с людьми? Я ведь не за глаза это всё говорю, а в личной беседе с человеком!» — отвечает она. И всё же мой вопрос, почему она всегда озвучивает только негативные наблюдения, поставил её в тупик. И правда, почему? Неужели у неё нет ни одной положительной мысли об окружающих? Или она считает, что не нужно никого хвалить, а то загордятся, не дай Бог, и совсем общаться перестанут?
Наверное, каждый из нас хотя бы одним глазком смотрел сериал «Доктор Хаус». Итак, доктор Хаус — прекрасный специалист, который просто гениально вникает в суть медицинской проблемы и ставит диагнозы в безнадёжных ситуациях. Несмотря на это, большинство людей, с которыми он сталкивается, от него далеко не в восторге.
Более того, они возмущены и обижены. Ведь доктор Хаус всегда говорит правду в глаза. И это прекрасно, если эта правда, даже высказанная в достаточно жёсткой форме, помогает решить проблему и справиться с заболеванием. Но в другой ситуации, например, где-то на вечеринке, подобное поведение — полная катастрофа.
Если люди хотят отдохнуть и расслабиться, выпить и посмеяться, поболтать ни о чём, им вовсе не нужен «борец за правду», который появится вдруг из ниоткуда, чтобы сделать абсолютно серьёзное заявление: «Вам давно пора скинуть пару килограммов, вы же в это платье уже не влезаете!»
И дело тут не в правде, возможно, килограммы действительно давно пора скинуть. Но всему своё время: люди, настроенные на положительные эмоции, будут возмущены, если кто-то вдруг одарит их эмоциями отрицательными. Не для того они пришли на вечеринку, чтобы выслушивать неприятные вещи, им хочется просто расслабиться и не думать ни о чём серьёзном.
Именно поэтому поведение моей знакомой чаще всего вызывает шок у окружающих. Никто не будет задаваться вопросом, хороший ли она специалист в своей области и есть ли у неё вообще какие-то достоинства. Обычной реакцией её собеседников является желание пуститься в бега. Впрочем, моя знакомая не расстраивается по этому поводу, общение для неё не так важно, как возможность озвучить свои мысли честно и откровенно. Правда, иногда она нарывается на себе подобных и обижается в свою очередь. Кому же хочется услышать неприятную правду о себе?
Чтобы успешно общаться, нам приходится умалчивать многие вещи. Действительно, если мы будем говорить всё, что думаем, вряд ли окружающие будут считать нас приятным собеседником. Люди охотно идут на контакт с теми, кто дарит им положительные эмоции. Комплименты на самом деле очень важны.
Конечно, не нужно намеренно врать и выдумывать что-то не присущее нашему собеседнику. Подобную фальшь не заметит только тот, кто очень любит лесть. Но можно ведь сконцентрироваться не на недостатках, а на достоинствах человека, и подчеркнуть их приятным комплиментом. В этом случае все будут довольны, кроме, пожалуй, моей знакомой. Она-то считает своё поведение абсолютно естественным и уверена, что все должны вести себя подобным образом.
Кстати, сериал про доктора Хауса ей не понравился. И на мой вопрос, не напоминает ли ей поведение доктора Хауса её собственное, она ответила: «Ну вот ещё! Он же садист какой-то, издевается над людьми. А я просто пытаюсь быть честной!»
В любом случае, даже если мы очень трепетно относимся к правде, прежде чем что-либо сказать, нужно пять раз подумать: а уместно ли наше замечание в данной ситуации? Иначе мы рискуем прослыть в глазах окружающих злостным садистом, который издевается над людьми…
Что такое психосоматика и как это лечить?

— В 80—90-е годы прошлого века у нас в институте (Первый Московский государственный медицинский университет имени И. М. Сеченова. — Прим. ред.) работал очень известный психолог профессор Ю. М.Орлов. Ему принадлежала теория «саногенного мышления». Её смысл сводился к тому, что если мыслить правильно, культивировать хорошие эмоции и бороться с плохими, то можно предотвратить множество заболеваний. Надо признать, что для неокрепших умов юных медиков его теория выглядела весьма убедительно…
Могут ли эмоции влиять на здоровье? Определённо да. Быть причиной — нет. Негативные эмоции активизируют симпатическую нервную систему, что, в свою очередь, приводит к повышению артериального давления, увеличению частоты пульса и спазму сосудов. Всем известны истории, когда на фоне, например, испуга или гнева у людей случались инфаркты и инсульты. Повторю: эмоция в этом случае не причина заболевания, а лишь провоцирующий фактор, триггер.
В отдельных случаях негативная эмоция, конечно, может стать и причиной заболевания. Например, если со злости ударить кулаком по стене, можно сломать руку. Вот вам вполне отчётливая причинно-следственная связь. Кстати, не надо забывать и о существовании обратной взаимосвязи. Нередко причиной негативных эмоций становятся хронические телесные страдания. Вспомните Бабу-ягу с костяной ногой — возможно, она была бы очень милой старушкой, если бы не хроническая боль в тазобедренном суставе…
«Все болезни от нервов» — это миф?
Это даже не миф, это просто старая студенческая шутка. Полная цитата звучит так: «Все болезни — от нервов, и только пять — от любви» (имеется в виду пять классических венерических болезней). Впрочем, хронический стресс — действительно доказанный фактор риска развития как минимум сердечно-сосудистых заболеваний. Несколько лет назад при помощи позитронно-эмиссионной томографии (высокоточного исследования, позволяющего изучать обменные процессы в различных тканях) учёные выявили механизмы, трансформирующие стресс в хроническое воспаление, которое, в свою очередь, служит ключевым механизмом развития атеросклероза.
— Однако повторяю снова и снова: стресс не причина болезней, а один из факторов риска, который работает лишь сообща с другими факторами, прежде всего генетическими.
Психосоматическое расстройства: каковы причины и механизмы их возникновения?
Психосоматические заболевания — это группа болезней, которые проявляются телесными страданиями (то есть симптомами заболеваний внутренних органов), но их основная причина всё же кроется в неполадках со стороны нервной системы. К ним относят целый спектр желудочно-кишечных расстройств (функциональная желудочная диспепсия и синдром раздражённого кишечника), фибромиалгию (специфический болевой синдром в проекции суставов), гипервентиляционный синдром (ощущение нехватки кислорода и потребность в частом дыхании) и много чего ещё.
То, как связаны между собой психические страдания и соматические симптомы, поясню на примере самой распространённой жалобы, с которой пациенты приходят к кардиологу — ощущения учащённого сердцебиения. Тахикардия (частый пульс) в норме возникает, когда надо отреагировать на внешний раздражитель, например убежать от опасности. В этой ситуации мышцам нужно больше крови, следовательно, сердце должно увеличить частоту сокращений. Но когда опасность проходит, пульс нормализуется. Пациент с невротическим расстройством внешне спокоен, за ним никто не гонится, ему никого не нужно догонять, но головной мозг даёт сигнал: «Ты в опасности, убегай!» В результате активируется симпатическая нервная система, повышается давление и учащается пульс. Пациент чувствует себя плохо… В этом случае лечить тахикардию как отдельный симптом по меньшей мере нелепо — надо лечить само невротическое заболевание, причём лечить таких пациентов должен не кардиолог, а психиатр или психотерапевт.
Что касается детской психосоматики, расскажу ещё одну историю. Недавно на приём пришла молодая женщина. Она выглядела очень встревоженной и всё время пыталась меня расспросить о здоровье своего мужа, хотя, по моим представлениям, её муж вполне мог сам прийти на приём. В разговоре выяснилось, что муж (много работающий и хорошо зарабатывающий человек) дома постоянно кричит на жену и ребёнка, при этом ещё успешно манипулирует своим повышенным давлением, но лечиться не хочет. В конце нашей встречи женщина спросила, нет ли у меня на примете хорошего невролога, специалиста по детским тикам… Стоит продолжать рассказ? По-моему, не надо быть доктором Хаусом, чтобы понять простую вещь: большинство преходящих неврологических и невротических симптомов у детей — это проблема с родителями.
Что такое «чикагская семёрка» и насколько актуальна такая классификация в наши дни?
Классификации психосоматических расстройств мне не очень нужны в повседневной работе, да и про «чикагскую семёрку» я впервые узнал благодаря этому вопросу. Прочитал и ужаснулся. Неужели в XXI веке кто-то всерьёз может рассматривать их как «болезни неотреагированных эмоций»! Перечислю эти семь заболеваний с указанием их истинных причин:
Болезнь Паркинсона возникает из-за стремления к контролю? Аденоиды у детей появляются, когда они чувствуют, что родители их не любят?
Приведённые примеры — плод неуёмного воображения диванных психологов. У обеих болезней есть гораздо более понятные причинные факторы, хотя и не до конца изученные. А вот психосоматические заболевания желудочно-кишечного тракта (функциональная диспепсия, синдром раздражённого кишечника) действительно характерны для людей мнительных, тревожных и неуверенных в себе. В древности даже существовала поговорка: любой невропат — колопат (colon — лат. «толстая кишка»).
Ипохондрия — это тоже психосоматика?
Строго говоря, «ипохондрическое расстройство» — это не психосоматика, это чистая «психика», то есть настоящее тревожное невротическое расстройство, в рамках которого пациент бесконечно ищет у себя соматические заболевания и цепляется к самым безобидным симптомам. Моя почта переполнена письмами от ипохондриков, которые, обнаружив у себя несколько десятков экстрасистол (внеочередных сокращений сердца), тут же интересуются, какова теперь у них вероятность внезапной смерти.
Как происходит диагностика психосоматических расстройств?
Пациенты с психосоматическими расстройствами могут посещать врачей любой специальности. У кого-то болезни проявляются немотивированной одышкой и сердцебиением, у кого-то тошнотой, рвотой и поносом, а у некоторых — болевыми синдромами.
— Главный диагностический критерий — обследование, зачастую неоднократное — не позволяет обнаружить никаких признаков органического заболевания. Именно этот факт должен навести на мысль о необходимости консультации с психиатром или психотерапевтом.
Основа диагностики — беседа с пациентом. Уже только на основании того, как пациент излагает жалобы, можно задуматься о наличии психосоматических расстройств. Если врач располагает достаточным временем для выяснения обстоятельств, связанных с началом или обострением заболевания, если найдёт аккуратные слова для выяснения психотравмирующих ситуаций, то картина болезни начнёт вырисовываться. Как я уже сказал, диссоциация между жалобами и отсутствием органической патологии — важный аргумент в пользу «психосоматики». Конечно, разумный объём дообследования всегда необходим, но он не должен быть избыточным.
Приведу в пример одно из классических психосоматических заболеваний — синдром раздражённого кишечника (СРК). В России считают, что для установки диагноза нужно обязательно сделать колоноскопию — непростое и недешёвое эндоскопическое обследование толстого кишечника. Во всём мире считают иначе. Если длительные симптомы кишечного дискомфорта (поносы или запоры, вздутие живота и так далее) не сопровождаются наличием так называемых «красных флагов» (снижение веса, кровь в кале, воспалительные изменения в анализах крови, поздний возраст начала болезни и наличие онкологических заболеваний у близких родственников), то мучить пациента такой непростой процедурой, как колоноскопия, смысла нет — диагноз СРК весьма вероятен.
Сколько лет проходит от обращения пациента с психосоматическим расстройством до постановки ему корректного диагноза? Бывает по-разному. Мне кажется, что если правильно построить общение с пациентом, то это совсем не сложно. Но мы этому хорошо обучены. Дело в том, что наш ныне покойный учитель, бывший директор клиники факультетской терапии Первого меда (ныне Сеченовский университет) профессор В. И. Маколкин большое внимание уделял изучению психосоматической патологии, в результате чего на базе клиники был фактически создан небольшой психосоматический центр. Сотрудники клиники довольно хорошо ориентируются в патологии такого рода, кроме того, нас поддерживает команда из нескольких психиатров.
Иногда случается, что от начала заболевания до получения профессиональной помощи проходят годы. Сложно сказать, с чем это связано. Скорее всего, с тем, что коллеги «не видят» психосоматику или же стесняются отправить пациентов к психиатру, опасаясь, что пациенты их неправильно поймут.
Как лечить психосоматику?
Всё зависит от ситуации; понятие «психосоматические расстройства» слишком широкое. В лёгких случаях специфическое лечение вообще не требуется, достаточно детальной беседы врача с пациентом и разъяснения сути происходящего. Дело в том, что порой пациента тревожат не столько сами симптомы, сколько неизвестность и подозрение на серьёзные органические заболевания. Если объяснить, что за «ощущением неполного вдоха» или «покалываниями в сердце» не стоят органические болезни сердца и лёгких, многих пациентов это вполне удовлетворит.
В отдельных случаях врач-интернист (терапевт, кардиолог, гастроэнтеролог и другие) самостоятельно может назначить психотропную терапию, если он умеет, конечно, это делать. Скажем, квалифицированный гастроэнтеролог вполне может и должен сам назначать антидепрессанты пациентам с функциональными заболеваниями желудочно-кишечного тракта, не прибегая к помощи психиатров. Зачем антидепрессанты гастроэнтерологическим пациентам? Они нужны для того, чтобы разорвать патологическую связь между сигналами в головном мозге и симптомами со стороны желудочно-кишечного тракта. Кстати, антидепрессанты давно уже перестали быть специфическими препаратами для лечения депрессии. Их с успехом применяют и в терапии некоторых болевых синдромов.
Если интернист чувствует, что пациенту нужна серьёзная комбинированная терапия, то лучше подключить к лечению психиатра, так как психофармакология довольно сложна и арсенал препаратов многообразен. Желательно консультироваться не просто с психиатром из районного диспансера, а со специалистом, который имеет опыт работы именно с психосоматическими пациентами.
Психотерапия (то есть лечение в разговорном жанре) может быть весьма полезна многим пациентам с психосоматическими расстройствами. Есть только два минуса: это дорого и долго. Противопоказание к психотерапии — симптомы «большого» психического заболевания (бредовые расстройства, галлюцинации), впрочем, это уже выходит за рамки темы «психосоматика».
А вот что пациенту точно не нужно — это видимость лечения с использованием пустышек: витаминов, «общеукрепляющих», «метаболических», «сосудистых» препаратов и так далее.
Могут ли психосоматические заболевания со временем трансформироваться в соматические патологии?
Маловероятно. Вернёмся в начало. Факторами риска они могут быть, причиной — нет. То есть гипервентиляционный синдром не превратится в астму, СРК не станет язвенным колитом, фибромиалгия не трансформируется в ревматоидный артрит. Важно только понимать, что с возрастом увеличивается риск настоящих соматических заболеваний. Нужно только не пропустить их начало.
Что такое психогигиена и чем она может помочь?
И последнее. Если чувствуете, что что-то в жизни идёт совсем не так и самостоятельно выкарабкаться не получается, не стесняйтесь обращаться к специалистам в области психиатрии и психотерапии. Современная психиатрия ушла далеко вперёд по сравнению с классическим представлением о ней в фильме «Полёт над гнездом кукушки».
Если вы хотите грамотно использовать все возможности современной медицины, а также не стать жертвой сомнительного лечения и избыточной диагностики, книги из курса «Академии доктора Родионова» — вам в помощь. Все авторы серии не только практикующие врачи и специалисты, но и наши постоянные эксперты (за что им огромное спасибо).
Как спасти Тринадцатую? (Перспективы лечения болезни Хантингтона)
Как спасти Тринадцатую? (Перспективы лечения болезни Хантингтона)
Тринадцатая — героиня сериала «Доктор Хаус» — знала, что может быть больна болезнью Хантингтона, поскольку от этой болезни умерла ее мать. Она долгое время не хотела делать анализы, потому что это заболевание все еще не излечимо, и знание диагноза не сделает жизнь лучше. Но новые исследования в этой области дают надежду, что в скором времени развитие болезни Хантингтона можно буде остановить на ранней стадии.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Сейчас сложно найти человека, который никогда не слышал про болезни Альцгеймера, Паркинсона или Хантингтона. Эти недуги относятся к группе нейродегенеративных заболеваний, вызывающих гибель нейронов и постепенное разрушение головного мозга. К сожалению, все они являются неизлечимыми. Поэтому ученые активно работают над тем, чтобы раскрыть механизмы развития этих болезней и найти терапию, которая поможет спасти пациентов. В своем исследовании мы обратились к пока еще малоизученному вопросу — что происходит с синаптической связью нейронов при нейродегенеративном процессе? Результаты этой работы открывают новое направление для разработки лекарства от болезни Хантингтона и других нейродегенеративных заболеваний.
Конкурс «био/мол/текст»-2013

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
С увеличением средней продолжительности жизни все больше людей страдают от болезни Альцгеймера и болезни Паркинсона. К сожалению, годы исследований пока не привели ученых к открытию причин развития этих заболеваний и возможной терапии. Это связано, главным образом, с тем, что почти ничего не известно о факторах, вызывающих болезнь, а также с тем, что очень мало пациентов имеют генетическую предрасположенность. Чаще всего эти заболевания являются спорадическими, т.е. причины их возникновения не установлены. Это приводит к бесконечным спорам — никто не знает, как искусственно вызвать это заболевание у модельных животных для экспериментов и поиска лекарств. Поэтому все больше ученых обращают свое внимание на генетические заболевания нервной системы, такие как болезнь Хантингтона (БХ). Это заболевание также, как болезнь Альцгеймера и болезнь Паркинсона, относится к группе нейродегенеративных заболеваний, с которыми его объединяет ряд схожих черт: гибель нейронов центральной нервной системы, накопление амилоидоподобных агрегатов белков, когнитивные и двигательные нарушения у больных. При этом БХ имеет важное преимущество с точки зрения исследователей, т.к. известно, какая мутация вызывает это заболевание. Это дает возможность создавать точные генетические модели и исследовать их на животных. Это важно, потому что если мы поймем патогенез болезни Хантингтона, то нам легче будет разобраться и со спорадическими нейродегенеративными заболеваниями. Это мы и попытались сделать в своем исследовании.
Болезнь Хантингтона
Болезнь Хантингтона (БХ, в русскоязычной литературе также «болезнь Гентингтона») — наследственное заболевание нервной системы, которое поражает примерно 1 из 10 тыс. людей. Болезнь была впервые описана Джорджем Хантингтоном (George Huntington) в 1872, и с тех пор носит его имя, однако клинические симптомы этого заболевания были известны еще в XVI веке под названием «хорея» (от лат. choreus — танец). К признакам хореи относили непроизвольные, нескоординированные быстрые движения, похожие на судороги; именно так описывают и современные медики моторные нарушения, характерные для БХ. Болезнь может порой длиться до двадцати лет, но исход неизменно один и тот же: больной теряет способность самостоятельно передвигаться, говорить, а затем и мыслить. Как правило, симптомы болезни Хантингтона проявляются в возрасте от 30 до 50 лет, хотя у 5–10% пациентов отмечается появление симптомов в возрасте до 20 лет — так называемая ювенильная форма заболевания [1].
Первый симптом болезни Хантингтона — непроизвольные подёргивания конечностей, торса и лицевых мышц. Довольно часто они сопровождаются резкими сменами настроения, депрессией, раздражительностью, неразборчивостью речи и неуклюжестью движений. По мере прогрессирования болезни, к этим симптомам добавляются затруднения или боль при глотании, неустойчивость походки, потеря равновесия, нарушение мыслительных функций и ухудшение памяти. В конце концов, больной теряет способность передвигаться без помощи посторонних и умирает обычно от пневмонии, остановки сердца или других осложнений.
Важной для врачей и исследователей особенностью БХ является то, что это заболевание является наследственным и вызывается мутацией в одном-единственном гене. Оказалось, что к развитию БХ приводит увеличение количества повторов триплета CAG, кодирующего глутамин, в первом экзоне гена белка хантингтина. При этом, чем больше количество повторов этого триплета, тем раньше начинается развитие заболевания. В норме в человеческой популяции встречается от 10 до 35 повторов. У пациентов с БХ количество повторов может быть от 36 до 121, при ювенильной форме — от 50 и выше [2]. Благодаря выявлению генетической основы заболевания, диагностика БХ в настоящее время не представляет проблемы; кроме того, возможной стала пренатальная диагностика заболевания и проверка эмбрионов перед имплантацией при ЭКО, которая позволяет иметь здоровых детей даже носителям мутантного гена.
К сожалению, выявление точной мутации все еще не позволяет ученым определить причину развития болезни Хантингтона и найти соответствующее лечение. Появление в клетке мутантного гена и, соответственно, измененного (мутантного) белка может привести к развитию патологии двумя путями: потеря функции (loss-of-function) или приобретение функции (gain-of-functin). В первом случае мутантный белок не может выполнять ту же функцию, что белок нормальный, и это приводит к нарушению клеточных процессов. Во втором случае, мутантный белок мешает нормальной жизнедеятельности клетки, начиная выполнять какую-то «лишнюю функцию». Чтобы разобраться, что происходит при БХ, ученые интенсивно изучают как функцию нормального белка хантингтина, так и поведение его мутантной формы [3].
К сожалению, попытки определить точную клеточную функцию хантингтина пока не увенчались успехом. Различные исследования указывают на участие этого белка в широком спектре биологических процессов, включая транспорт белков и везикул (мембранных пузырьков-транспортеров), организацию цитоскелета, клатрин-опосредованный эндоцитоз, постсинаптический сигналинг, регуляцию транскрипции и анти-апоптотические процессы [4]. Если удастся доказать, что нарушение какой-либо из этих функций является ключевым для развития заболевания, то лекарственные препараты для поддержания этой функции могут спасти пациентов с болезнью Хантингтона.
Если верна гипотеза о приобретении функции, особое внимание стоит обратить на поведение мутантной формы хантингтина. Оказалось, что мутантный белок формирует агрегаты, которые являются одной из характерных черт развития БХ как у людей,так и у модельных животных (см.врезку). Сначала агрегаты были описаны только в ядре, однако последующие работы выявили их также в цитоплазме и отростках нейронов [5]. В последние годы многие авторы склоняются к тому, что образование агрегатов несет скорее протективную функцию, а основной патогенной формой мутантного хантингтина является мономерный растворимый белок [6].
Модели для изучения болезни Хантингтона
Модели БХ на животных появились более 30 лет назад. Первыми были модели, основанные на введении в стриатум нейротоксических веществ (например, хинолиновой кислоты — агониста NMDA-рецепторов), которые вызывали гибель нейронов. В настоящее время большинство исследователей работает на моделях трансгенных животных, среди которых есть не только мыши и крысы, но и беспозвоночные животные — мушка Drosophila melanogaster и червь Caenorhabditis elegans.
Мышиные модели болезни Хантингтона отличаются друг от друга количеством CAG-повторов и уровнем экспрессии трансгена — искусственно внесенного гена хантингтина. Т.к. именно от этих факторов зависит развитие БХ, разные линии мышей отличаются друг от друга скоростью развития патологий. К наиболее широко используемым моделям относят линии мышей R6/2, R6/1 и YAC128, которые были использованы и в нашей работе. У мышей этих линий симптомы заболевания наиболее выражены и проявляются достаточно быстро. Кроме того, у этих животных с возрастом прогрессируют когнитивные и моторные нарушения, развивается частичная потеря нейронов в стриатуме и коре.
Еще одним из способов моделирования БХ является использование клеточной культуры. В самом простом случае используются культуры клеток со стабильной трансфекцией гена хантингтина. Например, это клетки линии PC12, содержащие индуцибельный трансген первого экзона хантингтина или нейроны стриатума с экспрессией фрагментов хантингтина разной длины. Кроме того, можно использовать первичные культуры из нейронов трансгенных мышей или иммортализованные нейроны.
Почему мы решили исследовать параметры синаптической передачи при болезни Хантингтона
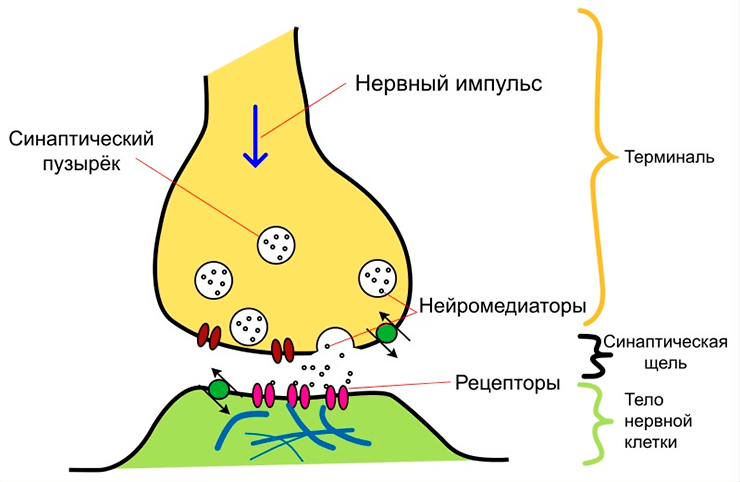
Синаптическая передача — это передача сигналов между нейронами с помощью синаптического контакта. При возбуждении одного нейрона его синаптическое окончание выделяет в синаптическую щель медиатор — химическое вещество, которое оказывает свое возбуждающее или тормозящее воздействие на синаптическое окончание второго нейрона (рис. 1). Таким образом, синапсы связывают нейроны между собой, обеспечивая нормальное функционирование нейронных сетей и всей нервной системы. Если какая-то из систем головного мозга перестает функционировать, причина может крыться либо в нарушении работы отдельных нейронов, либо в нарушении связи между ними, т.е. нарушении синаптической передачи.
Рисунок 1. Схематическое изображение устройства синапса.
При болезни Хантингона поражается специфическая область головного мозга, называемая стриатумом. Стриатум является частью важного нейронного пути — экстрапирамидной системы, которая участвует в управлении движением и поддержании мышечного тонуса. Гибель нейронов стриатума при болезни Хантингтона приводит к разрушению экстрапирамидной системы, что связано с потерей контроля над движениями у больного человека. Но когда возникают первые патологические симптомы (тремор, нарушение координации), головной мозг человека еще не поврежден: нейроны начинают погибать только через несколько лет после начала развития заболевания. Т.е. болезнь начинается, когда что-то меняется в работе самих нейронов или в синаптической передаче, и эти нарушения впоследствии ведут к гибели нейронов и необратимым последствиям.
В 2013 году Нобелевской премии по физиологии и медицине удостоены работы, благодаря которым стали ясны детали везикулярного транспорта — процесса образования и транспортировки мембранных пузырьков (везикул) между клетками: «Нобелевская премия по физиологии и медицине (2013): везикулярный транспорт» [8]. — Ред.
Изучение нарушенной синаптической передачи при БХ было темой нашего исследования. Может ли быть, что неправильная работа нейронов стриатума на ранней стадии БХ вызвана тем, что они «не слышат» команды нейронов коры? Может ли ослабление синаптической связи приводить к необратимым изменениям в нейронах стриатума и вести к их гибели? О чем мы узнали во время поиска ответов на эти вопросы, рассказано ниже.
Результаты исследований: изменения в синаптической передаче при болезни Хантингтона
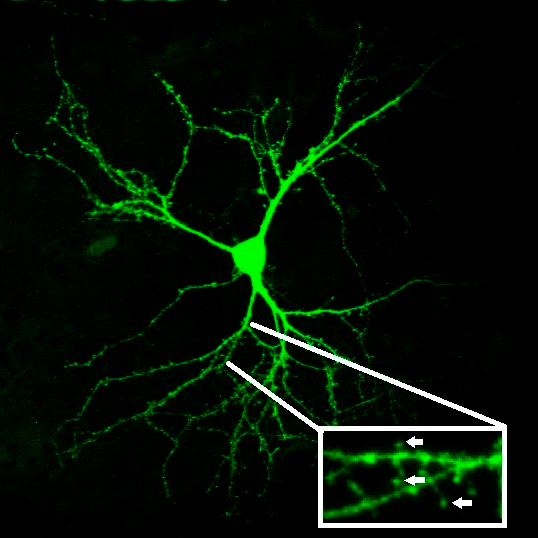
Изучать синаптическую передачу можно различными способами. Например, это можно делать, проникнув в нейронную цепочку с помощью методов электрофизиологии. Нейрон проявляет свою активность с помощью электрического тока, который можно измерить. Если экспериментатор возьмет цепочку из двух нейронов и, активировав один нейрон, зарегистрирует электрическую активность второго, он сможет выяснить, насколько хорошо проходит сигнал. Другой способ изучать функционирование синаптической передачи — исследовать морфологию нейрона. Дело в том, что многие нейроны (в том числе, нейроны коры и стриатума) имеют особые выросты мембраны — шипики, которые нужны им именно для образования синапсов (рис. 2). Чем более активно нейрон «общается» со своими соседями, тем больше на его поверхности шипиков. Взяв на вооружение эти два подхода, мы решили исследовать, как работает синаптическая передача при БХ.
Рисунок 2. Дендритные шипики на поверхности стриатного нейрона. Шипики — небольшие выросты на поверхности нейрональных отростков; на увеличенном изображении они отмечены стрелками.
фото автора статьи
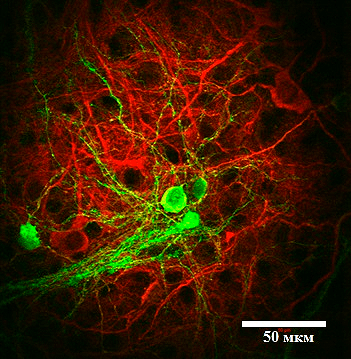
Рисунок 3. Нейрональная культура из нейронов коры и стриатума. С помощью специфических антител нейроны коры окрашены в красный цвет, а нейроны стриатума — в желто-зеленый.
фото автора статьи
В качестве модели для изучения болезни Хантингтона была использована клеточная культура из нейронов коры и стриатума. Для приготовления культуры незрелые нейроны из изучаемых зон мозга мышей высаживаются в чашки Петри, где они формируют полноценные нейрональные отростки и нейронные цепочки (рис. 3). Использовались мыши дикого типа (без мутаций) и мыши линии YAC128, которые несут мутацию в гене белка хантингтина и являются признанной моделью БХ. На 14–15 день после высаживания нейронов в чашку Петри они достигают зрелого состояния, соответствующего состоянию нейронов в мозге взрослого человека, а на 19–20 день нейроны считаются «старыми»: в них наблюдается ряд клеточных процессов, характерных для мозга пожилых людей. Кроме того, с возрастом в нейронах мышей YAC128 происходит накопление мутантного белка хантингтина и его агрегатов, поэтому изучение нейрональной культуры на этих двух этапах дает представление о том, что происходи в мозге пациента с БХ на ранней и на поздней стадиях заболевания.
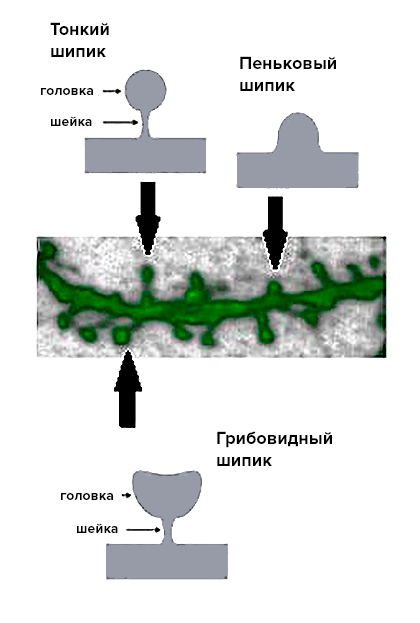
Рисунок 4. Шипики разных типов на поверхности дендрита — микрофотография и схематическое изображение.
Для начала мы исследовали морфологические отличия между двумя линиями, т.е. сравнили их внешний вид. Для нормальных нейронов стриатума характерно наличие большого количества шипиков, благодаря чему их называют средними шипиковыми нейронами (СШН). Именно шипики формируют большую часть синаптических контактов между нейронами стриатума и коры, и для осуществления нормальной синаптической передачи важно наличие определенного их количества. Так же важно и «качество» шипиков: в современной нейробиологии их разделяют на три группы согласно размеру и форме (рис. 4): грибовидные, тонкие и пеньковые. При этом шипики разных типов выполняют разные функции: считается, что только грибовидные шипики формируют активные синапсы, в то время как тонкие и пеньковые контактов с другими нейронами не образуют. Таким образом, для нормального функционирования нейронной цепочки и эффективной передачи информации по ней необходимо наличие определенного количества грибовидных шипиков.
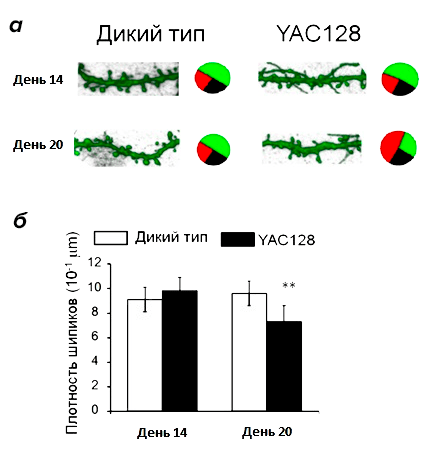
Для того, чтобы узнать, сколько грибовидных шипиков должно быть на СШН в норме, на всех этапах морфологического анализа как контроль использовалась культура нейронов из головного мозга мышей дикого типа. Оказалось, что количество шипиков на СШН стриатума на 14 день культивирования (молодые нейроны) одинаково в культурах YAC128 и дикого типа, но на 20 день (у «старых» нейронов) наблюдаются значительные изменения (рис. 5). В «постаревшей» культуре YAC128 снижается общее количество шипиков, причем относительное количество грибовидных шипиков, которые образуют активные синапсы, уменьшается в два раза [10]. Получается, что морфологические изменения нейронов, свидетельствующие о нарушении синаптической передачи, развиваются только к «старости» (на поздней стадии заболевания). Значит, на ранних этапах корень проблемы должен лежать в другой области.
Рисунок 5. Морфологический анализ нейронов стриатума. а — шипики нейронов на 14 и 20 дни культивирования. На микрофотографиях показаны участки дендритов нейронов. Относительное количество шипиков разных типов отмечено на круговой диаграмме: зеленый — грибовидные шипики, красный — тонкие шпики, черный — тонкие шипики. На 20 день культивирования на поверхности нейронов YAC128 снижается доля грибовидых шипиков и возрастает доля пеньковых. б — Плотность дендритных шипиков (среднее количество шипиков на участке дендрита длиной 10 мкм) на нейронах дикого типа и YAC28.
Поэтому мы сравнили электрофизиологические характеристики двух линий. Это возможно благодаря электрической активности нейронов, которую можно зарегистрировать с помощью специального метода, называемого пэтч-кламп. Для этого к поверхности нейрона прикладывают тонкую стеклянную пипетку, внутри которой находится электрод. Когда нейрон активируется, на его клеточной мембране изменяется напряжение, и это изменение регистрируется электродом. Если взять два связанных синаптическим контактом нейрона и, возбуждая один, регистрировать ответную электрическую активацию на втором, можно измерить эффективность передачи сигнала через синапс (рис. 6). Если ответная активация возникает не всегда, то, вероятно, синаптическая передача ослаблена. Этот метод может выявить нарушения работы синапса до изменений морфологии нейрона.
Рисунок 6. Схема эксперимента при совместном применении оптогенетики и электрофизиологической регистрации. Нейрон коры активируется при освещении синим светом, а на контактирующем с ним нейроне стриатума производится регистрация ответной активности с помощью стеклянной пипетки с электродом.
Чтобы активировать нейрон, можно использовать несколько способов. Можно добавить в окружающую его жидкость химическое вещество, открывающее ионные каналы, что приводит к электрическому возбуждению нейрона. Можно стимулировать нейрон электрическим током. Но мы для своих экспериментов выбрали более тонкий инструмент воздействия на нейроны, а именно — оптогенетику. Этот подход основан на внесении в нейроны специальных светочувствительных белков — опсинов, в результате чего и сами нейроны становятся чувствительными к свету (рис. 7). В результате, освещая нейроны светом определенной длины волны, можно изменять их активность. Освещение синим светом возбуждает нейрон, а желтым — вызывает торможение (т.е. подавляет активность нейрона).
Оптогенетические технологии в наши дни обещают даже вернуть зрение людям с дегенеративными поражениями сетчатки, придав световую чувствительность не разрушенным фоторецепторам, а клеткам-ганглиям: «Оптогенетика + голография = прозрение?» [11]. — Ред.
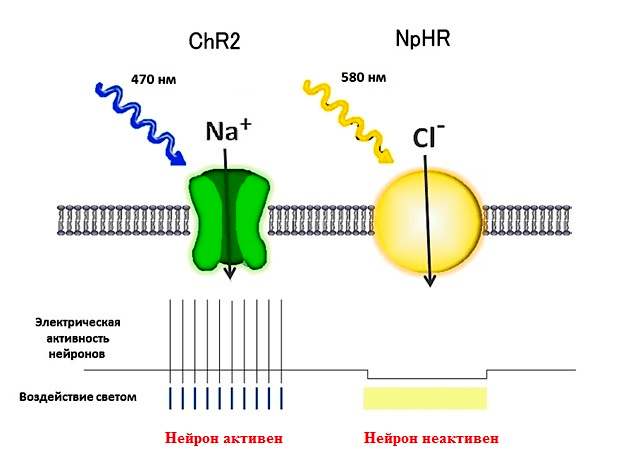
Рисунок 7. Опсины — светочувствительные белки, обеспечивающие движение ионов через клеточную мембрану и изменение активности нейронов. Каналородопсин (ChR2) вызывает деполяризацию мембраны и активацию нейрона, галородопсин (NpHR) вызывает гиперполяризацию мембраны и торможение нейрона.
Оптогенетика
Оптогенетика — метод, объединяющий подходы генетики и оптики для тонкого контроля электрической активности электровозбудимых клеток (нейронов и мышечных волокон) [9]. Для этого в изучаемые клетки вводят гены специальных светочувствительных белков — микробных опсинов, которые являются ионными каналами или насосами (рис. 7). Первая работа, показавшая возможность управлять электрической активностью нейронов при использовании опсина, была опубликована в 2005 году. За последующие несколько лет появился еще ряд экспериментальных работ, позволивших доработать эту методику и доказать ее применимость в различных экспериментальных условиях.
За последние годы было открыто множество различных опсинов, из которых наибольшее применение в оптогенетике нашли галородопсины и каналородопсины. При доставке гена опсина с помощью методов генной инженерии в нейрон, на плазматической мембране появляются светочувствительные каналы, а сама клетка становится светочувствительной. При действии синего света открывается пора каналородопсина (максимум поглощения — 470 нм), который вызывает движение положительно заряженных ионов внутрь клетки, обеспечивая деполяризацию мембраны нейрона и генерацию потенциалов действия. При действии желтого света активируется галородопсин (максимум поглощения — 580 нм), мембрана нейрона гиперполяризуется, вызывая торможение нейрона. Высокое временное разрешение метода оптогенетики позволяет обеспечить очень тонкую регуляцию синаптических событий и является, таким образом, важным инструментом для изучения межнейронных связей.
Совместное применение оптогенетики и классических методов электрофизиологии позволяет извлечь выгоду из положительных качеств каждого из этих подходов. Точность электрофизиологической регистрации объединяется с возможностью использовать световые стимулы разной длительности и интенсивности, что помогает ученым подробно изучать работу нейронных связей.
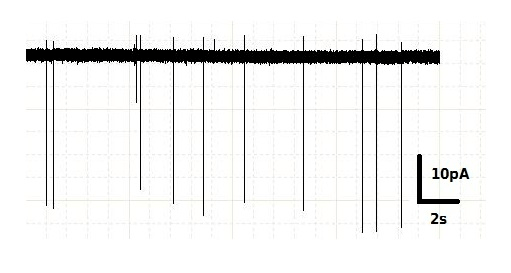
Электрическая активность нейронов выражается в резких скачках напряжения на клеточной мембране и появлении вследствие этого электрического тока. Эти резкие скачки называются спайками или потенциалами действия и длятся несколько миллисекунд (рис. 8). Мы выяснили, что чем дольше нейрон освещается синим светом, тем больше спайков он за это время создает. Если освещаемый нейрон связан синаптическим контактом с другим нейроном, то на втором нейроне можно зарегистрировать ответную активность — тоже в виде отдельных спайков.
Рисунок 8. Пример записи, получаемой при электрофизологической регистрации активности нейрона. Спайки (потенциалы действия) отражаются на записи в виде вертикальных линий, показывающих резкие скачки мембранного тока.
В наших экспериментах мы использовали пару молодых (14 дней) нейронов коры и стриатума, связанных синаптическим контактом. Нейрон коры активировали синим светом, а на нейроне стриатума производили регистрацию ответной активности. Оказалось, что для возникновения ответа на нейроне стриатума нужна определенная длительность освещения (порог активации). Если длительность освещения была ниже порогового значения, то спайк на нейроне стриатума возникал в ответ не на каждую вспышку света. И что самое важное: порог активации для нейронов из мозга здоровых мышей отличался от мышей YAC128 (с мутацией в гене хантингтина). Наиболее ярко эта разница была видна при 50%-активации нейрона стриатума, т.е. длительности освещения, при которой спайк возникает в ответ на каждую вторую вспышку света. Порог 50%-активации нейрона стриатума в ответ на облучение кортикального нейрона для культуры клеток YAC 128 был примерно в два раза (точнее в 2,3±0,8) выше по сравнению с положительным контролем [10].
Получается, что мутация в белке хантингтине приводит к тому, что синаптическая передача ухудшается уже в молодых нейронах, и при этом нарушения происходят на функциональном уровне (без морфологических изменений). Может ли быть так, что именно эти функциональные нарушения в дальнейшем приводят к появлению морфологических изменений, таких как исчезновение шипиков у старых нейронов стриатума?
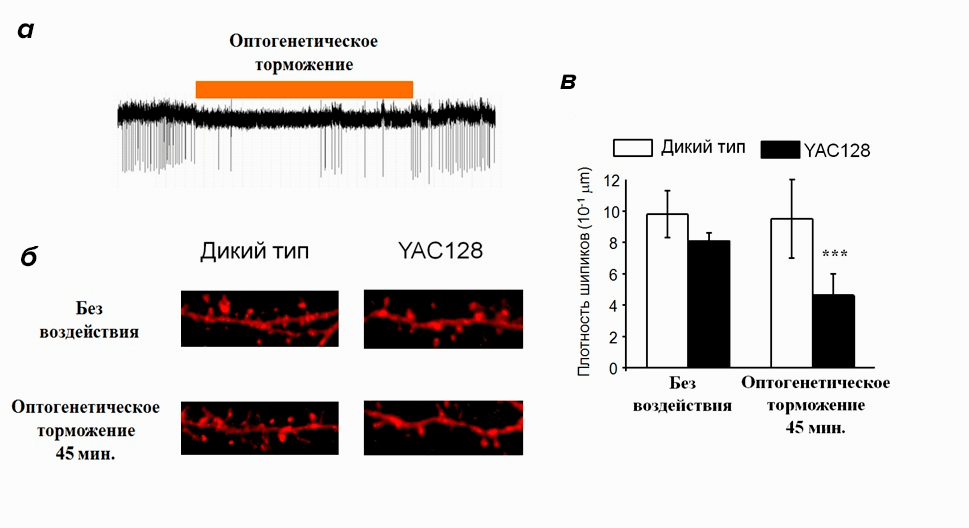
Чтобы ответить на этот вопрос, мы снова обратились за помощью к оптогенетике, но теперь с ее помощью мы подавляли светом активность нейронов (рис. 9а). Если наше предположение верно, то временное отсутствие активирующего воздействия коры должно привести к исчезновению шипиков на нейронах стриатума в культуре YAC128. Действительно, после эксперимента количество шипиков в положительном контроле осталось неизменным, но в культуре YAC128 значительно снизилось (рис. 9б, в). Получается, что моделирующие БХ нейроны особенно чувствительны к ослаблению активирующего воздействия нейронов коры, поэтому длительное ослабление синаптической связи между этими нейронами приводит к уменьшению количества шипиков на 20 день культивирования [10].
Рисунок 9. Влияние на нейроны с помощью оптогенетики. а — подавление активности нейрона коры с помощью оптогенетики. При освещении нейрона желтым светом (оранжевая полоса) он становится неактивен — на электрофизиологической записи в этот промежуток времени почти нет спайков. б — влияние длительного оптогенетического торможения на морфологию нейронов. На микрофотографиях видно уменьшение количества шипиков на дендрите нейрона YAC128. в — изменение плотности дендритных шипиков после оптогенетического торможения. В культуре дикого типа количество шипиков не изменяется, а в культуре YAC128 плотность шипиков значительно снижается.
Таким образом, мы обнаружили, что в нашей модели БХ наблюдается нарушение синаптической передачи, которое развивается в два этапа. На ранней стадии (молодые нейроны, на 14 день культивирования нейронов) происходит функциональное ослабление сипаптической связи, которое на более поздней стадии (старые нейроны, на 20 день культивирования) приводит к морфологическим нарушениям синаптических контактов.
Вывод: нарушение синаптической передачи и нейродегенеративные заболевания
Исследование подтвердило нашу первоначальную догадку: нарушение работы стриатума при БХ связано, прежде всего, с нарушением синаптической передачи. Нейроны стриатума перестают «слышать» команды нейронов коры, и, в результате, человек начинает терять контроль над своими движениями. Но на ранней стадии заболевания эти нарушения носят функциональный характер и, вероятно, обратимы. Если выяснить причины, ведущие к нарушению работы синапсов, то возможно разработать лекарственное средство, которое поможет остановить патологические изменения, обеспечит нейронам стриатума необходимый уровень активации и, таким образом, предотвратит развитие необратимых морфологических нарушений.
Результаты этой работы подталкивают и к другому важному заключению: при изучении нейродегенеративных заболеваний ученым следует обратить больше внимания на синаптическую передачу и взаимодействие нейронов. Мы знаем достаточно много о том, как влияет накопление амилоидных агрегатов при болезни Альцгеймера на жизнедеятельность клетки, и какие нейроны погибают при развитии болезни Паркинсона, но это все еще не привело к появлению эффективной терапии. Возможная причина этих неудач — мы не учитываем последствия нарушения синаптических связей — те, которые мы открыли при исследовании болезни Хантингтона. Хочется надеяться, что наши находки подскажут исследователям направление для разработки эффективных способов лечения болезни Хантингтона, и Тринадцатая наконец-то будет здоровой!
Исследование было проведено в лаборатории молекулярной нейродегенерации СПбГПУ (зав. лаб. — проф. Техасского университета Илья Борисович Безпрозванный) под руководством к.б.н. Дмитрия Николаевича Артамонова.