синдром шарко что это такое
Синдром шарко что это такое
Синонимы синдрома Шарко I. S. Erb—Charcot. S. Souques—Charcot. Перемежающаяся хромота (claudicatio intermittens). Перемежающаяся дисбазия (Erb). Перемежающийся мышечный паралич (Grassmann). Эндартериит нижней конечности. Хирургическая спонтанная гангрена. Ангиосклеротическая пароксизмальная миастения (Highier). Angina cruris.
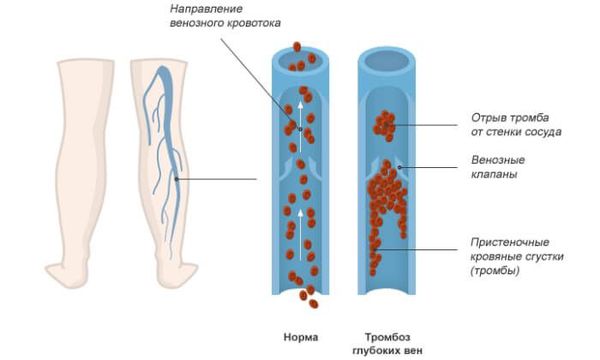
Определение синдрома Шарко I. Перемежающееся расстройство походки в результате функционального или органического сужения сосудов и недостаточности кровоснабжения мускулатуры нижней конечности.
Автор. Charcot Jean Martin — французский невропатолог, Париж, 1825—1893. Синдром был им впервые описан в 1858 г. До этого аналогичные случаи заболевания были известны лишь у лошадей.
Симптоматология синдрома Шарко I:
1. Парестезии и судорожные болевые приступы в нижней конечности, вынуждающие больного внезапно остановиться (перемежающаяся хромота).
2. Цианотический белый или мраморный оттенок пальцев ноги. Ослабление или отсутствие пульса на ступне.
3. Развитие гангрены в области пальцев ноги.
4. Заболевают преимущественно мужчины.
5. При наличии перемежающейся «хромоты» рук или языка правильнее говорить о S. Determann.
Этиология и патогенез синдрома Шарко I. Гипоксемическое нарушение мышечного обмена вследствие недостаточности кровообращения (спазм сосудов, склероз артерий и вен с закрытием сосудистого просвета). Предрасполагающими факторами являются диабет, интоксикация никотином, врожденное сужение сосудов.
Дифференциальный диагноз. S. (Weir) Mitchell (см.). S. Martorell (см.). Синдром Рота-Bernhardt (см.). Неврит. Старческая гангрена. Псевдопаралитическая злокачественная миастения (S. Erb — Goldflam — см.). S. Laverie (см.). Варикозно-статические расстройства. «Ишиальгия». Эмболия. Артерио-венозная фистула. S. Leriche (см.). S. v. Winiwarter—Buerger (см.). S. Nygaard— Brown (см.).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое боковой амиотрофический склероз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Калинкина М. Э., невролога со стажем в 8 лет.
Определение болезни. Причины заболевания
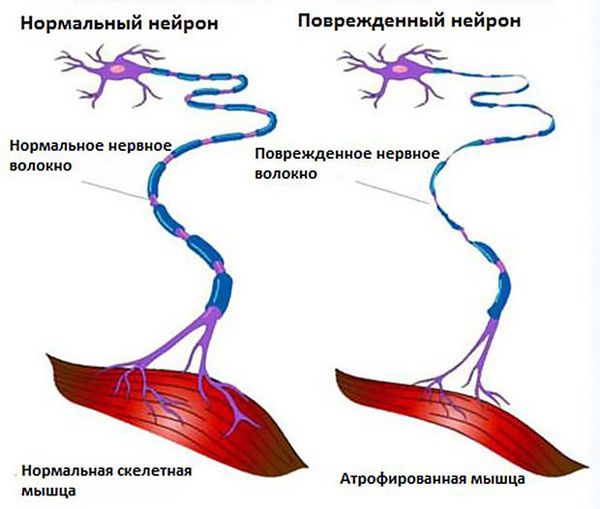
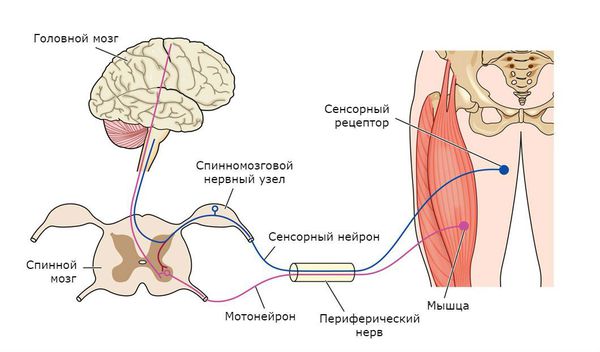
Чтобы понять суть заболевания, необходимо коснуться строения и функций головного и спинного мозга. В структуре спинного мозга на всём его протяжении и частично в стволе головного мозга существуют клетки, посылающие нервный импульс прямо к мышечным волокнам. Они называются нижние мотонейроны, так как своими импульсами приводят мышцы в движение. Группируясь в передней части поперечного среза спинного мозга, нижние мотонейроны образуют так называемый «передний рог».
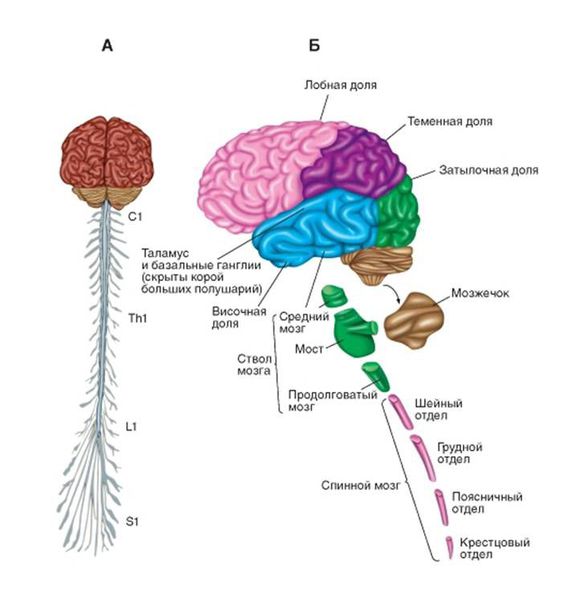
Также спинной мозг выполняет функцию соединяющего нервного «кабеля» между головным мозгом и частями тела. В норме спинной мозг подчиняется головному мозгу. Это означает, что, если импульс от головного мозга укажет мышце поднять руку, а импульс спинного мозга укажет опустить, то рука поднимется.
Головой мозг имеет сложное строение, но в данной статье нужно уделить внимание верхним мотонейронам. Они группируются в области, которая отвечает на исходную генерацию двигательных импульсов в организме — коре больших полушарий и стволе мозга. Импульсы, в свою очередь, идут по спинному мозгу вниз к вышеупомянутым нижним мотонейронам, а оттуда к мышцам, приводя их в движение. Именно этот путь поражается при боковом амиотрофическом склерозе.
Боковой амиотрифический склероз — представитель группы болезней двигательного нейрона, т. е. болезней мотонейронов. Кроме БАС, в эту группу включены: первичный латеральный склероз, прогрессирующая мышечная атрофия и прогрессирующий бульбарный паралич.
В ходе многолетних исследований были найдены негенетические модифицируемые факторы образа жизни, предрасполагающие к БАС:
Обобщая вышесказанное, можно сказать, что БАС развивается в результате комбинированного воздействия генов, факторов окружающей среды и образа жизни. Эта модель (ген-время-среда) предполагает, что развитие БАС является многоэтапным процессом, в котором генетические дефекты являются лишь одним из нескольких этапов, в конечном итоге приводящих к БАС.
Симптомы бокового амиотрофического склероза
Начальные симптомы БАС варьируют у пациентов в зависимости от степени поражения верхних и нижних двигательных нейронов и от того, какие участки тела вовлечены. Поэтому особенность бокового амиотрофического склероза заключается в том, что врачи часто вынуждены наблюдать за развитием жалоб в течение нескольких месяцев, прежде чем поставить верный диагноз (например, определить тип заболевания двигательного нейрона или тип БАС)
| Уровень поражения нижнего мотонейрона | Ствол головного мозга | Шейный отдел спинного мозга | Грудной отдел спинного мозга | Поясничный отдел спинного мозга |
|---|---|---|---|---|
| Группы мышц, которые поражаются | Мыщцы лица, мягкого нёба, язык, мышцы гортани и глотки | Мышцы шеи, рук | Мышцы спины, живота, диафрагмы | Мышцы спины, живота, ног |
По мере развития заболевания будут наблюдаться признаки поражения верхнего мотонейрона, а также постепенное присоединение соседних отделов спинного мозга.
Признаки поражения верхнего мотонейрона:
Патогенез бокового амиотрофического склероза
Патогенез заболевания чётко не определён. Примерная схема такова: ген в хромосоме (например ген супероксиддисмутазы-1, находящийся на 21-й хромосоме) «ломается» по неизвестным причинам. В результате синтезируются неправильные белки, которые мешают нормальной работе клеток нервной системы. Нервные клетки из-за этой поломки погибают, но процесс переработки мёртвых клеток (процесс аутофагии) также по какой-то причине не происходит. Из-за этого мёртвые клетки не распадутся на составляющие, а значит не создают «строительного материала» для новых клеток.
Все это соотносится с клиникой. Повышенная активность здоровых нейронов вызывает подёргивание мышц. Вскоре из-за скопления мёртвых клеток и отравления глутаматом нейроны погибают, происходит денервация мышц (разобщение связей мышц с нервной системой), в результате чего те слабеют и истончаются.
Классификация и стадии развития бокового амиотрофического склероза
Единой классификации БАС не существует, поскольку не существует единства представлений о его патогенезе. Рассмотрим Североамериканскую классификацию, которая близка к отечественной. Согласно этой классификация, БАС делится на две большие группы в зависимости от причин: семейный и спорадический (случайный).
Спорадический БАС делится на группы относительно уровня поражения моторных нейронов двигательного пути в дебюте заболевания. БАС может впервые проявиться на уровне ствола мозга, шейного, грудного (в том числе в виде слабости диафрагмальных мышц), поясничного отдела спинного мозга или на всем протяжении пути единовременно.
Семейная группа делится на виды в зависимости от типа мутации конкретного гена супероксиддисмутазы-1 (СОД-1) или мутаций в других хромосомах (около 10 других известных генов).
Североамериканская классификация БАС
Спорадический (случайный) БАС
В первую группу кроме классического БАС входят три патологии: первичный латеральный склероз; прогрессирующая мышечная атрофия; прогрессирующий бульбарный паралич. В нашей стране их считают отдельными заболеваниями и объединяют в группу болезней двигательного нейрона. В США данные патологии рассматривают как варианты проявления БАС. Несмотря на разницу классификаций, проявления этих заболеваний будут одинаковыми в любой стране.
Осложнения бокового амиотрофического склероза
Диагностика бокового амиотрофического склероза
При подозрении на болезнь двигательного нейрона пациент сначала отвечает на стандартные вопросы невролога о жалобах, развитии болезни, сопутствующих заболеваниях (стоит обратить внимание на онкологию и инфекции, так как они могут стать причиной ложноположительного БАС-симптома, а не самой болезни). Врач также спрашивает о болезнях родственников, стране рождения, о мочеиспускании и дефекации.
Невролог должен осмотреть мышцы тела, оценить их силу, тонус, проверить рефлексы с помощью молоточка, оценить чувствительность кожи при помощи иголки и камертона. При подозрении на БАС мышцы непроизвольно сокращаются и истончаются. В них теряется сила, даже если пациент занимается физическими упражнениями для их укрепления. Также врач может задать вопросы, похожие на определение IQ. При снижении интеллектуальных способностей можно заподозрить некий патологический процесс в коре головного мозга, где находится верхний мотонейрон.
Диагноз бокового амиотрофического склероза невозможно достоверно поставить с первого посещения невролога только после одного исследования ЭМГ. Иногда с целью уточнения заболевания или формы БАС врач дополнительно может назначить:
Функциональную способность пациентов оценивают в баллах по специальной шкале. В соответствии с этой шкалой максимальный балл 48 соответствует полной функциональной способности больного, а минимальный балл 0 соответствует максимально выраженной инвалидизации пациента.
Лечение бокового амиотрофического склероза
Препарат эдаравон является поглотителем свободных радикалов. Это внутривенное лекарственное средство для лечения БАС, которое было одобрено агентством Министерства здравоохранения США в мае 2017 года (примерно через 2 года после его одобрения для лечения БАС в Японии и Южной Корее). Использование этого препарата было оценено при разных неврологических расстройствах, включая БАС, в нескольких клинических испытаниях. Результаты были примечательными. Отмечалось замедление снижения показателей функциональной шкалы на 33 % за 6 месяцев и замедление ухудшения качества жизни людей с БАС в целом. Относительно расстройств дыхания не удалось достичь статистически значимых результатов.
Прогноз. Профилактика
Профилактика заключается в исключении или снижении влияния факторов риска: необходимо отказаться от курения; не контактировать с вредными веществами (пестицидами, гербицидами, свинцом и др.); исключить микротравмы головы.
Появляются и другие исследования, опровергающие пользу «витаминотерапии» для стран, не испытывающих проблем голода и нехватки пищи среди населения. В связи с этим более целесообразно рекомендовать пациентам покупать продукты «средиземноморской диеты», т. е. употреблять в пищу естественные витамины, антиоксиданты, жирные кислоты, не опасаясь передозировки этих веществ. Жителям отдалённых регионов с материальной точки зрения иногда выгоднее покупать пищевые добавки для непродолжительного курса приёма, чем продукты средиземноморской диеты.
Болезнь Шарко
Болезнь Шарко (в литературе еще встречается как «Болезнь Шарко-Мари», «Болезнь Шарко-Мари-Тута», код по МКБ- G60) –генетически обусловленное хроническое заболевание нервной системы, которое характеризуется развитием постоянно прогрессирующей периферической полинейропатией.
Частота диагностирования болезни Шарко-Мари-Тута согласно статистическим данным где-то один случай на две с половиною тысячи пациентов. Первые симптомы появляются в молодом возрасте. Выраженность симптомов и скорость прогрессирования болезни Шарко-Мари разная у каждого пациента. Процент инвалидизации при заболевании очень высок.
Причины заболевания болезнью Шарко:
Заболевание имеет много форм, вызванные разным видом мутаций. Качество жизни и возможности работоспособности при болезни Шарко-Мари-Тута значительно ухудшаются, но на продолжительности жизни обычно это не сказывается.
Симптомы болезни Шарко связанные с поражением моторных и сенсорных нервных волокон. Диагностика болезни Шарко-Мари заключается в исключении диагнозов, которые могут давать подобную клиническую картину, и в проведении ДНК-диагностики, но учитывая, что не все виды мутаций известны, она не всегда информативна.
Лечение болезни Шарко-Мари-Тута заключается в симптоматической терапии. Специфическое лечение на данный момент все еще находится в стадии разработки.
Юсуповская больница – одно из лучших медицинских учреждений, где лечатся пациенты с болезнью Шарко-Мари-Тута. Несмотря на то, что терапия направлена только на купирование симптомов, неврология стремительно развивается и питается найти способы лечения многих заболеваний, в том числе и болезни Шарко. Ведение пациентов изданной патологией достаточно сложное, ведь клиническая картина разнообразна, симптомы выражены в неодинаковой степени и п.т. Опыт работы специалистов Юсуповской больницы позволяет оказывать качественную и эффективную медицинскую помощь. Доктора следят за клиническими исследованиями, новыми разработками, препаратами, изучают их эффективность. В случае необходимости, диагностика проводится быстро и с использованием нового оборудования. Персонал работает на благо пациента.
Симптомы болезни Шарко
Симптомы болезни Шарка-Мари появляются в молодом возрасте, чаще всего до двадцати лет. Прогрессирует заболевание постепенно, пациенты долгое время сохраняют работоспособность и возможность самообслуживания. Причинами, которые ускоряют развитие заболевания, могут стать вирусные и бактериальные инфекции, воздействия неблагоприятных факторов среды, травматизм, недостаток витаминов и т.п.
По МКБ-10 болезнь Шарко-Мари-Тута кодируется как «G60 Наследственная моторная и сенсорная невропатия», что связано в какой-то мере с клинической картиной.
В начале заболевания беспокоит чрезмерная усталость, невозможность долго стоять на одном месте, чувство онемения, «беганье мурашек», а дальше присоединяется атрофическое поражение мышц стоп, которое чаще носит симметричный характер. При обследовании выявляют выпадение сухожильных рефлексов. Стопа деформируется на столько, что больные не могут ходить, опираясь на пятки. Прогрессируя, атрофический процесс поражает голени и бедра.
Все виды чувствительности нарушаются, но больше всего страдает поверхностная, особенно температурная.
Диагностика болезни Шарко
Полное обследование необходимо для исключения заболеваний, в которых клиническая картина сходна. К ним относят: боковой амиосклероз, миотония, метаболическая невропатия. Для исключения хронических полинейропатий проводят биопсию мышц.
Лечение болезни Шарко
Все способы лечения болезни Шарко-Мари-Тута не радикальны. Симптоматическое лечение включает медикаментозную терапию, физиотерапию, лечение у ортопеда и т.п.
Физиотерапевтическое лечение болезни Шарко-Мари-Тута включает ЛФК, массаж, электрофорез, диадинамотерапию, терапию лечебными грязями, разные виды ванн и др.
Медикаментозная терапия направлена на улучшение питания мышечных волокон. С этой целью назначают кокарбоксилазу, глюкозу, аденозинтрифосфат и др. Так же широко применяют антиоксидантные средства, препараты, улучшающие микроциркуляцию, и витамины. Хорошо зарекомендовали себя препараты, которые тормозят активность ацетилхолинэстеразы и повышают уровень ацетилхолина, например, прозерин, галантамин.
Дальнейшие разработки новых препаратов, направленные на радикальные меры – это мир без болезни Шарко-Мари-Тута. Прогрессирование болезни Шарко-Мари-Тута не отражается на том, сколько живут пациенты.
В Юсуповской больнице специалисты долгие годы помогают пациентам держать болезнь под контролем. Минимальная выраженность симптомов и медленное прогрессирование – результат работы врачей. В комфортных палатах, на новых тренажерах, в хорошо оснащенных кабинетах – вот где проходит лечение болезни Шарко-Мари-Тута. Не затягивайте с лечением, запишитесь на консультацию.
Невральная амиотрофия Шарко-Мари-Тута
Невральная амиотрофия Шарко-Мари-Тута — это прогрессирующее хроническое наследственное заболевание с поражением периферической нервной системы, приводящем к мышечным атрофиям дистальных отделов ног, а затем и рук. Наряду с атрофиями наблюдается гипестезия и угасание сухожильных рефлексов, фасцикулярные подергивания мышц. К диагностическим мероприятиям относятся электромиография, электронейрография, генетическое консультирование и ДНК-диагностика, биопсия нервов и мышц. Лечение симптоматическое — курсы витаминотерапии, антихолинэстеразной, метаболической, антиоксидантной и микроциркуляторной терапии, ЛФК, массажа, физиопроцедур и водолечение.
МКБ-10
Общие сведения
Невральная амиотрофия Шарко-Мари-Тута (ШМТ) относится к группе прогрессирующих хронических наследственных полиневропатий, в которую входят синдром Русси-Леви, гипертрофическая невропатия Дежерина-Сотта, болезнь Рефсума и другие более редкие заболевания.
По различным данным, невральная амиотрофия Шарко-Мари-Тута встречается с частотой от 2 до 36 случаев на 100 тыс. населения. Зачастую болезнь носит семейный характер, причем у членов одной семьи клинические проявления могут иметь различную выраженность. Наряду с этим наблюдаются и спорадические варианты ШМТ. Лица мужского пола болеют чаще, чем женщины.
Причины
На сегодняшний день практическая неврология как наука не располагает достоверными сведениями о этиологии и патогенезе невральной амиотрофии. Проведенные исследования показали, что у 70-80% пациентов с ШМТ, прошедших генетическое обследование, отмечалось дублирование определенного участка 17-й хромосомы. Определено, что невральная амиотрофия Шарко-Мари-Тута имеет несколько форм, вероятно обусловленных мутациями различных генов. Например, исследователи выяснили, что при форме ШМТ, вызванной мутацией кодирующего митохондриальный белок гена MFN2, происходит образование сгустка митохондрий, нарушающего их продвижение по аксону.
Болезнь Шарко-Мари-Тута характеризуется аутосомно-доминантным наследованием с пенетрантностью на уровне 83%. Встречаются также случаи аутосомно-рецессивного наследования.
Патогенез
Установлено, что большинство форм ШМТ связаны с поражением миелиновой оболочки волокон периферических нервов, реже встречаются формы с патологией аксонов — осевых цилиндров проходящих в центре нервного волокна. Дегенеративные изменения затрагивают также передние и задние корешки спинного мозга, нейроны передних рогов, пути Голля (спинномозговые проводящие пути глубокой чувствительности) и столбы Кларка, относящиеся к заднему спинномозжечковому пути.
Вторично, в результате нарушения функции периферических нервов, развиваются мышечные атрофии, затрагивающие отдельные группы миофибрилл. Дальнейшее прогрессирование болезни характеризуется смещением ядер сарколеммы, гиалинизацией пораженных миофибрилл и интерстициальным разрастанием соединительной ткани. В последующем нарастающая гиалиновая дегенерация миофибрилл приводит к их распаду.
Классификация
В современной неврологической практике невральная амиотрофия Шарко-Мари-Тута подразделяется на 2 типа. Клинически они являются практически однородными, однако имеют ряд особенностей, позволяющих провести такое разграничение.
Отмечена связь болезни Шарко-Мари-Тута и атаксии Фридрейха. В отдельных случаях у пациентов с ШМТ со временем отмечаются типичные признаки болезни Фридрейха и наоборот — иногда по прошествии многих лет клиника атаксии Фридрейха сменяется симптоматикой невральной амиотрофии. Некоторыми авторами даны описания промежуточных форм этих заболеваний. Наблюдались случаи, когда у одних членов семьи диагностировалась атаксия Фридрейха, а у других — амиотрофия ШМТ.
Симптомы
В отдельных случаях невральная амиотрофия манифестирует расстройствами чувствительности в стопах, наиболее часто — парестезиями в виде ползания мурашек. Типичным ранним признаком ШМТ является отсутствие ахилловых, а позже и коленных сухожильных рефлексов. Основной симптом, на который пациенты чаще всего сами обращают внимание – приступообразные болезненные сокращения в икроножных мышцах (крампи), усиливающиеся в ночное время или после длительной физической нагрузки.
Развивающиеся первоначально атрофии затрагивают в первую очередь абдукторы и разгибатели стопы. Результатом является свисание стопы, невозможность ходьбы на пятках и своеобразная походка, напоминающая вышагивание лошади, — степпаж. Далее поражаются приводящие мышцы и сгибатели стопы. Тотальная атрофия мышц стопы приводит к ее деформации с высоким сводом, по типу стопы Фридрейха; формируются молоткообразные пальцы стопы. Постепенно атрофический процесс переходит на более проксимальные отделы ног — голени и нижние части бедер. В результате атрофии мышц голени возникает болтающаяся стопа. Из-за атрофии дистальных отделов ног при сохранности мышечной массы проксимальных отделов ноги приобретают форму перевернутых бутылок.
Зачастую при дальнейшем прогрессировании болезни Шарко-Мари-Тута атрофии появляются в мышцах дистальных отделов рук — вначале в кистях, а затем и в предплечьях. Из-за атрофии гипотенара и тенара кисть становиться похожей на обезьянью лапу. Атрофический процесс никогда не затрагивает мышцы шеи, туловища и плечевого пояса.
Часто невральная амиотрофия Шарко-Мари-Тута сопровождается легкими фасцикулярными подергиваниями мышц рук и ног. Возможна компенсаторная гипертрофия мышц проксимальных отделов конечностей. Сенсорные нарушения при невральной амиотрофии характеризуются тотальной гипестезией, однако поверхностная чувствительность (температурная и болевая) страдает значительно больше глубокой. В некоторых случаях наблюдается цианоз и отек кожи пораженных конечностей.
Для болезни Шарко-Мари-Тута типично медленное прогрессирование симптомов. Период между клинической манифестацией заболевания с поражения ног и до появления атрофий на руках может составлять до 10 лет. Несмотря на выраженные атрофии, пациенты длительное время сохраняют работоспособное состояние. Ускорить прогрессирование симптомов могут различные экзогенные факторы: перенесенная инфекция (корь, инфекционный мононуклеоз, краснуха, ангина, ОРВИ), переохлаждение, ЧМТ, позвоночно-спинномозговая травма, гиповитаминоз.
Осложнения
Невральная амиотрофия Шарко-Мари-Тута характеризуется ранней инвалидизацией. Вследствие прогрессирующей атрофии дистальных отделов конечностей и выраженных нарушений чувствительности больные постепенно теряют способность к самостоятельной ходьбе. Из-за грубых деформаций кистей рук пациенты не могут сами себя обслуживать. Контрактуры суставов нередко требуют хирургической коррекции.
На ранней стадии заболевания слабость в мышцах ног, гипестезия и гипорефлексия приводят к частым падениям, что повышает вероятность травм и переломов. Наиболее грозные неблагоприятные последствия происходят при сочетании болезни Шарко-Мари-Тута и атаксии Фридрейха. К ним можно отнести слепоту, кардиомиопатию, дыхательную недостаточность.
Диагностика
Курацией пациентов занимаются врачи-неврологи и ортопеды. При опросе больного уточняется возраст, в котором начали появляться симптомы (для болезни ШМТ типична манифестация в 15-25 лет). Важное значение имеет семейный анамнез (наличие близкого родственника с этой патологией). Во время общего осмотра обращается внимание на изменение походки, деформацию стоп и кистей.
При неврологическом осмотре отмечается уменьшение тонуса дистальных отделов верхних и нижних конечностей, ослабление или полное отсутствие сухожильных рефлексов (ахилловых, коленных), снижение кожной чувствительности. Для уточнения диагноза проводятся следующие методы исследования:
Дифференциальный диагноз невральной амиотрофии Шарко-Мари-Тута необходимо проводить с наследственными нейромышечными заболеваниями (спинальная мышечная атрофия Верднига-Гоффмана, адренолейкодистрофия, болезнь Пелицеуса-Мерцбахера) и приобретенными хроническими полинейропатиями (синдром Гийена-Барре).
Лечение невральной амиотрофии Шарко-Мари-Тута
Медикаментозная терапия
Для прохождения лечения все больные подлежат обязательной госпитализации в стационар. В настоящее время не существует специфической терапии, способной замедлить прогрессирование аксональной дегенерации и демиелинизации. Однако своевременно начатая грамотная и индивидуально подобранная терапия способна значительно улучшить качество жизни пациентов. Из лекарственных препаратов для симптоматического лечения невральной амиотрофии ШМТ применяются:
Немедикаментозная терапия
Основное внимание уделяется немедикаментозному лечению невральной амиотрофии Шарко-Мари-Тута. Для достижения максимального терапевтического эффекта применяется комплекс следующих мероприятий:
Комплексное проведение данных мероприятий позволяет увеличить мышечную силу, исправить нарушения равновесия и походки. Благодаря этому удается повысить бытовую, социальную адаптацию, работоспособность пациентов.
Хирургическое лечение
При выраженных атрофических явлениях и деформации стопы, значительно затрудняющих самостоятельную ходьбу, когда консервативные методы оказываются безуспешными, показаны ортопедические оперативные вмешательства – метатарзальная остеотомия, остеотомия пяточной кости. В некоторых случаях для восстановления опорной функции стопы может понадобиться проведение артродеза.
Экспериментальное лечение
Продолжаются поиски эффективного лекарства для борьбы с невральной амиотрофией Шарко-Мари-Тута. В клинических испытаниях, где пациенты принимали препарат PXT3003 (комбинация малых доз баклофена, налтрексона и сорбитола), были отмечены положительные результаты в виде увеличения мышечной силы, возобновления чувствительности и сухожильных рефлексов.
Рассматривается возможность использования в качестве лечения ингибиторов HDAC6 – ферментов, стимулирующих регенерацию белков цитоскелета нервных клеток. Эксперименты на лабораторных животных показали, что данные вещества способны значительно замедлить прогрессирование демиелинизации и аксональной дегенерации.
Прогноз и профилактика
Невральная амиотрофия Шарко-Мари-Тута – тяжелое инвалидизирующее заболевание. Большинство пациентов утрачивают способность ходить через 15-20 лет после начала появления симптомов. Однако в виду того, что преимущественно поражаются дистальные отделы конечностей, продолжительность жизни больных практически не отличается от таковой в общей популяции.
Летальные исходы в молодом и среднем возрасте наблюдаются при сочетании с атаксией Фридрейха, когда в патологический процесс вовлекается дыхательная мускулатура и миокард. Специфических методов первичной профилактики не существует. Предупредить развитие осложнений и максимально сохранить работоспособность позволяет своевременное начало комплексной терапии.